Gliomas de alto grado
la doctora Mª Teresa García Campos +info
+Linkedin de la doctora
Introducción a los gliomas de alto grado
Los tumores primarios del SNC constituyen el 2% del total de las neoplasias del adulto y el 20% de los niños y de ellos el grupo más frecuente son los gliomas.
Se trata de tumores de origen neuroectodérmico que nacen a partir de las células gliales y pueden encontrarse a lo largo de todo el sistema nervioso.
En función del tipo de célula de la que provenga tenemos diferentes tipos de tumores
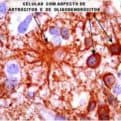
El sub-grupo más frecuente y más importante es el de los astrocitomas que constituyen el 60% y de ellos un 80% son grado IV es decir Glioblastomas multiformes(GBM).
Sobre este tipo de tumores destacar, como ya es sabido, que no existe curación y que la supervivencia sin tratamiento en el caso del GBM es inferior a 6 meses.
Evolución en el tratamiento:
Por lo descrito anteriormente, ha habido a lo largo de los años diferentes intentos de mejorar el tratamiento, destaca Walter Dandy a principios del s XX, el cual, en un intento de curarlos llevó a cabo las hemisferectomías, pero, incluso en estos pacientes hubo recurrencias en el otro hemisferio.
Durante la segunda mitad del siglo XX la tendencia fue a no operar gliomas localizados en zonas profundas o elocuentes, el motivo del cambio en la forma tratar estos tumores fue que se dieron cuenta del grado de agresividad de los gliomas a pesar de una cirugía extensa, y de la morbilidad que esta generaba, llegando a realizar en su mayoría biopsias abiertas o estereotáxicas
Con esta premisa se intervenían solo tumores de localización frontal o temporal.
La aparición de los primeros sistemas de navegación en los 80 basados en la localización tridimensional con un marco de estereotaxia permitió realizar abordajes con mayor seguridad, guiando al neurocirujano en la trayectoria a través del sistema nervioso.
Fue también en esa época tras la llegada de la Tomografía axial Computarizada y su utilización sistemática para obtener información en 3D del tumor, cuando la radioterapia conformada tridimensional RTC3D comienza a estandarizarse para los tratamientos con intención curativa. La posibilidad de planificar en 3D permite diseñar haces de irradiación para obtener distribuciones de dosis con la forma del tumor.
Como agentes quimioterápicos a destacar entre otros, en primer lugar, tendríamos la temozolamida, aunque la comercialización de éste se inició en 1998, su uso en GBM en concomitancia con radioterapia, no se estandarizó hasta el 2005 cuando Stupp y colaboradores, publicaron sus resultados finales en un grupo de pacientes con glioblastoma, a los que, la administración de Temozolamida (TMZ) concomitantemente con radioterapia como tratamiento de primera línea, prolongó la supervivencia, demostrando su seguridad y eficacia
Otros agentes quimioterápicos que se están utilizando serían los implantes de carmustina o gliadel o el bevacizumab, son tratamientos de segunda línea útiles en recidivas.
Con todo ello, la tendencia quirúrgica a seguir es la de la resección radical como veremos posteriormente.
Pese a ello, continúa habiendo tumores no candidatos a la extirpación completa ya sea por su extensión o localización anatómica, esto fue descrito por el Dr Gazi Yasargil, posiblemente el considerado padre de la Neurocirugía moderna, que define lo que en la mayoría de los casos suponen tumores irresecables, como son los de localización en TE, cuerpo calloso, septales difusos, bilaterales.
Pronóstico:
Con todas las armas de las que disponemos, podemos ver que la supervivencia va aumentando con los diferentes tratamientos, de forma que, sin tratamiento la supervivencia de los gliomas de alto grado es menor 6 meses e incluso en algunos casos menor a 3, con biopsia y RT es 8,8 , biopsia+RT+QT 14,6 meses con una proporción de supervivencia a los 2 años del 26,5%, con la resección parcial + terapia adyuvante es de 16,6 meses y que la supervivencia global con resección macroscópica radical+RT+QT es de 18,7 meses incluyendo cirugía de rescate.
En el caso de GBM recurrente,está demostrado el aumento de supervivencia con resección radical al menos una vez y con resecciones mayores que 80%.
Factores pronósticos:
No debemos olvidar que hay diferentes factores que modifican el esquema de tratamiento y que influyen de forma significativa en la supervivencia.
Estos factores serían la edad, el estado funcional del paciente según la escala de Karnosfky en la que se determina de 0 a 100 el estado general del paciente, de forma que en un Karnofsky de 100 la persona es autónoma e independiente y en uno de 50 el paciente es dependiente para las actividades de la vida diaria.
Otros factores pronósticos serían las características de la imagen preoperatoria y la histología inicial que determina mayor o menor grado de agresividad y el grado de resección llevada a cabo en la cirugía.
Pero ¿realmente es necesario hacer una resección radical?
Para responder a esta pregunta debemos acudir a la literatura:
En el estudio EORTC-NCIC study 26981-22981 european organisation research treatment cancer resecciones radicales + RT+QT consiguieron aumentar la supervivencia 4,1 meses comparada con resecciones parciales (+1,8 meses).
También obtuvieron una supervivencia dos meses mayor en pacientes con RT+QT que con RT solo.
Además, los pacientes con resección completa se beneficiaron de forma más significativa de la RT y QT concomitante llegando a la conclusión de que la resección completa aumenta la supervivencia e incrementa la eficacia de la terapia adyuvante.
En otro estudio prospectivo en el que se evaluó el grado de resección mediante RM postop y la influencia de la misma en la supervivencia, se dedujo que pacientes con tumor residual tienen 6,6 veces más riesgo de muerte que en pacientes con resección completa y que la RT disminuye el riesgo de muerte en relación a pacientes sin RT
Pacientes sin tumor residual en RM postooperatoria tiene mayor supervivencia que aquellos con tumor residual 17,9 meses vs 12,9 meses p<0,001.
También Sanai y Berguer en el 2009, señalaron, al examinar una serie de 28 artículos sobre gliomas de alto grado publicados, y 10 de bajo grado que, a pesar de la ausencia de evidencia clase I, una resección segura y lo más radical posible de los tumores malignos es imprescindible para lograr una mayor supervivencia.
Pero ¿A qué llamamos resección radical?
Según un estudio sobre 416 pacientes intervenidos de GBM entre 1993 y 1999 la resección de al menos el 98% de la lesión aumenta la supervivencia de 8,8 a 13 meses p < 0.0001 especialmente cuando otros factores pronósticos, como el estado funcional, edad…son favorables.
También está demostrado que al menos una resección del 89% determina una mejoría significativa de los síntomas.
Sabemos que un mayor grado de resección se asocia a una supervivencia más elevada, pero ahora bien, está resección no está exenta de dificultad para el cirujano
Diferentes estudios señalan el porcentaje de veces en el que en el cirujano asegura haber conseguido una resección macroscópica completa y haber encontrado restos tumorales captantes de contraste en la RM postoperatoria.
Una carta al editor escrita a raíz del Congreso de ASNR (American Society of Neuroradiology) del 2001 señala que en algunos casos ese porcentaje llega a ser del 80%.
Pero ¿Porqué existe esta dificultad?
Esto es debido a que, a diferencia de otros tumores, el tejido tumoral glial no se reconoce fácilmente durante la cirugía y a que las células cancerosas tienen la capacidad de infiltrar el tejido circundante.
Por ello, a través de los años han ido apareciendo nuevos avances con la finalidad de ayudar y complementar la destreza del cirujano.
Entre ellos se encuentran:
- La neuronavegación, ya mencionada anteriormente
- La RMi
- La ultrasonografía y
- El ácido 5 aminolevulínico o gliolán
La neuronavegación es una herramienta que proporciona al neurocirujano una guía continua durante la cirugía con la cual se pueden planificar craneotomías o trayectorias dentro del cerebro a través de un sistema de triangulación satelital.
Para ello, se realizan estudios por imágenes, TAC y/o RMN cerebral del paciente bajo un protocolo especial, esta información es transferida al neuronavegador, el cual, con la ayuda de un programa permite localizar y “pintar” la lesión, planificar trayectorias y abordajes, etc .
Una vez obtenido esto, y con el paciente en quirófano, se hace un reconocimiento inalámbrico del contorno de ciertas estructuras anatómicas del paciente (nariz, ojos, tabique nasal, etc),así, a través de un sistema de referencia fijo y un lector infrarrojo, se detecta continuamente nuestros movimientos y se reconstruye las imágenes del cerebro en forma tridimensional (axial, coronal y sagital).
Sin embargo, a pesar de la ayuda y de lo que significó la llegada de la neuronavegación, ésta tiene sus limitaciones.
Y estos se deben principalmente al fenómeno “brain shift” que no es más que la distorsión de la anatomía intraoperaoria comparada con la que vemos en la imagen, esto ocurre tras la apertura de la duramadre y determina, junto con la ausencia de plano de clivaje entre la corteza sana y el tumor, que esta herramienta no nos permita conseguir una resección radical.
La RM intraoperatoria solventa estos problemas en parte al permitir localizar restos de tejido tumoral y extirparlos en el mismo acto quirúrgico, sin embargo, su elevado coste y la ausencia de infraestructuras dificultan su uso extendido.
Ácido 5 Aminolevulínico (5-ALA):
Se trata de una molécula intracelular utilizada por Stummer en 1998.
Es un precursor bioquímico natural del hemo que se metaboliza en la mitocondria a porfirinas fluorescentes como la protoporfirina IX.
Tiene una absorción intestinal activa y atraviesa mal la barrera hematoencefálica sana, pero bien la alterada.
La administración sistémica de 5-ALA provoca una sobrecarga del metabolismo celular de las porfirinas y la acumulación de PPIX en algunos epitelios y en las células de los gliomas de alto grado, siendo su concentración significativamente más alta en el tejido maligno que en el cerebro normal.
Al utilizar una luz azul (longitud de onda de 400 nm) la PPIX es intensamente fluorescente.
Se usa para gliomas de alto grado (III, IV) y se administra a dosis 20 mg/kg vía oral 3 horas antes de la inducción anestésica disolviendo un vial en 50 ml de agua.
Es importante recordar que es necesaria protección ocular y cutánea durante 24 horas.
En un estudio de 30 pacientes con diagnóstico de GBM intervenidos con 5 ALA se recogieron muestras de la zona de mayor captación, otras de la interfase entre tejido tumoral y sano con menor captación, y muestras de zonas no captantes, el resultado anatomopatológico fue que las zonas con captación más intensa correspondían a tumor sólido con alta celularidad atipia, mitosis y proliferación vascular.
Las zonas con captación rosa revelaban zonas con atipia sin proliferación vascular con menor densidad celular, y las zonas no captantes: tejido con baja celularidad.
Así, podríamos clasificar, en función de la fluorescencia, que las zonas de más captación en rojo corresponden a tumor sólido, que las zonas que se tiñen de rosa corresponden a células tumorales infiltradas o borde invasivo y que el tejido sano se ve de color azul.
Destacar también que el tejido necrótico no se tiñe y que algunas estructuras como los plexos coroides se tiñen de color rosáceo.
Una vez más, debemos recurrir a la literatura científica para comprobar si realmente el uso de gliolán aporta alguna ventaja:
En un estudio observacional retrospectivo, realizado sobre 322 pacientes con sospecha de glioma de alto grado en el que la mitad fueron intervenidos con 5ALA y el otro 50% con luz convencional, se observó, que la ausencia de lesiones captantes de contraste en RM postoperatoria en los pacientes con 5ALA fue del 65% frente al 47% en los pacientes intervenidos con luz convencional, eso se tradujo en una supervivencia a 6 meses dos veces mayor que en pacientes intervenidos con luz blanca.
El tiempo para las reintervenciones también fue significativamente mayor en pacientes intervenidos por primera vez con 5ALA.
También en España encontramos el VISIONA, que se trata de un estudio multicéntrico en el que son evaluados 140 pacientes intervenidos con gliolán, en él, el porcentaje de resecciones completas confirmadas mediante RM con 5-ALA es del 67% frente al 47% p<0,00005. Hay que tener en cuenta que existe disparidad según centros.
Con RMi se han obtenido los mismos resultados.
Con todo ello podemos concluir que entre las ventajas del uso del gliolán estarían que:
– No tiene efecto biológico sobre el tumor
– Se trata de una herramienta para el neurocirujano
– Existe evidencia de que mayor resección tumoral beneficia al paciente
– El uso de 5-ALA conlleva una mayor frecuencia de resección radical
Como inconvenientes podríamos señalar la fotosensibilidad y la morbilidad añadida en caso de tumores de localización cercana a áreas elocuentes.
Como efectos secundarios, descritos en caso de sobredosificaciones e intoxicación se han visto náuseas, hopotensión, vómitos y elevación de enzimas hepáticos.
Contraindicaciones:
– Fotosensibilidad
– Alergia
Primun non nocere
Es lógico pensar, que si queremos aumentar la supervivencia de estos pacientes, no debemos añadir ninguna morbilidad añadida por la cirugía.
Como cualquier herramienta que añade la facilidad para realizar resecciones radicales, el uso de 5-ALA conlleva mayor riesgo de daño neurológico al introducirnos en áreas elocuentes.
Una revisión del 2011 del estudio de Stummer, señala la aparición de nueva focalidad en un 26% de los casos a consecuencia del uso del 5-ALA, esto se debe a la resección de estructuras limítrofes que te tiñen de rosa y que corresponden a áreas funcionales.
Para evitar este perjuicio para el, utilizamos la neurofisiología intraoperatoria.
que nos permite identificar la función cerebral continua en el tiempo, percibiendo cambios en la función monitorizada y de esta manera, alertar al neurocirujano para cambiar de estrategia quirúrgica.
A este respecto, hallamos un estudio prospectivo publicado en el 2010 en Neurosurgery, en él, se incluyen pacientes con tumores cerebrales malignos en áreas elocuentes entre mayo 2007- mayo 2009 con una escala de Karnofsky de al menos del 70% y en los que se utilizó gliolán introperatorio.
Tras la cirugía fueron evaluados con pruebas de imagen periódicas definiendo la supervivencia libre de enfermedad por la progresión tumoral en imágenes.
Durante la cirugía se efectuó registro cortical y subcortical de áreas funcionales y haces alrededor de las lesiones.
En las 25 intervenciones realizadas sobre 18 pacientes se observó una supervivencia libre de progresión superior a 6 meses en el 83% de los pacientes.
En 6 de las cirugías la resección se paró por la identificación de área funcional y en dos casos la hemiparesia aumentó tras la intervención.
La escala Karnosfky fue del 90% antes y del 89% tras la cirugía.
El 5ALA fue bien tolerado, sin efectos adversos, exhibiendo fluorescencia en todos los pacientes, incluyendo las recidivas. El resultado histopatológico fue en todos de gliomas de alto grado.
Muchos estudios se centran en conseguir la resección total del tumor, pero olvidan el alto riesgo de déficit neurológico que conlleva sobre todo en áreas elocuentes.
Se podría decir, que el uso de neurofisiología limita las ventajas del 5ALA pero se debe pensar como una herramienta más de seguridad y de eficacia en estos pacientes.
Nuestra experiencia:
Como decíamos anteriormente, con la llegada del microscopio de última generación, a fecha de octubre del 2012, hemos utilizado en estos últimos meses el 5ALA en 8 pacientes.
3 de ellos son mujeres y 5 varones con edades comprendidas entre los 28 y 80 años con una mediana de 57,5 años.
2 de ellos se encontraban a nivel frontal, 2 en zona parietal, 3 en zona temporal y uno en cerebelo.
4 de ellos eran recidivas de glioma, y en dos de ellos era primera intervención.
A todos ellos se les trató con cirugía+ RT+ QT, en caso de reintervenciones en 3 de ellos se les implantó carmustina local.
Método:
– Se administró 5-ALA 20 mg/kg oral 3 horas antes de la inducción anestésica.
– Con protección ocular y cutánea durante 24 horas
– Se llevó a cabo la resección de tumoración con microscopio con técnica de fluorescencia (pentero- Zeiss)
o Luz blanca para resección general
o Luz azul en los límites
– Se utilizó monitorización neurofisiológica en localizaciones elocuentes
– Anestesia general
– Durante la intervención se recogieron 3 muestras, el tumor, muestra de la zona que más se iluminaba y muestra de la zona que no se teñía con luz azul
– Control de RM a las 48-72 horas de la cirugía en 7 de ellos
– Se continuó el tratamiento postirugía según el esquema Stupp
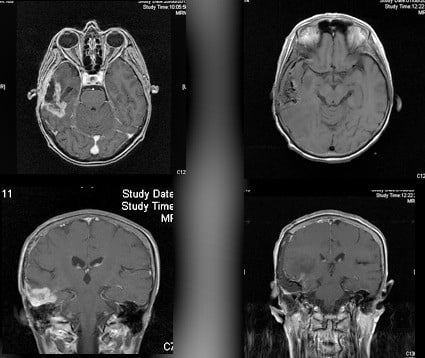
En las imágenes de la izquierda podemos ver la RM preoperatoria, en la que se ve en este caso, una recidiva de un Gliosarcoma temporal derecho y a continuación vemos la RM postoperatoria donde no se aprecia captación de contraste.
A continuación podemos ver imágenes intraoperatorias de ese paciente, donde podemos observar una foto del tumor con luz azul (arriba a a la izquierda).
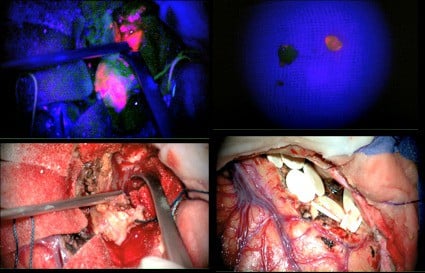
Hay que tener en cuenta, que a la hora de tomar la imagen, ésta pierde un 20% de luz, y que desde el visor del cirujano se aprecia más la fluorescencia.
Debajo vemos la misma imagen con luz blanca mientras resecamos el tumor, y arriba a la derecha vemos dos fragmentos del tumor, uno de la zona que captaba y otro no captante que se correspondían, según el informe anatomopatológico, con zonas de alto grado y zona de necrosis, la siguiente foto es justo antes del cierre en el que se aprecian implantes de carmustina sobre el lecho quirúrgico.
La siguiente paciente tiene una recidiva de un astrocitoma grado III en hemisferio cerebeloso izquierdo, con luz azul el tejido tumoral se teñía de rosa, y a continuación podemos apreciar la RM postoperatoria.
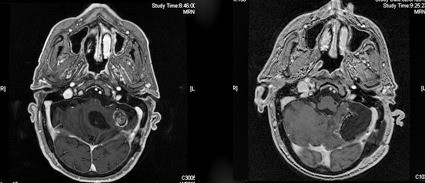
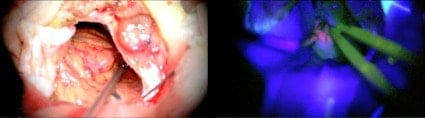
Estas son imágenes del mismo paciente, en el que se aprecia la muestra tumoral una vez resecado con áreas de necrosis y donde al final se aprecia el lecho quirúrgico sin zonas de captación.
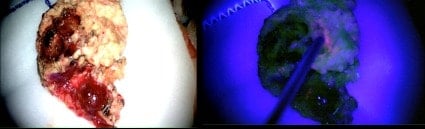
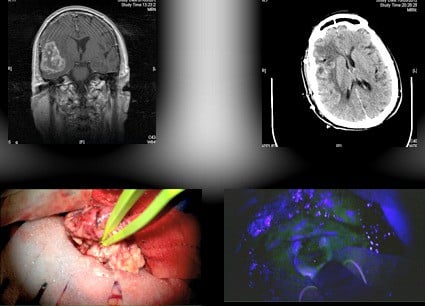
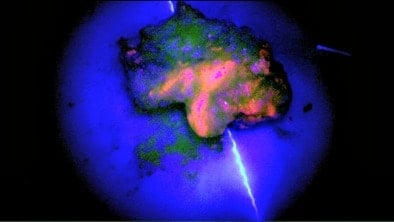
El siguiente paciente tiene una loe frontotemporal derecha, no disponemos de RM postoperatoria pero si de TAC de control, en las imágenes se aprecia la fluorescencia del tumor y como, una vez resecado, no hay fluorescencia en el lecho, la última imagen muestra el tumor iluminado con luz azul
Los informes anatomo-patológicos fueron de:
– 6 GBM
– 2 Astrocitoma grado III
Como resultados destacan:
- Una intensa captación en GBM y astrocitomas grado III
- La ausencia de complicaciones por el uso de 5-ALA
- No se produjo focalidad neurológica de nueva aparición
Conclusiones:
- El tratamiento de los gliomas malignos supone un reto para la medicina actual debido a su frecuencia y agresividad.
- Mayor grado de resección eleva la supervivencia.
- Las armas terapéuticas actuales a nuestra disposición, como el 5-ALA, permiten obtener un porcentaje elevado de resecciones macroscópicas radicales.
- El 5-ALA es útil en recidivas.
- Se debe utilizar la neurofisiología intraoperatoria en aquellas lesiones próximas a áreas elocuentes para evitar un aumento de la morbilidad.
- El objetivo final es aumentar la supervivencia de los pacientes y mejorar su calidad de vida.

En noviembre del 2025 me operaron de un tumor y en los resultados de patología salió que era oligodendroglioma grado 3 y actualmente estoy en radioterapia llevado 15 de 30 sesiones con quimioterapia en pastillas temozolomida 140gr de lunes a viernes y quisiera saber cuál es la esperanza de vida que tengo y si voy a vivir pero con una calidad mala al grado de no poder valer me por mi mismo ?
Actualmente tengo 26 años
Hola Soy Monse de México A mi hermana le detectaron un astrocitoma hace ya 3 años en esa ocasión se realizó la cirugía y todo regresó a la normalidad, la Dra nos dijo que no eran necesarias Radios ni quimios ya que era un tumor grado II “Benigno”, nos dijo que este tipo de tumores tienden a crecer y cambian de fase así que cuando esto empezara ahí era donde iniciarías con tratamientos oncologicos. Todo venía marchando de maravilla hasta que el año pasado mi hermana se embarazó y empezamos este proceso, convulsiones mes a mes, hospitalizaciones, estudios y la… Leer más »
LO SIENTO EN EL ALMA : TENGO UNA AMIGA MUY CERCANA Y LO ESTAMOS VIVIENDO SU DETERIORO POR DESGRACIA. :
TODO MI APOYO Y SOBRE TODO VIVIR POR ESA CRIA MARAVILLOSA QUE TRAJO AL MUNDO.
MI APOYO DESDE MALAGA. yolrm@hotmail.com
Buen día soy Karina de Buenos Aires Argentina. A mi mamá le realizaron la cirugía de glioblastoma multiforme el 7 de julio con resección total, ella tiene 73 años y ahora la flia estamos repensando si va a ser mejor o no realizarse quimio y radio que es lo indicado a seguir Ella quedó con secuelas en el hemisferio derecho que no puede mover , dificultades en habla y usa pañales. Ella era una mujer activa que amaba cocinar para sus nietos que eran su debilidad Al salir de la cirugía nos encontramos con otra mamá pero hoy por hoy… Leer más »
Hola Karina, a mi papá de 77 años una personal totalmene funcional, hasta que inició con problmeas de lenguaje, fue entoces que le detectaron tumor celebral, le quitaron glioblastoma grado IV, salio relativamente bien de la cirugía, lamentablemente conforme se aculmularon las radioterapias y quimio, la calidad de vida fue disminuyendo, al ser pacientes imunosuprimidos empiezan a salir padecimientos de unos y otros, con todas estas complicaciones realmente su final fue devastador, el último mes iniciamos con cuidados paliativos, posterior a la cirugía solo vivió 4 meses muy díficiles. Si yo hubiera tenido idea de todo lo que pasaría, definitivamente… Leer más »
Hola Karina. Mi mama tiene 69 estoy en la misma situacion q tu. Asi mismo como era tu mama era la mia y a veces las personas me preguntan si era mejor no haberla operado? Yo iba a empezar el tratramiento de la radioterapia. Normalmente el tratamiento debe de empezarse despues de operada en la 5 ta o 6 ta semana. Por problemas del hospital las radioterapias iban a comenzar en la 7ma semana. Y cuando le hicieron el TAC tiene edema cerebral y segun ellos tiene o restos del tumor o un tumorcito nuevo. Me explicaron q darle unas… Leer más »
Hola Karina, entre a esta pagina buscando inforamción. Entiendo tu preocupación, mi mamá también tiene 73 años y le hicieron la cirugia el 5 de agosto, tenemos la misma duda si iniciar RT y QT. Si alguien nos puede contar su experiencia sería maravilloso.
Hola Luz Adriana, la experiencia que nos tocó vivir con mi papá de 77 años, fue muy díficil, iniciamos con quimio y radio (3 semanas) porque teníamos la esperanza de poder salvar su vida, y porque nos negamos en aceptar la realidad, pero si hubiera tenido idea de que la radio y la quimio traerían tantas consecuencias negativas en su calidad de vida, y con pocas expectativas de vida, no lo habría sometido a esos tratamientos, reconozco que fue un gran error, a pesar de que lo hice con la mejor de las intenciones, pido perdón a mi padre desde… Leer más »
Hola Luz Adriana le respondi a Karina espero te sirva a ti tambien. A mi mama la opere el 1 de agosto. Ahora estoy a su lado todo el tiempo, mimandola y dandole mucho amor y cariño. Pienso q Dios nos ha dado la oportunidad de poder despedirnos de ellas y poder hacer lo mismo q ellas hicieron por nosotras cuando eramos niñas.
Me duele mucho pq mi mama identica a la de Karina, excelente madre, buena hija, hermana y abuela y tiene muchos amigos q la adoran. Espero q el final no sea tan duro.
Hola a todos, por mi mente nunca paso que existiera un enfermedad como esta, así empezó todo hace aproximadamente 3 años:: nos dimos cuenta que mi hermana repetí muchas veces la misma pregunta y olvidaba cosas básicas con facilidad. La llevamos al médico, nos remitió a sicologia; diagnósticó que podía ser demencia senil leve, la remitió. Terapia ocupacional y a siquiatría, también dijo puede ser demencia senil o Alzheimer, la remitió a neurología, le mandó hacer resonancia , acudimos a muchísimas terapias de cada especialidad y nada, todos se quedaron en que: puede ser demencia o Alzheimer pero ninguno concretó… Leer más »
Hola, soy stefi . El 21 de abril operaron a mi mamá de un glioma cerebral. Recién hoy nos dijeron que le dan un año de vida. Tengo el corazón destrozado. Nos dieron 30 sesiones de radioterapia y quimio con pastillas, pero leyendo los mensajes no sé qué hacer al respecto, tengo miedo que empeore
Hola, si quieres contactarme y compartimos experiencias en cuanto a esta terrible enfermedad. Se que no todos los casos son iguales pero por lo menos estaremos preparados carmelita1583@hotmail.com
MUCHAS GRACIAS CARMELITA POR TU APOYO.
PERO ESTO ES MUY DURO DE VERAS
Mi madre de 93 años tenía un tumor cerebral glial de alto grado, glioblastoma multiforme. Dijeron que al ser mayor era inoperable y la sedaron para morir. ¿Cree que tenía alguna oportunidad si la hubiesen operado o era demasiado mayor?
Un abrazo. A mi me hace mucha falta. En febrero le diagnosticaron glioblastoma parietal izquierdo a mi compañero de vida, de 75 años. Con cirugía mas rt+q un año o mas de vida, sin cirugía seis meses. Le costaba mucho hablar, ese fue el primer síntoma. A hoy, se agudiza al punto que es muy difícil comunicarse, muy débil duerme harto. Estamos en cuidados paliativos. El desde un inicio quería terminar pronto. No deseo nunca esta agonía atroz de verse y sentirse de esta manera. Es inhumano que no le permitan decidir sobre su vida. La ley de eutanasia aquí… Leer más »
Buen día mi hijo de 45 años ha sobrevivido 8 años con Glioblastoma Multiforme grado IV. Con 3 operaciones y 3 radioterapias Hoy mayo 2025 está en la última etapa terminal. Su médico neurocirujano de Chile lo operó siempre y gracias a el ha sobrevivido todo estos años. Solo darle ánimo a los pacientes jóvenes que están con esta enfermedad que el paciente pone el 100% para vivir aúnque la calidad de vida se va perdiendo paso a paso. Y varias etapas logran vivir unos años más. El deja dos niños hermosos pre adolescentes que han vivido junto a su… Leer más »
Hola, soy de Chile, como puedo contactarte? Necesito de tu orientación con el neurocirujano, por favor.
Hola no podría decir buenas noches pero he leído los comentarios y quiero narrar lo vivido con mi padre que también fue diagnosticado con Glioblastoma cerebral grado IV el tiene 64 años y me duele profundamente ver como esta enfermedad se ha llevado a mi padre, el fue diagnosticado en septiembre del 2024 estuvo en EEUU pero regreso a Perú ya que nosotros (su familia) vivimos aquí… comenzó sus tratamientos en enero del 2025 y lamentablemente los tratamientos nose si aceleraron la enfermedad aunque el ya tenía un diagnostico difícil, creo que es muy complicado aceptarlo al menos yo siempre… Leer más »
ESTOY LEYENDO LOS COMENTARIOS , YA QUE HACE 15 DIAS OPERARON A MI MARIDO DE GLIOBASTOMA MULTIFORME GRADO 4 , SACARON EL 80 X CIENTO Y AHORA ME HABLAN DE RADIOTERAPIA Y QUIMIO , ESTOY PERPLEJA YA QUE EMPEZO CON DOLOR DE CABEZA Y LO LLEVE ENSEGUIDA A GUARDIA Y ESE MISMO DIA ME DICEN DEL TUMOR DESPUES DE UNA TOMOGRAFIA Y LA VERDAD ES QUE LOS PRONOSTICOA NO SON ALENTADORES 14 , 16 MESES , Y REALMENTE HAY QUE IR PREPARANDOSE PARA LO PEOR , TIENE 67 AÑOS Y NUNCA SUFRIO DE UN DOLOR DE CABEZA, SOY DE TANDIL… Leer más »
Hola María Teresa, soy caro de Buenos Aires. Operaron a mi papá el 4 de abril. No pudieron sacar todo el tumor. Nos dieron la biopsia esta semana, es un gliobastoma de alto grado. 60 años mi papá, estamos devastadas con mi mamá y mis hermanas. Te abrazo