Gliomas de bajo grado. Tratamiento y sus controversias
Introducción
Los gliomas son un grupo de neoplasias del SNC que provienen de células neurogliales (astrocitos, oligodendrocitos…) con varios grados de agresividad. A las lesiones de lento crecimiento nos referimos como gliomas de bajo grado mientras que a las de rápido crecimiento como alto grado. Los de bajo grado son menos comunes, son aproximadamente el 15% de los tumores del SNC diagnosticados en adultos cada año.
El único factor de riesgo, es la exposición a radiación ionizante. Los factores hereditarios no juegan un papel importante aunque estos tumores son más frecuentes en paciente con NF-1 y sd. Fraumeni ( mutación que afecta al gen supresor tumoral TP53).
La principal forma de presentación es en forma de crisis, que ocurren en el 80% de los casos, debido probablemente a la localización superficial y a la baja tasa de crecimiento. La mayoría permanecen asintomáticos incluso aunque tengan efecto masa, los síntomas de HTIC son poco frecuentes.
Los podemos dividir según su histopatología y dependiendo de ésta, el manejo será diferente.
Clasificación de la WHO:
– Astrocitoma difuso grado II
– Oligodendroglioma
– Oligoastrocitoma
– Ganglioglioma
– Gangliocitoma
– Astrocitoma pilocítico
– Xantoastrocitoma pleomorfo
– Tumor neuroepitelial disembrioplásico (DNT)
Clasificación espacial:
– Tipo 1: Tumor sólido sin infiltración de parénquima. Resección completa, pronóstico favorable. Gangliogliomas, astrocitoma pilocítico, xantoastrocitoma pleomorfo, algunos astrocitomas.
– Tipo 2: tumor sólido asociado a infiltración de parénquima alrededor. Resección puede ser posible, depende de la localización. Astrocitomas de bajo grado
– Tipo 3: Tumor infiltrante sin parte sólida. Resección dificultada por riesgo de déficit neurológico. Oligodendrogliomas.
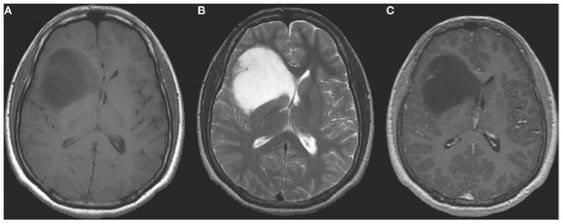
1) Astrocitoma difuso:
Ocurren en adultos, con pico de edad a finales de los 30 años, asientan frecuentemente en los hemisferios cerebrales (temporal, frontal posterior y lóbulo parietal anterior), la mayoría se presentan como crisis. Anaplasia y mitosis ausentes. Infiltran el tejido neural circundante. Mejor pronóstico si ocurre en jóvenes, peor pronóstico si HITC, alteraciones de la consciencia, cambios de personalidad, déficits neurológicos, captación de contraste. Según la histopatología, pueden dividirse en:
- – Fibrilar: surge de la profundidad de la sustancia blanca, es duro y correoso por fibrillas neurogliales que produce. Baja celularidad con mínima atipia nuclear. Es el subtipo más frecuente.
– Gemistocítico: compuesto por células grandes y densas, apariencia de globo. Propenso a progresar de grado de malignidad.
– Protoplásmico: La celularidad es baja y la actividad mitótica está ausente. Es el menos común. Suele surgir de la corteza.
Suelen tener mejor pronóstico que otros astrocitomas difusos.
La mayor causa de morbilidad ocurre con la desdiferenciación a mayor grado. Los fibrilares tienden a transformarse más rápidamente cuando el diagnóstico es >45 años que cuando es antes. El gemistocítico se desdiferencia más rápidamente que el fibrilar.
2) Oligodendroglioma:
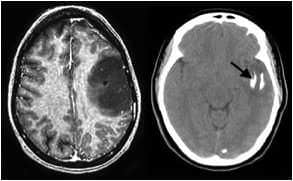
4-8% de los gliomas cerebrales, aunque hay estudios que dicen que están infradiagnosticados.
Hombre:mujer 3:2. Entre 26-46 años, con media de edad a los 40 y con un pequeño pico de edad entre los 6-12 años.
Metástasis en LCR en 10%. La forma de presentación es en forma de crisis en un 50-80%. Calcificaciones se presentan en un 90%. Su localización más frecuente son los lóbulos frontales. Pueden ser de alto (III) o de bajo grado (II).
A pesar de ser tumores infiltrantes, por lo general muestran límites bien definidos, y a ello contribuye su alta densidad celular, lo que hace que el límite con el tejido adyacente sea neto confiriéndoles una falsa apariencia de buena limitación. Es típica la invasión del córtex adyacente, ya que afectan fundamentalmente la sustancia blanca y corteza cerebral adyacente. La consistencia es sólida, aunque pueden presentar áreas de reblandecimiento de aspecto mucoide, e incluso quistificaciones y en un número elevado de casos es posible observar focos de calcificación.
La imagen del oligodendroglioma es monótona, con células de núcleo central redondo. La membrana nuclear es neta y a su alrededor el citoplasma es muy claro y transparente (células en huevo frito) como consecuencia de imbibición de agua durante la fijación del tejido. Esta característica no está siempre presente y cuando se ha congelado previamente la muestra, se pierde y los núcleos se angulan.
3) Oligoastrocitoma:
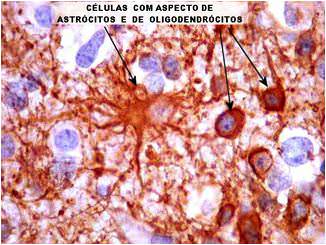
Variante de oligodendrogliomas en los que se pueden identificar astrocitos fibrosos o protoplasmáticos, gemistocitos e incluso astroblastos o espongioblastos, lo que puede ocurrir en alrededor del 50% de los casos. Dichos elementos pueden encontrarse entremezclados o en zonas tumorales separadas. Histológicamente corresponden, al igual que el oligodendroglioma bien diferenciado, a un tumor de bajo grado de malignidad. Pueden ser de alto (III) o de bajo grado (II).
4) Astrocitoma pilocítico:
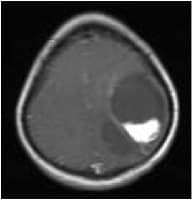
Tumores de lento crecimiento, generalmente delimitados, y frecuentemente quísticos. Generalmente en niños y adultos jóvenes, aunque tb pueden darse en personas de más edad. 85 % se encuentran infratentoriales y 15 % supratentoriales. Más frecuentemente asientan en hemisferio cerebeloso y alrededor del III ventrículo, pero también pueden encontrarse en los hemisferios cerebrales.
Localización:
- – Gliomas hipotalámicos y gliomas ópticos.
– Hemisferios cerebrales: en adultos jóvenes: pueden confundirse con astrocitomas fibrilares, suelen distinguirse por tener un componente quístico con un nódulo que realza contraste y algunos tienen calcificaciones.
– Gliomas de tronco: normalmente son de tipo infiltrante y solo un pequeño grupo son pilocíticos.
– Cerebelo. Forma de presentación: hidrocefalia, alterraciones cerebelosas…
– Médula espinal: raro
Exhiben una patente monomorfa que ha sido llamada pilomixoide y predomina una densa trama de fibrillas gliales con abundantes fibras de Rosenthal. La presencia de proliferación vascular en la histopatología son hallazgos posibles en el astrocitoma pilocítico, y al contrario que en otros gliomas, no son indicativos de malignidad.
Mejor pronóstico que los astrocitomas difusos (supervivencia a los 10 años: 94%).
En TC o RM normalmente están bien circunscritos, 94% realzan contraste, frecuentemente con un componente quístico con un nódulo mural y con poco o nada de edema. A veces tienen calcificaciones.
5) Gangliogliomas:
Células ganglionares procedentes de neuroblastos primitivos y células gliales generalmente astrocitos en cualquier fase de diferenciación. Más frecuentes en el lóbulo temporal, frecuentemente hallazgo en cirugía de la epilepsia tras resección temporal. Curso benigno y rara la transformación maligna. Forma de presentación: crisis.
6) Gangliocitoma:
Los gangliocitomas son tumores de estirpe neuronal que se presentan en individuos jóvenes y niños. Su localización más habitual es supratentorial (lóbulo temporal…). La presentación más habitual es en forma de epilepsia refractaria.
7) Xantoastrocitoma pleomorfo:
Es un tumor de estirpe astrocitaria considerado grado II de la OMS, excepto en los casos con alto índice mitótico o necrosis. Pertenece al grupo de los astrocitomas circunscritos (localizados o no infiltrativos). Tumores generalmente bien definidos y de crecimiento lento. Parecen originarse de astrocitos subpiales o de células precursoras multipotenciales neuroectodérmicas. Surgen con mayor frecuencia a nivel supratentorial en los lóbulos temporales y parietales de los niños y adultos jóvenes con historia clínica de crisis convulsivas, aunque hay reportes de localizaciones poco frecuentes como el cerebelo y la médula espinal. Las características de los estudios de imagen son las de una masa intracortical hemisférica en situación periférica, bien delimitada, con un componente quístico y de nódulos murales, generalmente protruyendo en la meninge. El componente quístico es hipointenso en T1 e hiperintenso en T2 y FLAIR. El componente sólido tiene generalmente una señal intermedia en todas las secuencias con un realce moderado a intenso tras el contraste. La masa puede deformar las meninges adyacentes que se realzan de manera intensa.
8) Tumor neuroepitelial disembrioplásico (DNT):
1 a 2% de los tumores del sistema nervioso central, suele diagnosticarse entre los 20 y 39 años de edad, la localización más frecuente es supratentorial e intracortical, específicamente en el lóbulo temporal, con afección de las estructuras mesiales. Es una neoplasia nodular bien delimitada, los hallazgos microscópicos más frecuentes son neuronas maduras y columnas de células parecidas a oligodendrocitos dispuestas en una matriz de mucina o “componente glioneuronal específico”. Cuando solamente se observa este componente se denomina “forma simple” y cuando se asocia con nódulos neurogliales o displasia cortical,“forma compleja”. La lesión suele tener crecimiento mínimo o nulo, pues su potencial de proliferación es de 0 a 8%, por lo que se clasifica como lesión de comportamiento benigno y, según la OMS, neoplasia de grado I. La manifestación más común se relaciona con crisis convulsivas parciales de difícil control.
T1 hipointenso, T2 hiperintenso.
Diagnóstico:
Se basa en la clínica y en las pruebas de imagen.
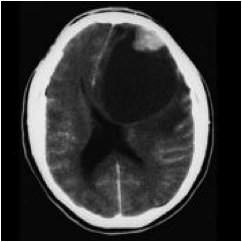
Alta probabilidad de glioma de bajo grado cuando presenta déficits neurológicos pasajeros con crisis, en pruebas de imagen lesión que no realza contraste y produce ligero efecto masa, en RM se ven mejor en secuencias T2, no realzan con gadolinio en T1. La clínica la puede dar la localización del tumor o por HTIC.
Controversias en tratatmiento de los gliomas de bajo grado:
– Tratamiento agresivo inmediato vs intervención diferida en pacientes con enfermedad limitada y sintomáticos.
– RT/QT: terapia adyuvante tras cirugía o solo si hay evidencia de progresión.
Manejo inicial:
1) Cirugía:
Objetivos de la cirugía: confirmación histológica, mejoría neurológica del paciente, reducir el riesgo de crecimiento del tumor, prevenir la transformación maligna.
En pacientes con gliomas de bajo grado, la cirugía nos da un diagnóstico histológico y a su vez, puede ser terapéutica. En pacientes donde es posible una resección radical, la cirugía puede ser el único tratamiento. La resección total a menudo no es posible llevarla a cabo sin secuela neurológicas por la naturaleza infiltrativa del tumor. En estas situaciones está indicada RT y QT neoadyuvante. En pacientes con buen pronóstico (jóvenes, solo presentan crisis) la observación tras la resección es una opción terapéutica.
Factores asociados a peor pronóstico: tumores >4cm, astrocitomas u oligoastrocitomas peor que oligodendroglioma, enfermedad residual > 1cm en RM.
El uso de RT/QT en estos pacientes es incierto, pero normalmente se pospone hasta que haya progresión.
2) Tiempo de resección:
Cirugía inmediata se realiza en pacientes con grandes masas o síntomas neurológicos, tanto para diagnóstico histológico como para disminuir la lesión. En paciente con tumores pequeños y síntomas mínimos hay controversia.
Muchos neurocirujanos están a favor de una resección máxima y segura en el momento del diagnóstico para todos los pacientes con gliomas de bajo grado basados en revisiones de la literatura que indican que mejoran el pronóstico.
Otros cirujanos son más conservadores en paciente con lesiones pequeñas y con crisis como único síntoma. En estos casos, la cirugía agresiva y RT se dejan hasta que haya evidencia de crecimiento del tumor, crisis intratables, deterioro progresivo neurológico, o evidencia radiográfica de transformación a alto grado. Sin embargo en estos casos, puede haber un porcentaje de pacientes no candidatos ya a cirugía debido a la progresión.
No hay estudios aleatorizados que comparen pacientes operados con pacientes en los que se haya retrasado la cirugía hasta que haya evidencia de progresión clínica o deterioro neurológico. Los datos que hay sobre esto son de estudios observacionales, hay una cohorte retrospectiva que buscó compara la cirugía temprana con la diferida en 2 centros de Noruega, se estudiaron 153 pacientes con gliomas de bajo grado, en un centro se realizó una máxima resección segura (se hizo en el 86% del los pacientes) y en el otro se hizo biopsia diagnóstica y se esperó (se hizo en el 71% de los pacientes, con un 50% de resección finalmente). La supervivencia fue mayor en el grupo de resección temprana (74 vs 60 % de supervivencia a los 5 años), aunque esto puede ser debido a la alta tasa de resección (89 vs 50%) y no al tiempo de la misma. Sobre el 40% de pacientes en ambas cohortes presentaron síntomas de cefalea y/o déficits neurológico además de crisis y la media de edad de ambos fue de 45 años. (Jakola AS, Myrmel KS, Kloster R, et al. Comparison of a strategy favoring early surgical resection vs a strategy favoring watchful waiting in low-grade gliomas. JAMA 2012; 308:1881.).
Hasta que se hagan más estudios, se sugiere la resección mejor que la observación en pacientes con síntomas y pequeños tumores que no produzcan efecto masa. Sin embargo una observación cuidadosa podría ser una alternativa en estos pacientes con resección quirúrgica si hay evidencia de crecimiento o transformación a alto grado o crisis intratables o deterioro neurológico progresivo.
3) Grado de resección:
En un estudio de Smith y cols, se usó la RM para ver el volúmen pre y postoperatorio en 216 pacientes con gliomas de bajo grado hemisféricos operados en un único hospital. El volúmen se usó para ver el grado de resección y se correlacionó con los resultados al alta. El análisis multivariante encontró que la resección completa inicial fue el factor más importante de supervivencia, mientras que el bajo volumen preoperatorio se correlacionó con un aumento de supervivencia libre de progresión.
(Smith JS, Chang EF, Lamborn KR, et al. Role of extent of resection in the long-term outcome of low-grade hemispheric gliomas. J Clin Oncol 2008; 26:1338.)
RT adyuvante:
Es ampliamente usada para tratar la enfermedad residual tras la cirugía en pacientes con astrocitomas difusos. Los avances tanto en la radiología (RM, secuencia Flair), como en la oncoRT (radiación en un solo punto) han mejorado significativamente la planificación de la radioterapia.
Las controversias en el uso de radioterapia vienen tanto de la dosis como del momento de iniciar la irradiación.
- 1) Tiempo de irradiación: un estudio de la organización europea de la investigación y el tto del cáncer (aleatorizó 311 pacientes a recibir RT postqx o no, tras biopsia o resección parcial) demostró que la RT inmediatamente postoperatoria disminuye el tiempo libre de enfermedad, pero no afecta a la supervivencia total. La ausencia de beneficios en la supervivencia, indica que la RT ralentiza la progresión a alto grado, pero no la evita. Esto podría justificar el retraso en dar la RT hasta que haya progresión para así evitar la toxicidad de la misma. Tb observaron un mejor control de las crisis. Se utilizan los factores pronósticos para ver quien se puede beneficiar de la irradiación temprana: pacientes con rápida progresión, histología de astrocitoma puro, persistencia de enfermedad/síntomas, recurrencia, progresión, edad >40 años, tamaño del tumor >6cm, tumor que cruce la línea media, alto índice proliferativo.
2) Dosis de RT: la mayoría de los oncólogos, están de acuerdo en dar entre 45-60Gy
QT adyuvante:
Muchos estudios han investigado el tto postquirúrgico de gliomas de bajo grado de nuevo diagnóstico con QT usando PCV (procarbazina, lomustina y vincristina) o Temozolamida. Estos estudios están en fase II, resultados preliminares sugieren que la Temozolamida está asociada a una mejor calidad de vida, un mejor control de crisis y mayor sv libre de enfermedad. Un estudio limitado de 16 pacientes con oligodendroglioma, los datos sugieren un mejor control del tumor con el uso de PVC.
Temozolamida: los mejores respondedores son paciente con oligodendrogliomas y oligoastrocitomas. La deleción 1p/19q en heterozigosis está asociada significativamente a alta tasa de respuesta tb.
Recidivas:
La mayoría recidivarán, hay que distinguir recurrencia de radionecrosis que a veces puede ser difícil y puede ser necesaria una biopsia. Además la recurrencia puede ser como bajo grado o como transformación a alto grado.
Algunas consideraciones según el tipo de tumor:
Xantoastrocitoma pleomorfo: máxima resección segura. RT solo en caso de grado III (hay controversias), no QT. Sv general 5 años: 80%, 10 años: 71%. Mejores predictores de resultados son el grado de resección, el índice mitótico y la aparición de necrosis.
Astrocitoma pilocítico: supervicencia a los 10 años: 94%. Suficiente con la excisión del nódulo, el quiste no es neoplásico. No hay que radiarles debido a la alta supervivencia, son más los efectos secundarios de la radiación. Indicada la reintervención si recidiva. En recurrencias irresecables está indicada la RT
Gliomas de tronco: El tratamiento es habitualmente no quirúrgico. Cirugía solo indicada
1. Tumores con crecimiento dorsal hacia 4 ventrículo o ángulo pontocerebeloso
2. Shunts en hidrocefalia
Tratamiento habitual es la radioterapia
Oligodendrogliomas: cirugía. Siempre QT con PCV, tb estudiada la temozolamida para los anaplásicos. RT si transformación anaplásica.
DNT: cirugía. Excepcional que recidiven.
Gangliogliomas y gangliocitomas: cirugía. Si recidiva o agresividad: RT
Conclusiones:
– Tras resección subtotal en tumores > 4cm, astrocitomas, enfermedad residual >1cm: indicada la RT.
– Si se opta por la observación y seguimiento: cirugía si hay evidencia de crecimiento, transformación a alto grado, crisis intratables o deterioro neurológico progresivo.
– La RT inmediatamente postoperatoria disminuye el tiempo libre de enfermedad, pero no afecta a la supervivencia total
– QT: indicada en transformación a alto grado

Hola. Soy Yanela, cubana. Cuando tenía 12 años me diagnosticaron un Xantoastrocitoma pleomorfo grado 3 de 2.50cm. La conducta tomada fue recepción completa del tumor y luego quimioterapia. Estuve en tto QT dos años, con un anticuerpo monoclonal llamado Nimotuzumab q fue ensayado en mi país en esa etapa y tuve la oportunidad de ser d los niños a los q utilizaron en estas pruebas. Mi tto fue satisfactorio gracias a ese maravilloso colectivos de especialistas y al poder de Dios pude seguir mi vida normal. A día d hoy casi 13 años después puedo ser de las supervivientes de… Leer más »
Gracias Yanela por compartir tu experiencia
Un saludo
Hola tengo una hija de 4 años ase un mes se llevo al doctor debido a síntomas de bomito por una hidrocefalias que se lo estaba causando ,los resultados arrojaron que tiene un tumor cerebral un glioma de bajo grado 1 no operable desde su diagnóstico asta la fecha de que el oncólogo programe un tratamiento irían 36 días me gustaría saber sus opinión del caso gracias
Hola Buenas Noches mi Nombre es Deysi Altahona Guerra, soy Venezolana y hace nueve años fui operada de un ganglioma tipo I; mi post tratamiento pues se me fue indicado primeramente anti convulsivos y luego se me practico una RM y habia mejorado mucho y pues mi medico me indico solo oxigeneantes cerebral. Hace tres años en base a mi chequeo anual, me vio otro medico( no el que me opero ) y pues me indico que tenia que ser nuevamente operada, motivado a que segun desde en mi post tratamiento tenia que recibir radioterapia y quimioterapia y puedo decir… Leer más »
Hola…me extirparon por completo un glioma de bajo grado …estoy libre de el …pero igual me recomiendan rayos y quimio en pastillas para prevencion … por suerte estoy bien … por mi edad y proticolo tengo que hacer ese tratamiento
Buenas tardes, mi nombre es Carolina. Mi hijo de 6 años ha sido diagnosticado con un tumor cerebral, glioma tectal de bajo grado, en mayo del 2021. Desde entonces le han hecho resonancias cada 3 meses. Ha comenzado sesiones de quimioterapia con vinplastina en mayo de este año 2022, porque ha crecido un poco y tiene una apariencia brillante el tumor. Deseo saber si en este caso seria viable la radiocirugia y la protonterapia , que riesgos hay, y que beneficios. Por el lugar donde esta el tumor, (tronco del cerebro) dicen los medico no pueden operar ni biopsiar. Quiero… Leer más »
Hola pregunto recibiste contestación a tu pregunta tengo mi hija con el mismo diagnóstico desde ya te agradecería si me contestas
Hola qué tratamiento tuvieron que hacerle?
Hola, mi nombre es Rocio, sufro de epilepsia desde los 16 años y ya me realizaron tres resonancias magnéticas y esta es la conclusión de la última:
Hallazgos compatibles con malformación del desarrollo cortical en amígdala, giro parahipocampal y cabeza del hipocampo derecho. Considerar glioma de bajo grado con diagnóstico referencial.
¿Alguien me podría ayudar a que se refiere?, ya que no tengo una respuesta fija con referente a mi caso.
Hola Dra. Soy de Mexico tengo 47 años convulsione y me diagnosticaron un oligoneoroglioma parietal derecho tomaron una biopsia y lo que se alcanzó a extraer que no fue todo y es un grado 2 me dice mi neurólogo que no se puede realizar radio solamente en el tumor por riesgo a que haya algunos otros creciendo por ahí y necesito quimioterapia pero cual será la mejor?
Buenos días. Me llamo Donny Gutiérrez, tengo 39 años, soy de Guatemala, soy médico. Me diagnosticaron un glioma, supuestamente de bajo grado, pues no me pudieron extraer biopsia, ni realizar cirugía. Hace 15 días concluí la radioterapia más temozolomida. La esperanza de vida que he encontrado para mi caso es de UN día, no veo más allá de un día, ahora trato de vivir cada uno al 100% y parecerá raro para quienes no me entiendan, pero este cáncer fue y sigue siendo una bendición. Me siento más cerca de Nuestro Señor y los dones y frutos del Espíritu Santo… Leer más »
Tengo un hijo de 11 meses de edad con glioma astrocitoma grado 2 en el bulbo raquideo los doctores ya ñe quitaron ñas quimioterapia porque no tiene resultado me podrían ayudar que debemos hacer mi hijo esta con traquea y gastroesofágico porque no deglute y esta con respirador artificial
Hola a todos,mi nombre es Carlos Dumas tengo 39 años soy Nicaragüense,fui operado hace un año de un tumor en la parte tempo parietal derecho, mi reacción fue subtotal, el diagnóstico de patología arrojó un astrocitoma difuso grado 2 recibí 54 Grey’s de radioterapia en Guatemala con acelerador lineal de intensidad modulada con temozolamida co adyuvante,y después recibí 5 ciclos más de temozolamida, en mi último estudio de resonancia magnética con espectroscopía, me salen tres lesiones,con captación de contraste en anillo, y el pico de colina elevado,el neurocirujano que me operó,me dice que no es recurrencia, ni recidiva,sino el mismo… Leer más »