SÍNDROME DE COMPRESIÓN MEDULAR. TUMORES VÉRTEBRO-MEDULARES
Tema VIII: Temario de Neurocirugía 2020 para alumnos de Facultad de Medicina de la UAM: 2020
Facultad de Medicina de la Universidad Autónoma de Madrid.
Directores:
PARTE I.- RECUERDO NEUROFISIOLÓGICO
1.1.- INTRODUCCCIÓN
En esta lección realizaremos un breve repaso de los datos anatómicos y clínicos vértebro-medulares más esenciales, que nos permitan un fácil entendimiento de la patología quirúrgica de la médula espinal.
A continuación se expondrá el síndrome de compresión medular clásico, para finalmente hacer un recorrido de la patología que más frecuentemente llega a afectar la médula espinal y cuya alternativa terapéutica más razonable es la quirúrgica.
1.2.- RECUERDO ANATÓMICO
1.2.1.- MEDULA
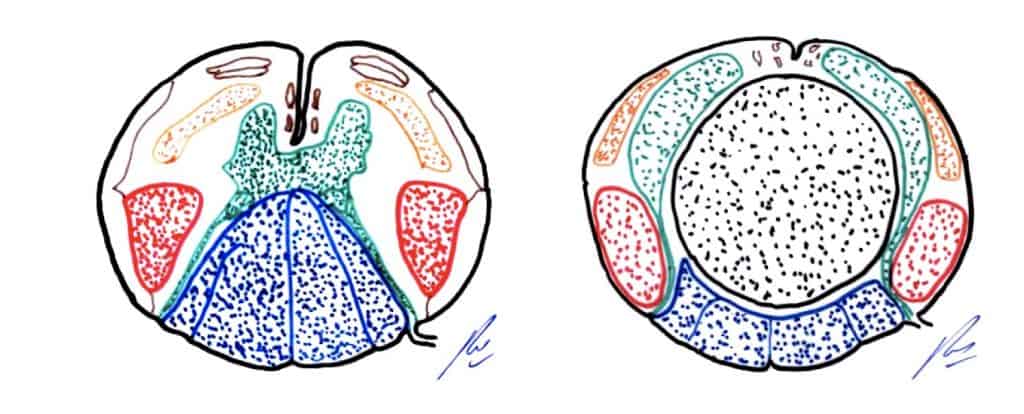
Desde el punto de vista clínico es esencial conocer al menos tres vías que recorren la médula, aparte de la disposición de la sustancia gris en astas anteriores motoras y posteriores sensitivas.
A. – La primera vía es el haz espino-talámico (lateral y anterior), que se sitúa en la parte anterior del cordón lateral. Esta vía se va constituyendo por prolongaciones provenientes de las neuronas del asta posterior del lado contrario, que cruzan la sustancia gris pasando por la zona periependimaria. La incorporación a esta vía de los axones se hace casi a la misma altura (1-3 metámeras) de la neurona origen. Es, por tanto, una vía cruzada a medida que se va formando. Lleva la sensibilidad táctil protopática, dolor y temperatura.
Pensemos en la disposición de los axones en esta vía. Vayamos viendo la médula de abajo hacia arriba, a medida que se van incorporando axones. Los que ya estaban en el haz espino-talámico van siendo rechazados hacia fuera por los nuevos que van entrando en el haz. De forma que la disposición en «capas» concéntricas en este haz, según ascendemos en la médula, sitúa las fibras de la zona inferior del cuerpo más exteriores que las fibras de la zona más superior que se están incorporando.
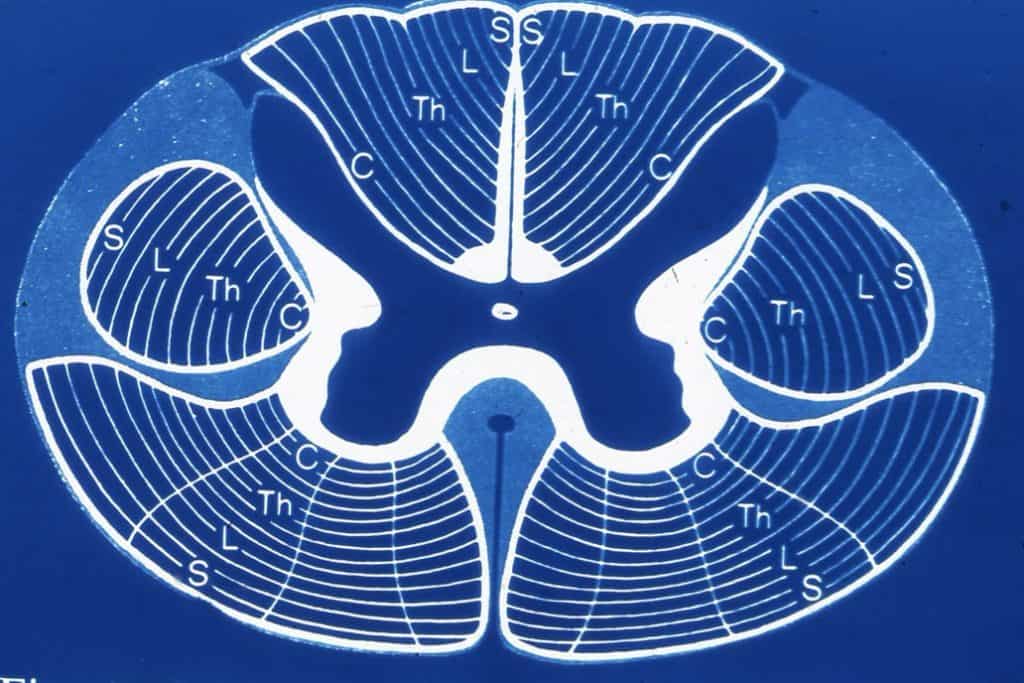
B. Haz piramidal cruzado, situado en la parte posterior del cordón lateral. Está constituido por las prolongaciones de las neuronas motoras piramidales corticales contralaterales. Es una vía no cruzada a lo largo de toda la médula, aunque se ha cruzado ya a nivel de la decusación de las pirámides en el bulbo.
Al descender a lo largo de la médula, las prolongaciones que antes abandonan la vía son las correspondientes a la parte más interna, ya que tienen que ir hacia el interior de la médula hacia las astas anteriores. De forma que, al final, la disposición de las fibras dentro del haz piramidal es similar al haz espino-talámico: las fibras más internas se corresponden con las zonas superiores del cuerpo y las fibras más externas, con las zonas más inferiores.
C. Cordones posteriores, formados por los haces de Goll y Burdach, que llevan la sensibilidad táctil epicrítica y la sensibilidad propioceptiva. A estos haces se van incorporando axones de las neuronas del ganglio raquídeo y asta posterior del mismo lado y ascienden sin cruzarse a lo largo de toda la médula. Se cruzarán posteriormente a nivel del tronco cerebral tras hacer conexión en los núcleos de Goll y Burdach, para llevar la información a las neuronas corticales contralaterales.
La disposición de las fibras dentro del haz es similar a las anteriores vías: la zona inferior del cuerpo va quedando más externa a medida que se incorporan fibras de zonas superiores, que quedan más internas con respecto al centro de la médula.
Esto tiene dos implicaciones clínicas importantes:
A.- Si seccionamos o comprimimos una de las mitades de la médula (hemisección medular) vamos a tener:
– Afectación de fuerza en las extremidades ipsilaterales por debajo de la lesión (síndrome piramidal, con paresia espástica, exaltación de reflejos osteotendinosos, desaparición de reflejos cutáneos y aparición del signo de Babinski).
– Alteración de la sensibilidad contralateral, por debajo de la lesión, sobre todo al calor y temperatura.
– Alteración de la sensibilidad epicrítica y profunda en el mismo lado de la lesión.
Esta disociación entre la afectación de fuerza en un lado del cuerpo y afectación de la sensibilidad en el otro diferencia las lesiones medulares de las cerebrales, donde la afectación de sensibilidad y fuerza ocurre en el mismo lado.
B.- Debido a la somatotopía que hemos visto en las grandes vías, si la lesión compresiva va afectando a la médula desde fuera (extramedular), se van a observar alteraciones progresivas de las vías referidas (fuerza y sensibilidad) que van a iniciarse en las partes más inferiores del cuerpo (extremidades inferiores) y va a ir ascendiendo hasta llegar al lugar de la compresión.
Por el contrario, si la lesión compresiva es intramedular se va a afectar primero la parte interna de las vías. Es decir, la clínica de paresia e hipoestesia va descendiendo desde el nivel de la lesión hacia extremidades inferiores.
1.2.2.- RAICES MEDULARES
Es importante recordar que en cualquier raíz o nervio van a coexistir tres tipos fundamentales de conducción: dolorosa, sensitiva y motora. Las fibras del dolor apenas tienen mielina, mientras que las fibras motoras son las que tienen una mayor capa protectora mielínica, estando las fibras sensitivas en una situación intermedia. Esto tiene importancia desde el punto de vista clínico, ya que una compresión mecánica progresiva va a manifestarse en un primer estadio por dolor, a continuación por hipoestesia-anestesia y finalmente por pérdida de fuerza.
1.3.- RECUERDO CLÍNICO
Otro paso importante en cuanto a nuestra capacidad de diagnosticar correctamente una lesión medular, es contar con conocimientos clínicos que nos permitan saber el nivel o altura a que se encuentra le lesión medular.
Para esto podemos contar con varios signos clínicos que se corresponden con determinadas metámeras que, de arriba abajo, son:
A.- Dermatomas:
– Hipoestesia en 1-2 dedos de la mano: C6-C7
– Hipoestesia en 4-5 dedos de la mano: C7-C8
– Hombro: C4
– Región umbilical: D10
– Hipoestesia en 1-2 dedos del pie: L5
– Hipoestesia en 4-5 dedos del pie: S1
B. – Reflejos osteotendinosos:
– Bicipital: C5-C6
– Tricipital: C7-C8
– Rotuliano : L3-L4
– Aquíleo: S1
C. – Reflejos cutáneos:
– Cutáneo abdominal superior: D6-D9
– Cutáneo-abdominal medio: D9-D11
– Cutáneo-abdominal inferior: D11-L1
– Cremastérico: L1-L2
D. – Reflejo plantar:
– En extensión: Babinski (afectación piramidal).
PARTE II.- SÍNDROME DE COMPRESIÓN MEDULAR
2.1.- CONCEPTO
Oppenheim en 1923 distingue tres estadios en el proceso de compresión medular:
1º. – Compresión precoz, con dolor radicular
2º. – Compresión acentuada con síndrome de Brown-Séquard
3º.- Compresión completa con lesión transversa medular. Scheid en 1963 divide esta última fase en:
– Síndrome transverso incompleto
– Síndrome transverso completo
El resultado final conduce a la misma situación que la sección medular, que veremos en el tema de los traumatismos raquimedulares. Pero la diferencia entre los síndromes de compresión y sección medular estriba en que el primero es de instauración lenta o crónica y el segundo es de instauración rápida o aguda.
2.2.- FISIOPATOLOGÍA
Cualquier lesión ocupante de espacio, que se desarrolle en el área del canal espinal, puede afectar a la médula. Para esto influyen una serie de condicionantes:
A.- Origen de la lesión: médula, raíces, meninges, vasos, hueso.
B.- Carácter de la lesión: tumoral (benigna o maligna), infecciosa, vascular…
C.- Capacidad de adaptación del conjunto raquimedular. En este sentido, desde el punto de vista mecánico, la médula tiene poca capacidad de adaptación ante una lesión ocupante de espacio. Pero es llamativo la compensación de la naturaleza, en el sentido de que, si la compresión es lentamente progresiva, hay una adaptación del hueso, que deja espacio a la lesión, con agrandamiento de agujeros de conjunción u oquedades o improntas en el cuerpo vertebral.
D.- Afectación vascular, que puede complicar la evolución al sobreañadirse un proceso isquémico. Esto es especialmente relevante en los casos de infecciones e infiltraciones malignas de los plexos venosos epidurales, que pueden acelerar el cuadro clínico de déficit neurológico.
2.3.- CLINICA
2.3.1.- Estadio I.- Fase radicular
Existe una fase inicial de irritación de las vías sensitivas medulares (raquídeas o intramedulares), muy focal, que se manifiesta por:
Dolor.- Tiene una gran importancia diagnóstica y va a ser de tipo radicular o por afectación del haz espinotalámico.
Hipoestesia.- Al mismo nivel del dolor.
Atrofia-Fasciculaciones.- Raro de ver, por ser muy limitada la afectación de la segunda neurona.
Lesiones óseas.- Podemos apreciar en las Rx convencionales: Aumento del canal vertebral, del agujero de conjunción, erosión de cuerpos vertebrales… También es posible apreciar signos indirectos de correcciones de curvaturas fisiológicas por contractura muscular antiálgica.
Este estadio es muy importante tenerlo en cuenta por dos circunstancias:
1. – Es el inicio del cuadro de compresión medular. Un diagnóstico precoz lleva a un tratamiento adecuado en el tiempo, con menores riesgos quirúrgicos y mucho mejor pronóstico.
2. – Todos los síntomas y signos detectan el nivel en el que se ha iniciado la lesión. Son localizadores de la altura a la que se está afectando la médula. Nos dirige, por tanto, a la zona a explorar con las pruebas diagnósticas a realizar.
2.3.2.- Estadio II.- Síndrome transverso incompleto y reversible
La lesión medular se inicia y avanza por efectos de la compresión y de los cambios circulatorios.
Sus características van a ser similares al síndrome de hemisección medular de Brown-Séquard (aunque con un desarrollo lentamente progresivo y no tan recortado). Como hemos referido anteriormente, la clínica va a consistir fundamentalmente en:
– Afectación de fuerza en las extremidades ipsilaterales por debajo de la lesión (síndrome piramidal, con paresia espástica, exaltación de reflejos osteotendinosos, desaparición de reflejos cutáneos y aparición del signo de Babinski).
– Alteración de la sensibilidad contralateral, por debajo de la lesión, sobre todo al calor y temperatura.
– Alteración de la sensibilidad epicrítica y profunda en el mismo lado de la lesión.
En esta fase ya se debe realizar el diagnóstico de localización de la lesión. Hay que tener en cuenta que, desde el punto de vista clínico, el nivel lo va a marcar los síntomas y signos de la fase radicular, que permanecen en este estadio.
Si no se realiza el diagnóstico y tratamiento en esta fase, el paciente continuará el curso fatal hacia la lesión medular irreversible. En esto influyen varias causas: indiferencia del paciente, poca capacidad médica para darse cuenta de la grave situación o rápida evolución del proceso clínico.
2.3.3- Estadio III.- Interrupción irreversible de la conducción a nivel medular o cola de caballo
Las formas pueden ser:
– Incompleta.- Igual que el estadio II, pero más estable e irreversible
– Completa.- Como la sección medular
La clínica, en resumen, consiste en:
o Anestesia por debajo de la lesión
o Parálisis espástica (médula) o flácida (cola de caballo), por debajo de la lesión
o Afectación de esfínteres. Por lo general, retención urinaria y estreñimiento.
o Alteraciones tróficas.
2.4.- DIAGNOSTICO
En el proceso diagnóstico tenemos que tener en cuenta que debemos conseguir los siguientes objetivos:
A. – Localizar el nivel
Depende de la estabilidad de los síntomas y es crucial detectarlo precozmente. Para esto hay que tener en cuenta dos hechos:
– Como ya hemos repetido varias veces, el estadio radicular lo marca. Incluso aunque estemos en la fase II, hay que rehacer en la historia clínica la correcta secuencia de los síntomas: Dónde se inició el dolor.
– La progresión de los síntomas va a ser:
– Desde el nivel de compresión hacia abajo, si la lesión es intramedular.
– Desde las extremidades inferiores hacia el nivel de compresión, si la lesión es extramedular (lo más frecuente).
B. – Topografía de la lesión
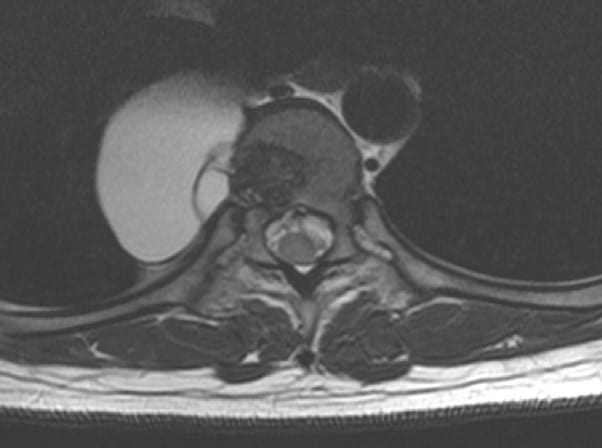
Clásicamente las lesiones compresivas medulares se dividen en tres tipos:
A.- Extradural
B.- Intradural extramedular
C.- Intradural intramedular
Además es importante detectar si la lesión comprime a la médula en su zona dorsal, ventral, lateral o llega a rodearla por completo (como un servilletero).
C. – Evolución del cuadro clínico
En esto hay que tener en cuenta:
– La velocidad de progresión de los síntomas (horas, días o meses)
– La edad y condiciones generales del paciente, que hagan predecir una más rápida o lenta evolución.
Dependiendo de este punto, el manejo diagnóstico y terapéutico va a tener que realizarse de forma urgente o se podrá diferir en el tiempo.
2.4.1.- Medios diagnósticos
Hoy día contamos con:
A. – Radiografía de columna:
Útil sobre todo para ver la afectación o destrucción ósea
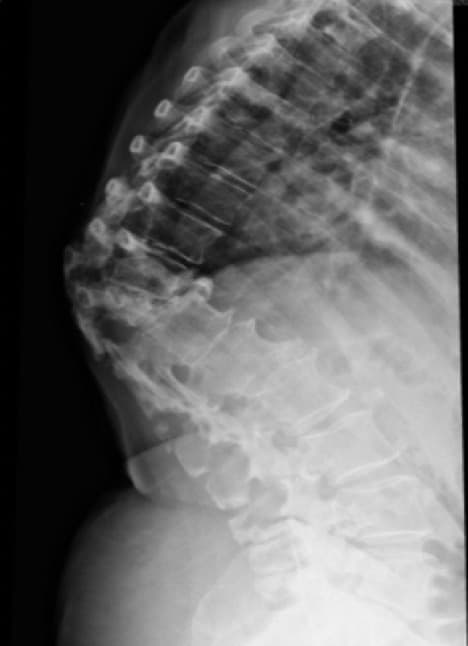
B. – TAC de columna:
Mejor visualización de la estructura ósea y si existen alteraciones a varios niveles
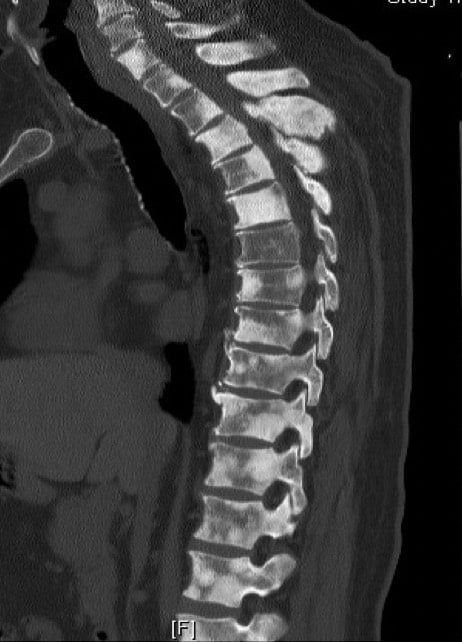
C. – RM de raquis
Es la prueba de elección al permitir ver la médula, su contenido y la estructura osea
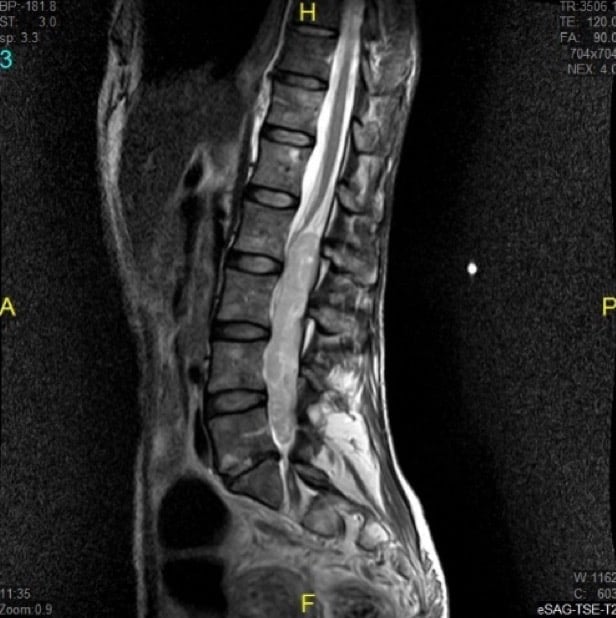
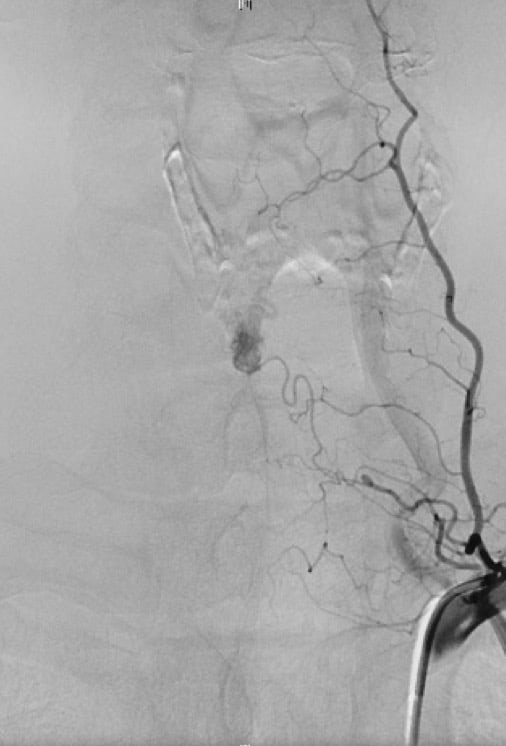
D. – Arteriografía medular
Útil en sospecha de patología vascular
E.- EMG
F. – Potenciales evocados somatosensoriales y motores
G. – En casos excepcionales, puede ser útil:
– Punción lumbar y estudio del LCR
– Estudio gammagráfico óseo
2.4.2.- Manejo diagnóstico
En la práctica diaria los esenciales son las Rx y la RM. En caso de no tener esta última, es útil el TAC. No nos cansaremos de repetir que en esta patología es el clínico el que guía la exploración radiológica. Por lo que, si se equivoca de nivel, el estudio va a ser negativo y retrasar el tratamiento.
No es la primera vez que un enfermo acude al médico, por ejemplo, por trastornos en la marcha o debilidad en extremidades inferiores, se le pide Rx e incluso RM lumbar y, por no hacer una historia clínica adecuada, no se detecta hasta más tarde que la lesión está en región cervical (donde el paciente presenta dolor local irradiado a uno de los hombros).
PARTE III.- ETIOLOGÍA DEL SÍNDROME DE COMPRESIÓN MEDULAR
Existen diversos tipos de lesiones compresivas medulares. Su clasificación y descripción de las características clínicas más sobresalientes, se hacen a continuación.
3.1.- LESIONES EXPANSIVAS INTRAMEDULARES
3.1.1.- Tumores primarios intramedulares: Constituyen el 15% de los tumores raquimedulares:
3.1.1.1. – Ependimoma
Los ependimomas derivan del epitelio ependimario. Se distinguen cuatro grados según su agresividad histológica: papilar, celular, epitelial y mixta. Aparecen entre la segunda y sexta década de la vida, con ligero predominio en varones y dan lugar a masas intramedulares bien delimitadas que se extienden a lo largo de varios cuerpos vertebrales (3-5). Una tercera parte de estos tumores se encuentran en el filum terminale, adquiriendo carácter extramedular.
Dan lugar a un cuadro clínico prolongado, al menos durante uno o dos años y excepcionalmente aparecen de forma aguda al originar hemorragias subaracnoideas junto a ciatalgias.
La clínica consiste en dolor a nivel del tumor (por afectación del haz espinotalámico), continuo, lancinante en ocasiones, que se exacerba por la noche e incluso despierta al paciente. Posteriormente van apareciendo síntomas motores de progresión descendente.
En la exploración nos podemos encontrar con un cuadro muy similar a la siringomielia.
En las Rx se puede apreciar un aumento del diámetro del canal espinal.
En la RM es fácil el diagnóstico de lesión intramedular, aunque en ocasiones es difícil de diferenciar de un astrocitoma.
El tratamiento es quirúrgico y en muchas ocasiones hay un plano de clivaje que permite su resección completa respetando la función medular. Es esencial el control neurofisiológico intraoperatorio.
La radioterapia puede completar el tratamiento, sobre todo en casos de ependimoma de cola de caballo, en que es prácticamente imposible la extirpación completa.
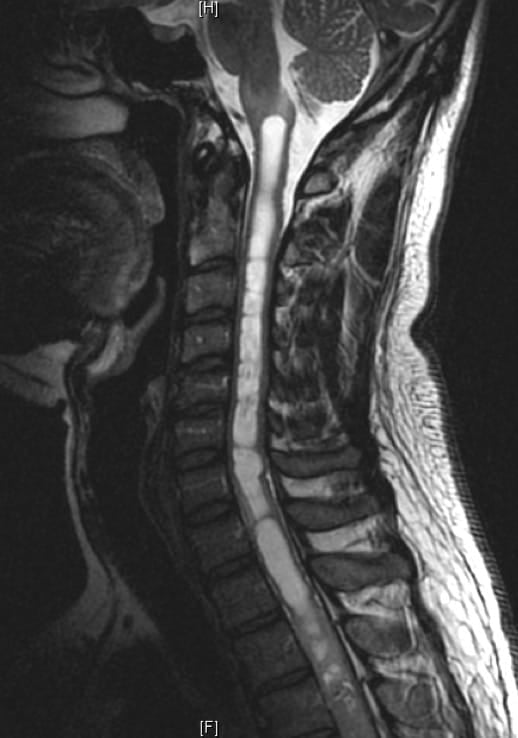

3.1.1.2. – Astrocitoma
Los astrocitomas son los tumores intramedulares que siguen en frecuencia. Suelen ser de bajo grado de malignidad y generalmente de tipo pilocitico. Predominan en la tercera década de la vida, más frecuentes en varones.
La localización preferente es a nivel torácico, aunque no es raro encontrar astrocitomas muy extendidos que abarcan prácticamente toda la médula. Es común encontrar quistes intratumorales y cavidades intramedulares asociadas.
La clínica y evolución son similares al ependimoma y muy lentamente progresiva.
El proceso diagnóstico es similar. Dado que la extirpación es imposible, hoy día se están haciendo esfuerzos diagnósticos con la RM para diferenciarlos del ependimoma, con el fin de evitar una intervención que sólo nos va a permitir un diagnóstico de certeza, pero no su extirpación.
La radioterapia es el único tratamiento a nuestro alcance en el momento actual.
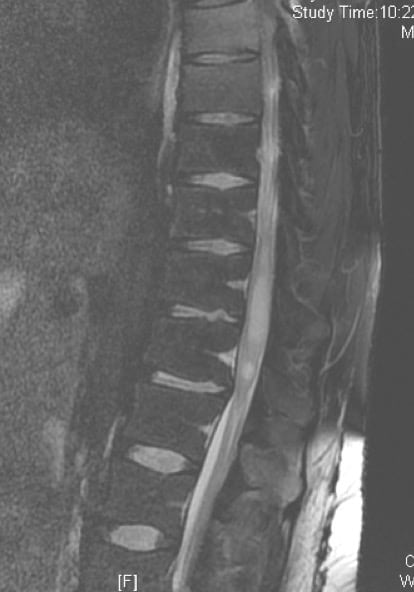
3.1.1.3. – Otros
Dentro de estos tumores intramedulares se incluyen otras neoplasias, unas malignas como los glioblastomas y otras benignas como los hemangioblastomas.
Los lipomas, dermoides, epidermoides y teratomas son raras neoplasias de carácter congénito, pudiendo encontrarse como intramedulares o intradurales-extramedulares. Todos estos se localizan con preferencia a nivel lumbosacro y aparecen en la infancia o en personas jóvenes, también asociados a alteraciones congénitas (disrafismo espinal), de las que hablamos en el Tema de Malformaciones.
3.1.2.- Tumores secundarios intramedulares. Son excepcionales, por metástasis, infiltrados leucémicos, etc.
3.1.3.- Malformaciones vasculares
Son también infrecuentes. Hay que distinguir 2 tipos:
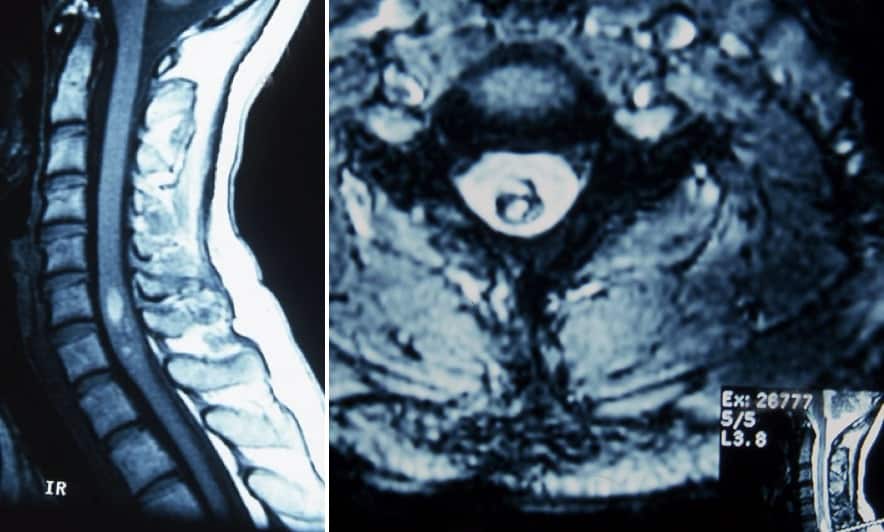
3.1.3.1. – Angioma Cavernoso
Se va a manifestar clínicamente mediante cuadros agudos o subagudos de pérdida de función medular, debido a hemorragias repetidas, que pueden llevar a lo largo de años a la lesión medular completa.
Suele presentarse en pacientes jóvenes.
El diagnóstico mediante RM es fácil, siendo la imagen similar a los cavernomas cerebrales con aspecto de una mora, con zona hipointensa circundante (antigua hemorragia) y zonas de hemorragia reciente..
El tratamiento es quirúrgico.
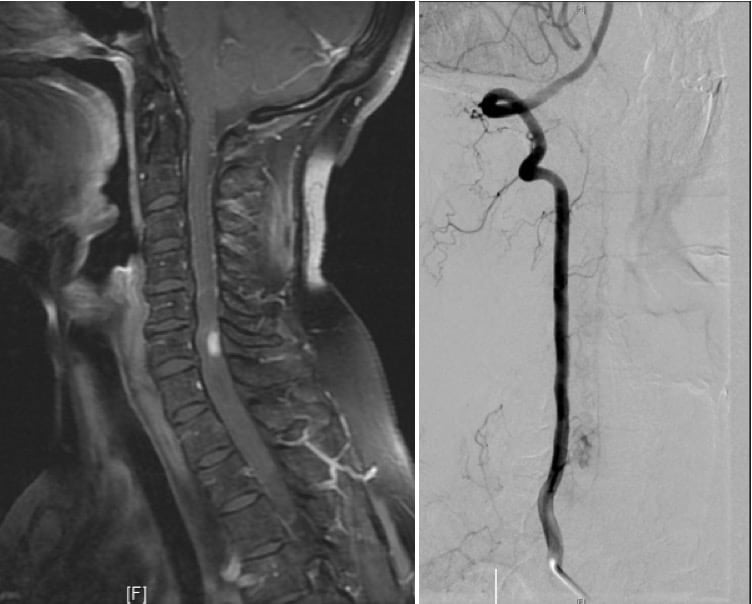
3.1.3.2. – Malformaciones arteriovenosas
Similares a las cerebrales y son raras, con predominio en varones, con edad entre los 20-60.
La clínica por la que se manifiestan es aguda, en casos de hemorragia (hemorragia subaracnoidea o intramedular [7-30%]), o crónica por déficit neurológico progresivo a causa de fenómenos isquémicos de robo.
El diagnóstico es mediante RM y angiografía medular.
El tratamiento es combinado, mediante técnicas endovasculares de embolización y quirúrgico.
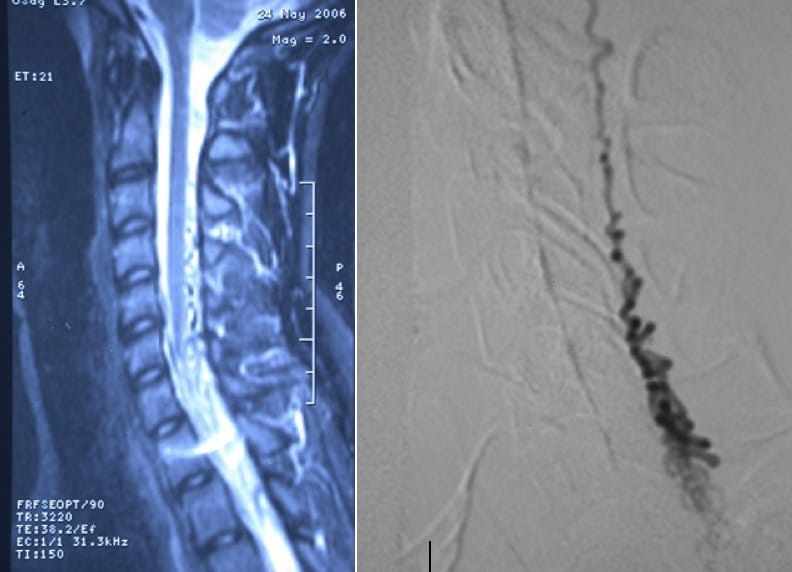
3.1.3.3.- Fístula dural
Entidad que se diagnostica cada vez más frecuentemente. Consiste en la unión de una arteria radicular con venas de drenaje medular.
La causa no es congénita, sino adquirida. En persoan por encima de los 60 años.
La clínica puede ser aguda o, más frecuentemente, insidiosa. Cursando con brotes de insuficiencia o isquemia medular progresiva.
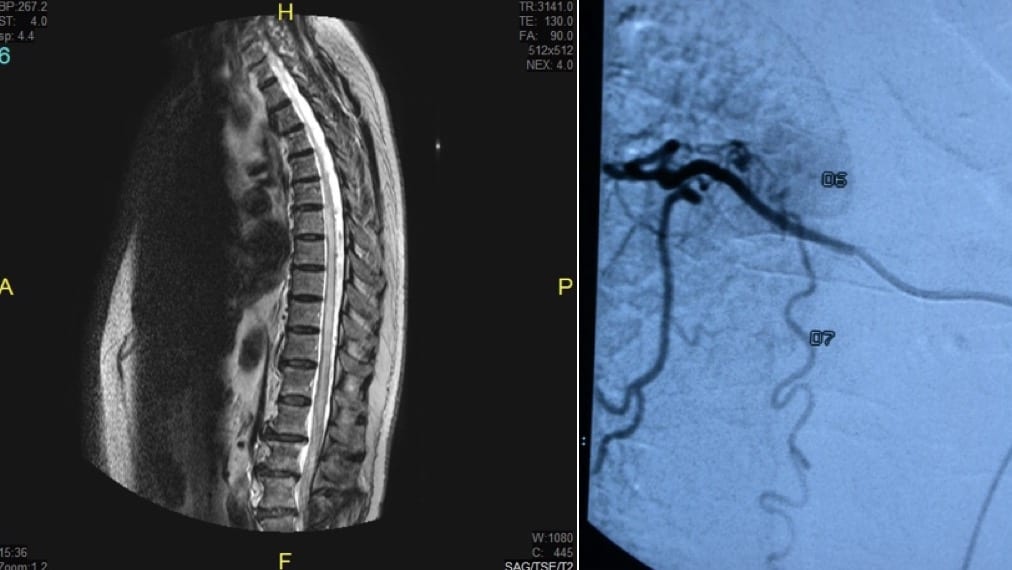
El diagnóstico se ha de hacer ante un cuadro como el descrito y se sospecha con RM. Se confima con estudio angiográfico medular.
El tratamiento se hace en conjunción con neurorradiología intervencionista. O bien se cierra con técnicas neurointervencionistas endovasxulares o bien con acceso directo quirúrgico a la fístula.
3.1.- LESIONES EXPANSIVAS INTRADURALES EXTRAMEDULARES
3.1.1.- Tumores benignos
Representan el 25 % de los tumores raquimedulares. Los más frecuentes son dos: meningiomas y neurinomas
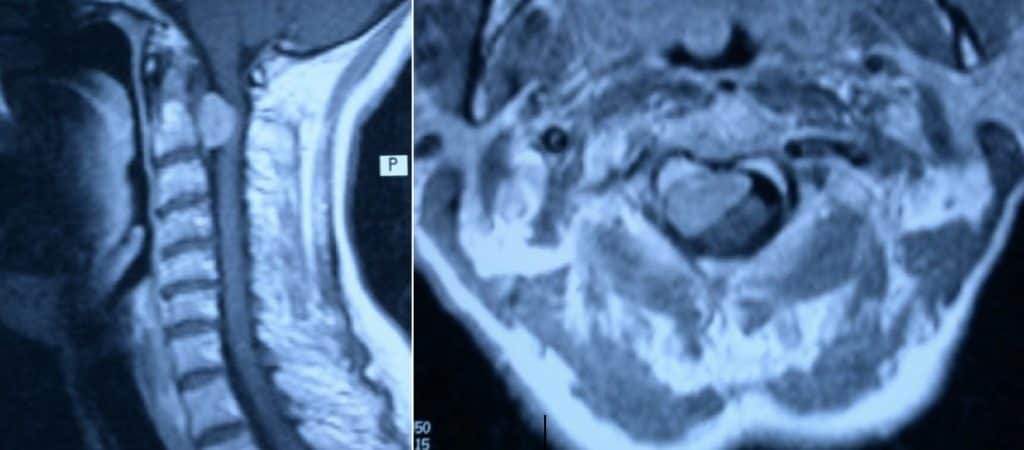
3.1.1.1. – Neurinoma
Son los más frecuentes. Se trata de neoplasias benignas que se desarrollan a partir de las vainas nerviosas.
Ocasionalmente progresan también hacia el espacio extrarraquídeo o través de los agujeros de conjunción tomando una forma denominada en reloj de arena (Figura 3). Pueden ser múltiples en los casos de neurofibromatosis o enfermedad de von Recklinghausen.
Aparecen entre la 3 y 6ª década de la vida, con discreto predominio por el sexo masculino.
La clínica es de inicio radicular y posterior compresión medular ascendente (iniciándose a distancia del dolor radicular, hasta que llega a este nivel). Son el arquetipo del síndrome de compresión extramedular.
Es característico encontrar aumento del agujero de conjunción de un lado, por lo que en toda exploración radiológica ha de realizarse proyecciones oblicuas que visualicen dicho agujeros de conjunción. El TAC y, sobre todo, la RM completarán el diagnóstico.
El tratamiento es quirúrgico, con extirpación completa de la lesión.
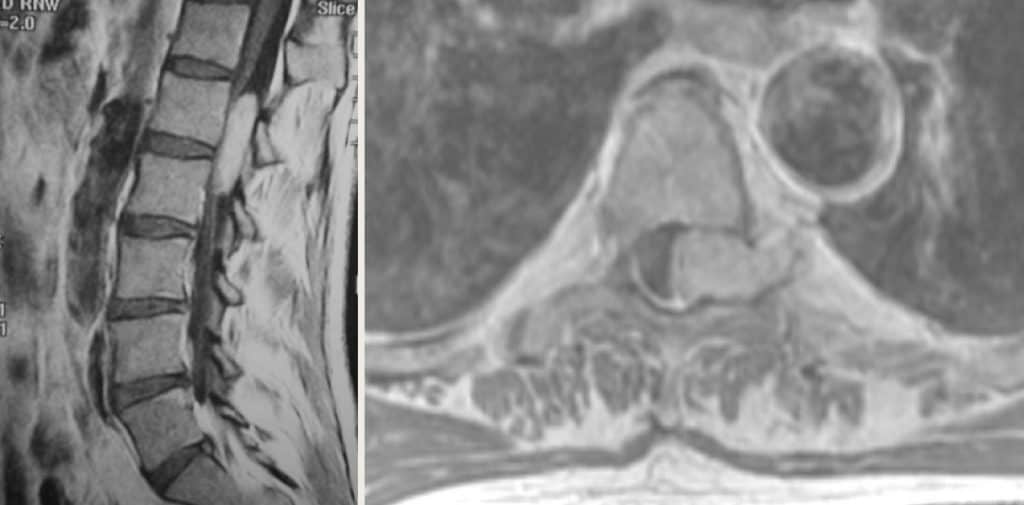
3.1.1.2. – Meningioma
El segundo tumor en frecuencia es el meningioma, que en su localización espinal representa la 1/4 parte del total de los meningiomas. Son benignos generalmente y sólo en raras ocasiones tienden a crecer fuera del canal raquídeo. El tipo histológico más frecuente en el meningotelial.
Existe un claro predominio femenino y la edad más frecuente es entre la 5ª y 7ª década. Las 3/4 partes se localizan en la columna torácica, con cuadro clínico crónico e insidioso de compresión medular. A veces sin dolor o éste es menos localizador (radicular) que el neurinoma.
El diagnóstico y tratamiento son similares al anterior.
3.1.2- Tumores malignos
Más raros, son otros tipos de lesiones tumorales. Hay que destacar las siembras ocasionadas por tumores intracraneales como el meduloblastoma, ependimoma, etc., o la carcinomatosis meníngea, ya vistos en las lecciones correspondientes.
3.2.- LESIONES EXPANSIVAS EXTRADURALES
Son las que ocasionan con mayor frecuencia el síndrome de compresión medular y, de hecho, suponen el 60 % del total de los tumores raquimedulares. Hay que clasificarlas, a su vez, en:
3.2.1.- Lesiones tumorales
Entre éstas, hay que destacar:
3.2.1.1. – Metástasis
Con diferencia, las metástasis óseas son las neoplasias más frecuentes de este grupo (70%). Predominan ligeramente en varones y la edad oscila entre 50 y 70 años.
Las vías de metastatización pueden ser hematógena o por contigüidad.
Su origen es muy variado, siendo los mas frecuentes pulmón, mama, próstata, mielomas y linfomas.
Suelen asentar en la región torácica y el cuadro de presentación puede ser agudo (por fractura espontánea asociada, por ejemplo), subagudo o crónico.
La clínica es la correspondiente a un síndrome de compresión medular por lesión extramedular. Suele haber dolor a la altura de la lesión.

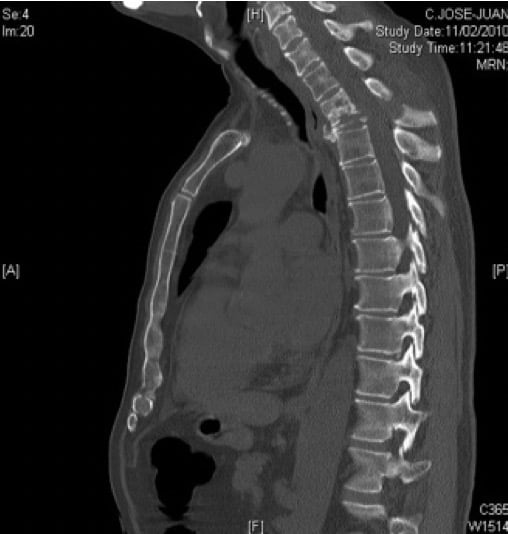
El diagnóstico de las lesiones tumorales es a veces muy fácil, solamente con la Rx de columna. Pero es clave, como ya hemos repetido varias veces, que se solicite el nivel adecuado de afectación posible medular.
Se pueden obtener signos de destrucciones óseas, aplastamientos vertebrales, zonas de condensación ósea, erosión de pedículos, dilataciones de los agujeros de conjunción. Todo este tipo de signos va a ser mucho más llamativo en las metástasis.
El TAC y RM completan el diagnóstico y la relación entre masa tumoral y médula. Una característica de diagnóstico diferencial frente a las espondilodiscities es que no se afectan los discos intervertebrales (Figura 16).
El tratamiento de las metástasis puede llegar a ser muy complejo. En primer lugar, es útil cuando se diagnostica un proceso compresivo medular la aplicación de corticoides antes y después de la intervención. También es muy útil la aplicación de técnicas de rehabilitación lo antes posible.
En segundo lugar, en el caso de metástasis única con signos de afectación medular incompleta, el tratamiento más adecuado es radioterapia. Se ha comprobado que el resultado a largo plazo es similar al tratamiento quirúrgico (laminectomía descompresiva) seguido de radioterapia. Por lo que la cirugía añade riesgos de complicaciones y no previene mejor de la aparición de una afectación medular completa irreversible.
A esto habría que exponer una excepción: cuando no se conoce el diagnóstico, por no localizar el tumor primitivo. Sólo en muy raras excepciones, en las que sea imposible la biopsia con aguja guiada por TAC, estaría indicada la cirugía, para descomprimir y tomar una biopsia.
En tercer lugar, si hay una situación de curso rápido de afectación medular, podría estar indicada la descompresión quirúrgica de urgencia..
Una cuarta situación es el caso de imágenes múltiples metastásicas, en la que la indicación quirúrgica es muy dudosa y suele ser más útil el tratamiento radioterápico.
Por último, en el momento actual se están dando dos circunstancias que están de nuevo cambiando algunas actitudes frente a las metástasis. Por un lado, se están obteniendo supervivencias muy prolongadas en los procesos malignos. Por otro lado, la aparición de una metástasis ósea es con gran frecuencia causa de inestabilidad a este nivel con dolor y posibilidad de fractura patológica. Por lo que, en personas con buen estado general y buen pronóstico en cuanto a control de su enfermedad, se plantea la posibilidad de extirpación del cuerpo vertebral y sustitución-fijación con técnicas complejas de instrumentación vertebral, seguido todo ello por radioterapia local.
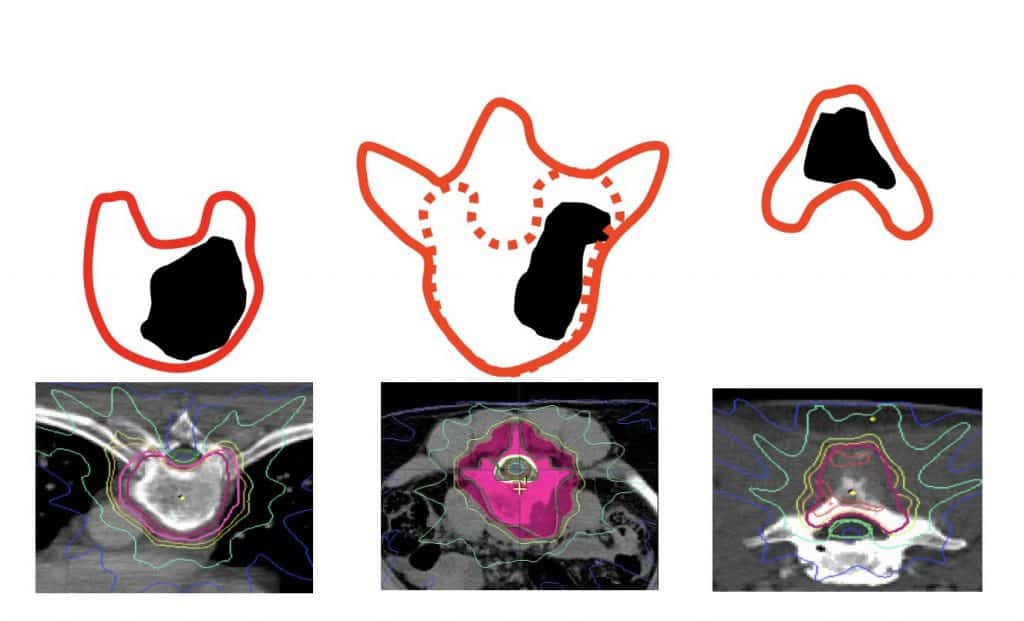
A medida que las técnicas de radioterapia están mejorando se pueden planificar tratamientos de radioterapia estereotáxica fraccionada, que incluyen toda la masa tumoral, respetando la médula. En este sentido, la cirugía ayuda de dos formas: a) Capacidad de biopsia y cimentación de la vértebra (Vertebroplastia-Cifoplastia). B) Fijación vertebral instrumentada con tornillos pediculares. En la misma intervención.
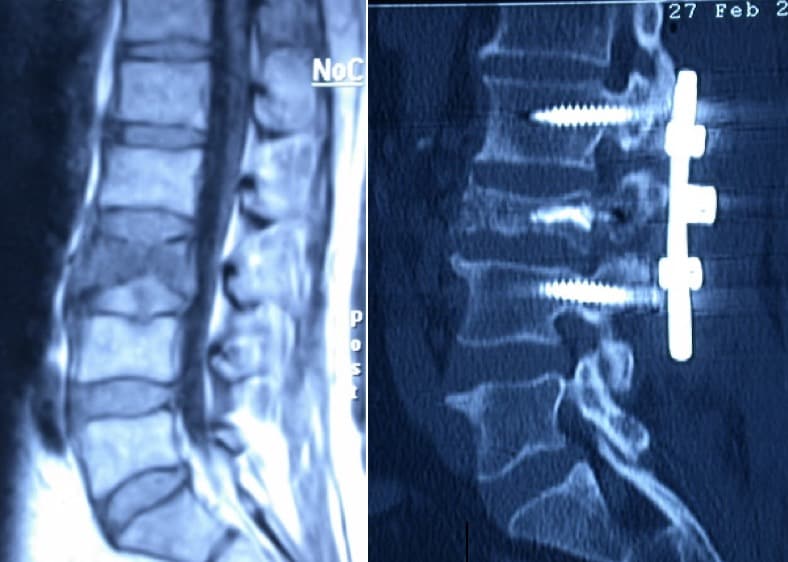
Por lo que, ante un paciente con posibles metástasis, la buena coordinación entre Oncología Médica, Oncología Radioterápica y Neurocirugía es la clave.
3.2.1.2. – Tumores óseos primitivos
Menos frecuentes son los tumores primitivos óseos, benignos como el osteoma osteoide, osteoblastoma, osteocondroma; o malignos como el condrosarcoma y osteosarcoma.
3.2.1.2.1.- Quiste óseo aneurismático
Tiene mayor incidencia en la segunda década de la vida. Es una lesión muy vascularizada en forma de panal de abeja con una capa cortical delgada que tiende a expandirse
El tratamiento es quirúrgico. Si no se reseca completamente tiene a reproducirse
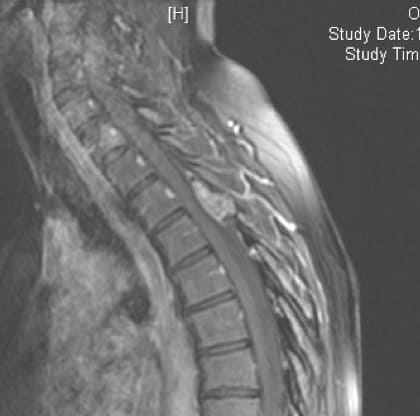
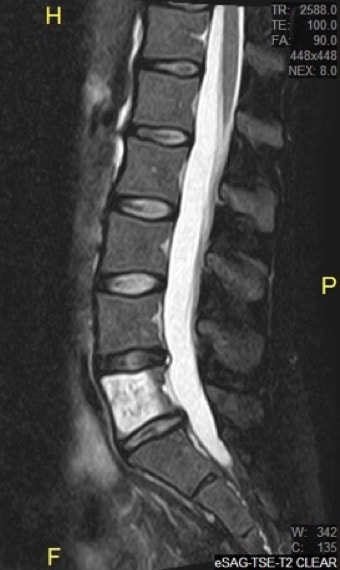
3.2.1.2.2.- Hemangioma vertebral
Incidencia del 9-12% de los tumores. Pueden ser múltiples. Las regiones más afectadas suelen ser a nivel torácico y lumbar. Afectan al arco posterior, cuerpo o a ambos. Se produce un reemplazo óseo por vasos con hipertrofia esclerótica del hueso con trabeculaciones orientadas en dirección rostral o caudal.
Con frecuencia son asintomáticos. Pueden producir dolor localizado. En algunos casos pueden provocar compresión medular si hay expansión del cuerpo vertebral
En radiografía tienen una imagen típica en panal de abeja. La RM descarta la compresión del canal y el TAC visualiza la extensión
Si son sintomáticos se pueden embolicar, cementar la vertebra o dar radioterapia
3.2.1.2.3.- Osteocondroma:
Tumor benignos mas frecuente en la infancia, se forma cartílago hialino maduro

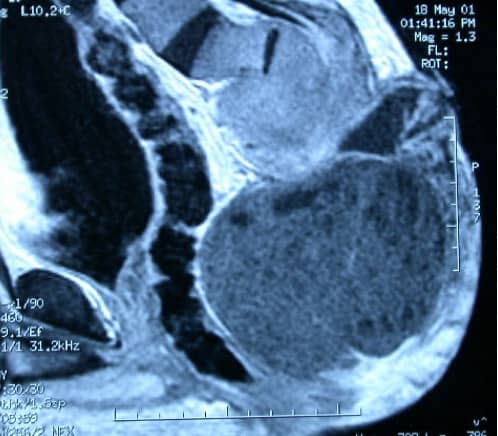
3.2.1.2.4.- Cordoma
Es un tumor extradural poco frecuente (<1 % de la totalidad de los tumores raquimedulares). Deriva de restos de la notocorda y crece lentamente. Se localizan preferentemente en región sacrocoxígea y también a nivel de atlas y axis. El diagnóstico se realiza con la Resonancia y el TAC para visualizar bien la afectación ósea. El tratamiento es quirúrgico intentando realizar resecciones radicales. A nivel del sacro plantea decisiones muy complejas de tomar, dados los altos riesgos de lesión neurológica que conlleva. Aunque son de crecimiento lento tienen una alta tendencia a recidivar. Se completa el tratamiento con radioterapia.
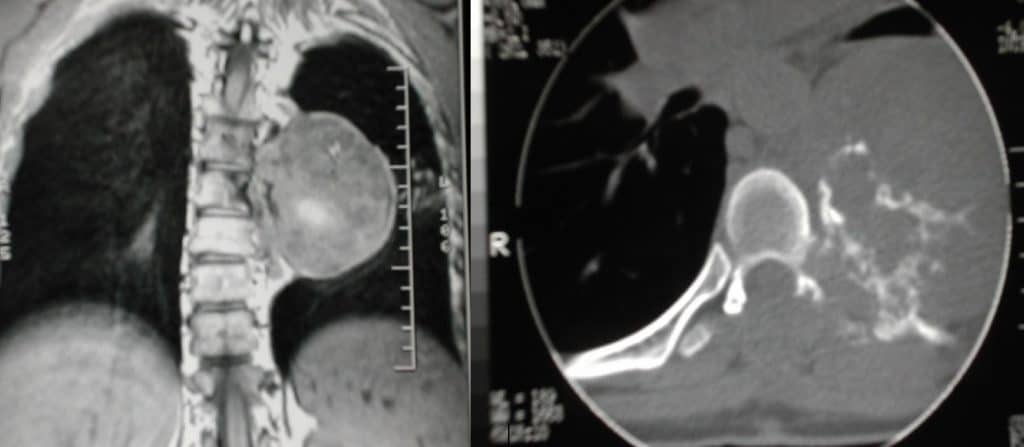
3.2.1.2.5.- Condrosarcoma
Tumor maligno que afecta al cartílago. Son tumores lobulados con zonas calcificadas
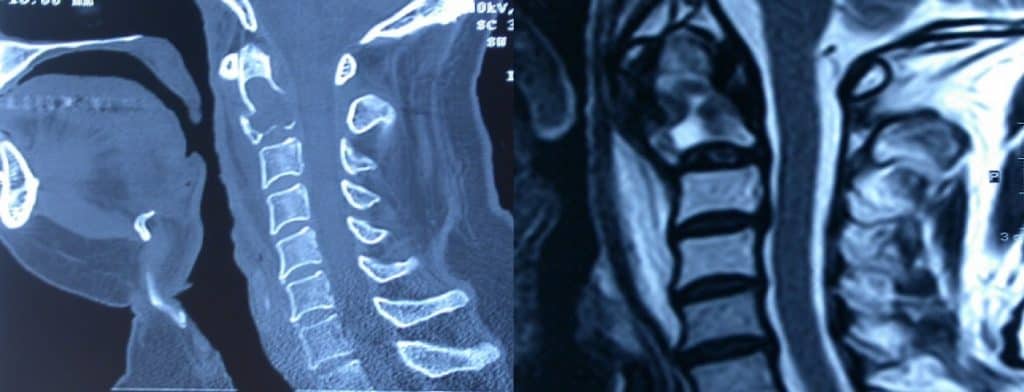
3.2.1.2.6.- Mieloma múltiple
Es una proliferación de células plasmáticas que infiltran los tejidos adyacentes. Si es una lesión única se denomina plasmocitoma. El diagnostico se puede realizar por determinación en orina de la proteina de Bence-Jones.
Clínica de cmpresión medular. Puede producir fracturas patológicas
Radiológicamente son lesiones líticas que pueden comprimir el canal.
El tratamiento es radioterapia y quimioterapia.
3.2.2.- Infecciones
3.2.2.1. – Osteomielitis, Discitis Piógena, Abscesos Epidurales Piógenos
Son poco frecuentes y se deben a sepsis generalizadas por un foco distal, con frecuencia de origen urinario. Diseminación hematógena o por contigüidad.
Otras veces puede ser una complicación postquirúrgica y en un 30 % de los casos no existe historia previa.
Los agentes más frecuentes son: estafilococo aureus, estreptococo, neumococo y pseudomonas.
Se origina en la estructura discal. Lo que los diferencia de las metástasis óseas cuyo origen es óseo.
Comienza con rigidez y dolor local, dolor radicular, ocasionalmente con fiebre y evoluciona a un cuadro de compresión medular, de forma aguda o subaguda. Las formas crónicas asemejan a un cuadro de tumor extradural. En casos de evolución aguda puede instaurarse un cuadro de paraplejía en tan solo unas horas.
Rx: signos de osteomielitis vertebral, en ocasiones. Signos de cambios en la curvatura fisiológica e incluso cifosis.
TAC y RM: signos inflamatorios a nivel del cuerpo vertebral (osteomielitis), disco (discitis), con material purulento en el espacio epidural (absceso epidural), que puede ocasionar compresión medular.
Puede ser necesario el tratamiento quirúrgico y, en muchas ocasiones, de urgencia. No se debe de abrir la duramadre, tras realizar la laminectomía. Se completa con tratamiento antibiótico.
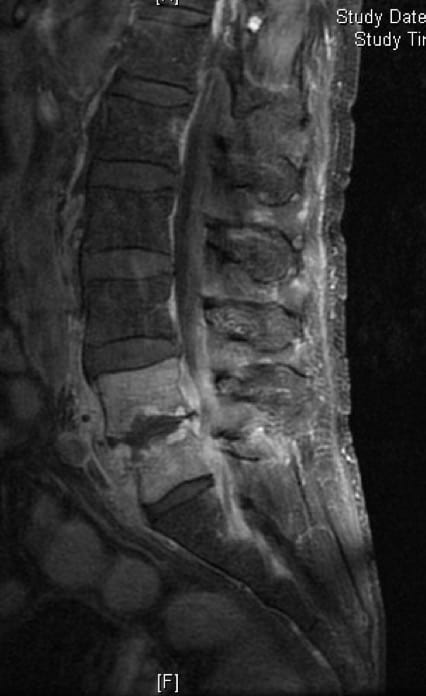
3.2.2.2. – Tuberculosis Raquimedular
De nuevo suelen presentarse casos con relativa frecuencia. Se requiere la presencia del neurocirujano sólo cuando existe lesión neurológica. El mal de Pott origina lesión neurológica por un colapso vertebral o por un absceso epidural secundario a tuberculosis del cuerpo vertebral.
La localización más frecuente es en columna torácica y suele haber historia previa de tuberculosis pulmonar. El curso suele ser insidioso.
La clínica más frecuente es de paraparesia progresiva, o paraplejía brusca cuando hay colapso vertebral.
Rx, TAC y RM.- similar a las osteomielitis-discitis piógenas, aunque con mayor frecuencia se ven imágenes de masas paravertebrales, correspondientes a abscesos.
El tratamiento es complejo. La finalidad es, en una sola sesión quirúrgica, intentar descomprimir, estabilizar y fijar el segmento vertebral afectado. A diferencia de las afecciones piógenas, la tuberculosis permite realizar no sólo descompresión del canal vertebral, sino que es posible la fijación con técnicas de artrodesis e instrumentación vertebral sin que exista riesgo de empeorar el cuadro infeccioso.
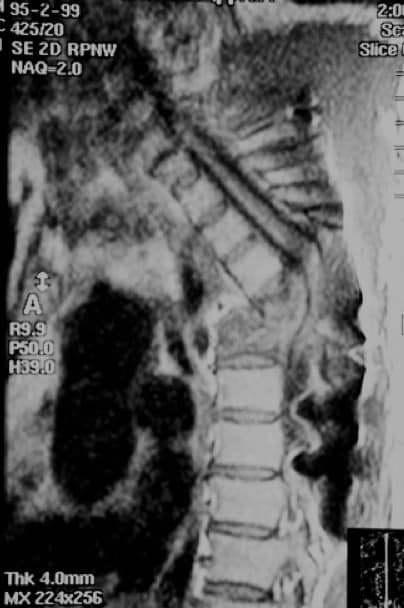
3.2.2.3. – Hidatidosis
En el momento actual es muy raro. La tenia echinococcus puede afectar los cuerpos vertebrales, por diseminación hematógena y producir un cuadro de compresión medular por invasión del espacio epidural o por fracturas patológicas de las vértebras afectadas. El tratamiento es médico-quirúrgico.