Tratamiento quirúrgico del dolor
Master en Neurocirugía funcional y Estereotáctica. Diploma en Neurociencia Clínica

Docentes:
Docente/s: Rafael García de Sola, Director de la Cátedra UAM “Innovación en Neurocirugía».
Universidad Autónoma de Madrid. Jefe del Servicio de Neurocirugía Hospital Ntra. Sra. del Rosario. Madrid.
Este artículo refleja las materias tratadas durante el Master de Neurocirugía Funcional y Estereotáxica que a la vez fueron expuestas por el Prof. Dr. Rafael García de Sola en el Congreso de la SENEC 2021.
Introducción
Objetivos
Contenidos
-
Bases fisiopatológicas del tratamiento quirúrgico del Dolor.
Técnicas quirúrgicas ablativas
Técnicas quirúrgicas neuromoduladoras
Ideas clave
Para comprender el tratamiento quirúrgico del Dolor es preciso:
-
1.- Conocer su fisiopatología.
2.- Profundizar en los conocimientos de la anatomía quirúrgica.
3.- Tener una visión global de las posibilidades ablativas. Sus beneficios, indicaciones posibles y contraindicaciones.
4.- De igual forma con las técnicas de neuroestimulación.
La mejora en el tratamiento médico y la falta de experiencia neuroquirúrgica han hecho menos visible la posibilidad del tratamiento quirúrgico a largo de la evolución clínica del paciente complejo con dolor crónico.
La revisión de los abordajes quirúrgicos, probablemente vuelva a ofrecer al paciente mayores posibilidades de control real de su dolor incoercible.
INTRODUCCIÓN AL TRATAMIENTO QUIRURGICO DEL DOLOR
Existen dos tipos de posibles actuaciones quirúrgicas sobre el dolor:
-
1.- Cirugía ablativa o destructiva. Consigue su objetivo lesionando centros o vías del dolor.
2.- Neuroestimulación-Neuromodulación. Su acción sobre un grupo de neuronas o haces de fibras introduce un cambio dentro de un sistema complejo, cuyo resultado final es la disminución de la información dolorosa a nivel de centros superiores.
Antes de referirnos a ellos, es importante dar un repaso a las bases fisiopatológicas del Dolor.
A continuación se expondrá en detalle los principales abordajes neuroquirúrgicos, con sus indicaciones, resultados y efectos adversos.
CONCEPTO DE DOLOR
No se pretende definir el dolor, sino dar unas pinceladas que nos permitan conocerlo mejor.
De entrada es una vivencia que se nos impone. Molesta. Se sobrelleva. Como dice Leriche en su libro sobre La Cirugía del Dolor (1939), no hay más que un dolor que sea fácil de soportar y es el dolor de los demás.
Sobre el Dolor han teorizado la Psiquiatría, la Neurología y otras ramas de la Medicina (Fisiología, Anatomía…). Tiene una función protectora y favorece la supervivencia y la evolución de las especies. Es uno de los temas centrales en el ámbito de la Filosofía, Teología. Está tratado en todas las religiones. Todos debaten. Es algo inherente a la naturaleza humana: Dolor-Sufrimiento, contraposición Dolor- Placer…
Cuando queramos contribuir a tratar o, mucho mejor, a controlar el dolor, tendremos que tener en cuenta todos estos factores.
Desde el punto de vista clínico, se pueden diferenciar claramente tres tipos de
Dolor:
-
1.- Como Síntoma
2.- Como Enfermedad (Bonica, 1980). Con las características que conlleva cualquier enfermedad: cronicidad, estabilidad, alteración del comportamiento.
3.- Dolor como Sistema complejo. Al igual que el sistema extrapiramidal ¿. Donde cada enfermedad es una entidad precisa, con su patogenia, clínica, diagnóstico y tratamiento diferentes. Todas metidas en el mismo “saco” (Fig. 1). O significando que hay una alteración específica y diferente dentro de la estructura que configura el Dolor en el sistema nervioso. Similar a cómo la enfermedad de Parkinson, el temblor esencial, las distonías o las coreoatetosis son enfermedades diferentes del sistema extrapiramidal.

- DOLOR SÍNTOMA
- DOLOR ENFERMEDAD
- SISTEMA “NEUROALGICO”?
MECANISMOS DE MODULACIÓN DEL DOLOR
I.-NOCICEPTORES Y NERVIO PERIFERICO
Un estimulo nocivo es aquel que potencialmente puede producir daño tisular y fisiológicamente se traduce en percepción de dolor por el sujeto consciente. La patología que produce dolor se relaciona a menudo con lesión tisular (heridas, fracturas…), inflamación, tracción, etc… Pero ya aquí, en el inicio de su percepción, comienza la complejidad del fenómeno doloroso.
En los años 30 Adrian y Zotterman fueron los primeros en analizar la actividad de los receptores sensoriales. Refieren que los impulsos a través de las fibras Aδ y C amielinícas pueden estar en relación con los estímulos dolorosos. Y aunque parece que el receptor primario que traduce el dolor es la terminación nerviosa libre, que conduce más lentamente la información, también hay nociceptores mecánico-sensitivos, térmicos o polimodales (que responden a estímulos mecánicos, químicos o térmicos) a nivel de piel, vísceras o músculo (Baumann, 2002).
La activación de las fibras Aδ se asocia con el dolor rápido, bien definido, mientras que las fibras C conducen la segunda sensación de dolor, lento, difuso, de mayor duración. En general las fibras gruesas tienen un umbral de estimulación más bajo, tanto natural como eléctrico; de forma que un estimulo suficientemente intenso como para activar las fibras delgadas amielinícas está por encima del necesario para estimular las fibras gruesas que conducen sensación diferente del dolor. Por consiguiente, es posible que no haya una respuesta electiva a un estímulo nocivo en la piel y, por tanto, se traduzca una información no totalmente específica de estimulación dolorosa. Acerca de este problema de transmisión sensitiva se han efectuado varias teorías, destacando las siguientes (Bonica, 1990):
- 1) Teoría de la especificidad de la sensación, de Mac von Frey (1894). Defiende que cada tipo de receptor transmite información de su estímulo específico.
2) Teoría de la sumación de estímulos de Goldscheider (1894). Propuso que el dolor se produce por sumación de impulsos dentro del Sistema Nervioso, después de aplicar estímulos mecánicos o térmicos a la piel.
3) Teoría del comportamiento del impulso, de Nafe (1934). La sensación no se basa en receptores específicos, sino en la forma en que un número determinado de impulsos es trasladado en el espacio (número y tipo de fibras) y en el tiempo (frecuencia). Melzack y Wall (1965) incorporaron y modificaron esta teoría manteniendo una postura ecléctica que añade la posibilidad de la existencia de especificidad de estímulo y ausencia del mismo.
Hoy día, la opinión mayoritaria esta recogida por Kerr y Wilson (1978), partidarios de que la duda entre la especificidad de la información dolorosa o la dependencia del comportamiento del estímulo parece que se está inclinando hacia admitir un sistema especifico en que los nociceptores, con sus correspondientes fibras aferentes, activan diferentes tipos de neuronas en el Sistema Nervioso Central (SNC). Algunas de ellas son unidades de alto umbral (responden sólo a estímulos nocivos), pero en otras convergen estímulos nocivos y no nocivos, tendiendo a oscurecerse algo su especificidad. Aunque ante un estimulo nocivo responden con un aumento en la frecuencia de las descargas.
II.- GANGLIO RAQUIDEO- RAIZ DORSAL
A nivel del ganglio raquídeo hay dos tipos de células: Las de mayor tamaño parece que dan origen a axones mielinizados y las pequeñas, a axones amielínicos. Estas últimas son nociceptivas y pueden subdividirse en dos tipos (Hökfelt, et al., 1975), según contengan como neurotransmisor sustancia P o somatostatina. Randic y Miletic (1977) sugieren que la sustancia P puede jugar un papel como transmisor excitador a nivel de la primera sinapsis, mientras que la somatostatina puede tener un efecto modulador inhibitorio.
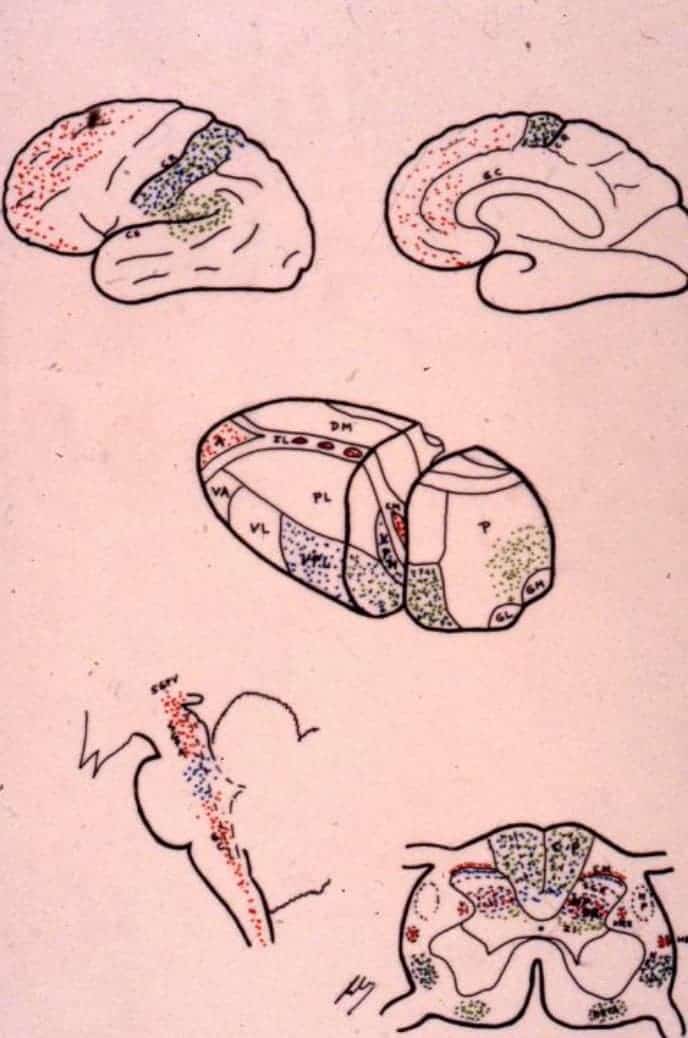
Las fibras gruesas convergen en un haz medial y penetran en los cordones posteriores, enviando colaterales en pequeña proporción a la zona dorsomedial del asta posterior, a nivel de la substancia gelatinosa de Rolando, y el resto terminan a nivel de las láminas IV y V de Rexed y en la sustancia gris intermedia (Fig 2).
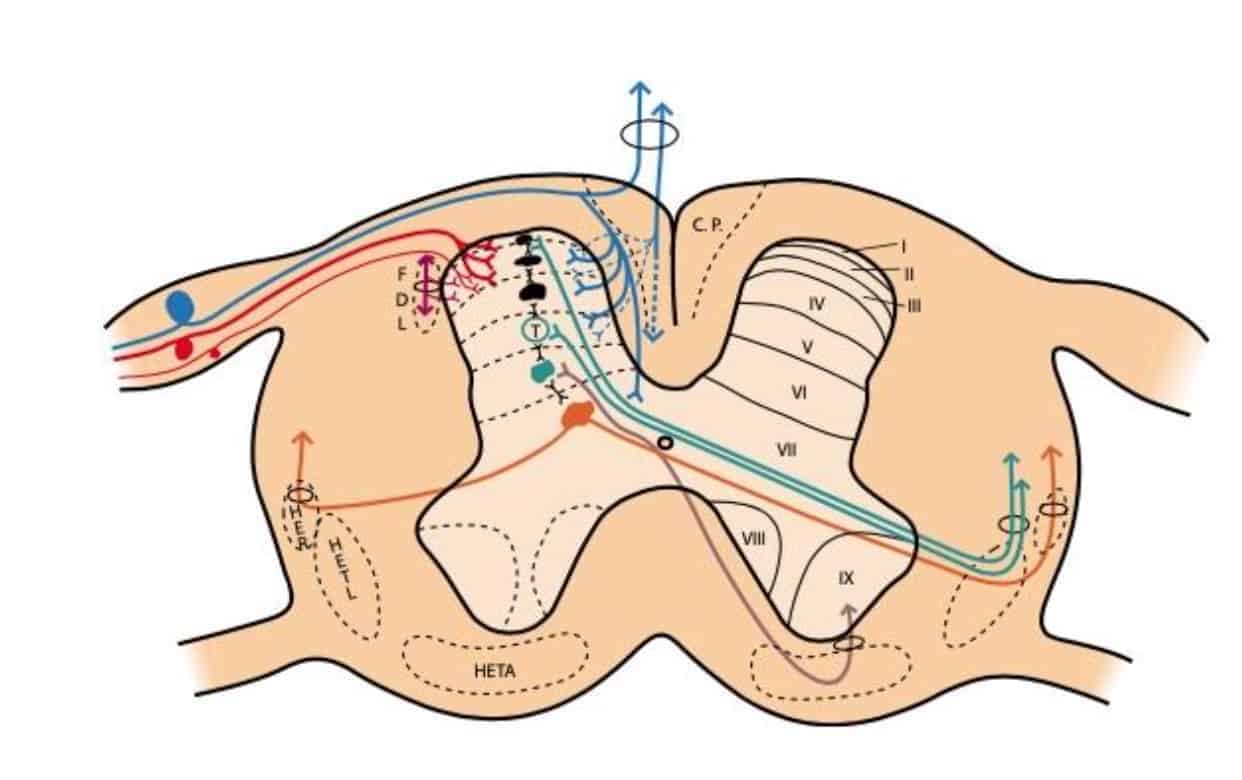
Las fibras Aδ y C convergen en dos haces: uno mayor en la porción ventrolateral de la raíz posterior y un segundo haz más pequeño en la superficie dorsomedial. Ambos tipos de fibras llegan al tracto de Lissauer y se distribuyen fundamentalmente a nivel de las láminas I, II, V.
III.- ASTA POSTERIOR MEDULAR
La substancia gris medular fue dividida por Rexed (1952), dependiendo de la citoarquitectura, en 10 láminas de las que las siete primeras toman parte en el fenómeno doloroso, siguiendo el siguiente esquema simplificado (Fig. 1):
- a) La lamina I (capa marginal de Waldeyer) está formada por grandes neuronas cuyas aferencias las forman en su mayor parte fibras Aδ y en menor proporción las fibras C amielínicas (Kumazawa y Perl, 1978). Se proyectan en los núcleos talámicos ventral posterior e intralaminares, así como a nivel de la sustancia gris periacueductal (SGPA) (Kerr, 1975). Estas neuronas pertenecen al tipo I de Iggo (1976) que responden a estímulos dolorosos o casi nocivos.
b) En las láminas II y III (Substancia Gelatinosa de Rolando) se encuentran neuronas de pequeño tamaño que reciben la mayoría de las aferencias a través de fibras C y el resto por colaterales de las fibras Aβ de los cordones posteriores (Kumazawa y Perl, 1978). Sus prolongaciones forman parte del fascículo dorsolateral de Lissauer a lo largo de tres o más segmentos. La función es aún oscura, actuando como interneuronas con una acción de mantener una influencia inhibidora o excitadora sobre las células de las laminas I, IV, y V (Cervero, et al., 1977).
c) Las células de las laminas IV, V, y VI (núcleo propio, cuello o substancia reticular y base respectivamente del asta posterior) son neuronas nociceptivas de t ipo II de Iggo, que responden a estímulos mecánicos periféricos de bajo umbral, pero que aumentan la frecuencia de descargas cuando el estímulo se hace nocivo (Hillman y Wall, 1969). Para Mayer y Price (1976) la activación de este tipo II de neuronas puede llevar a la experiencia dolorosa. De estas laminas se origina el haz espinotalámico que se proyecta a los núcleos sensitivos talámico (VPM y VPL) y sustancia gris periacuaductal (SGPA).
d) La lamina VII (zona intermedia) da origen al fascículo espino-reticular, junto al haz espinotalámico, y sus neuronas responden a estímulos que ponen en marcha los receptores de más alto umbral (Albe-Fessard, 1973).
IV.- VIAS PORTADORAS DE INFORMACION DOLOROSA
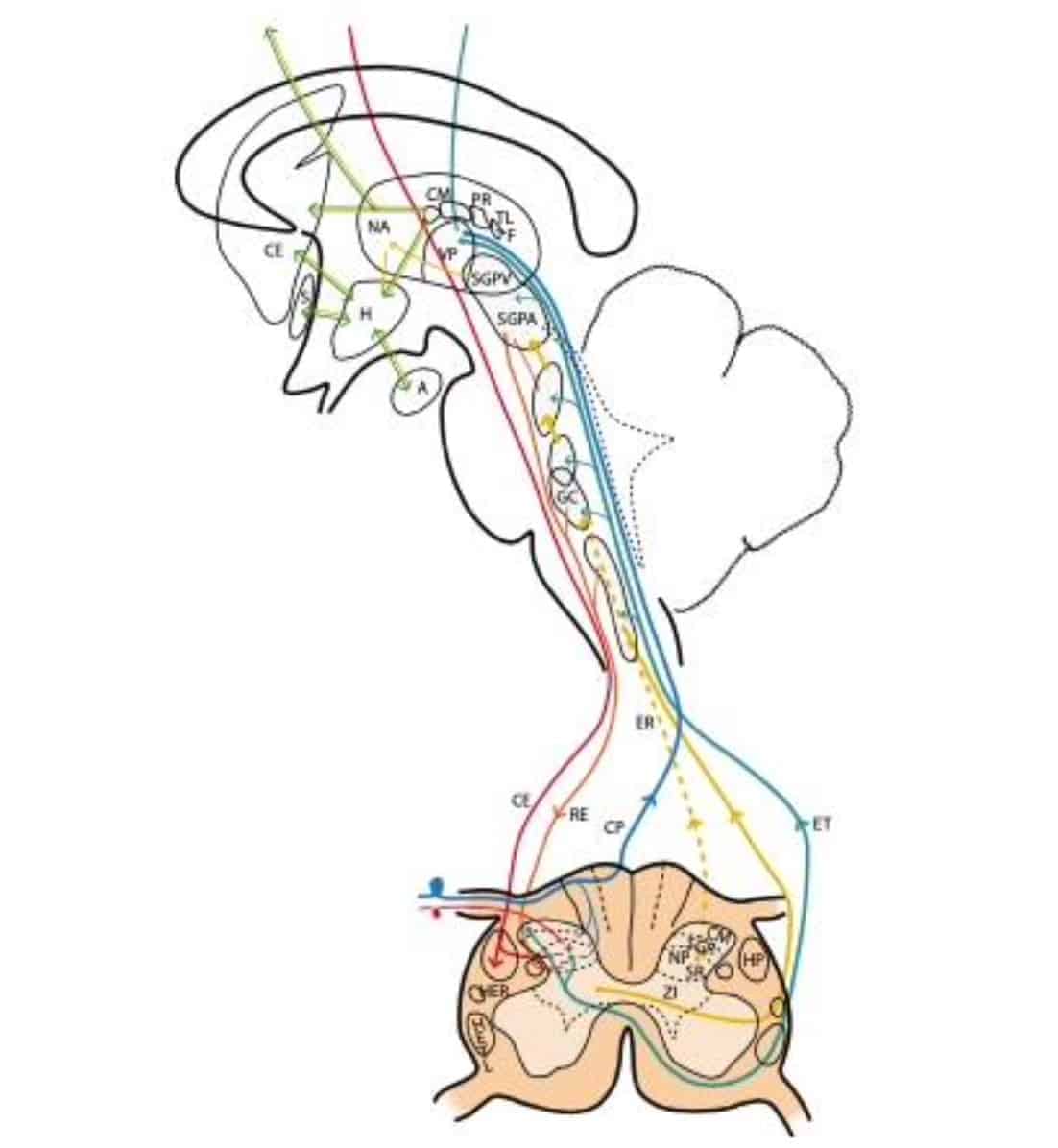
Al menos hay tres tipos de vías dolorosas ascendentes que llevan información hacia el cerebro (Figs. 2 y 3):
- 1º Vía neoespino-talámica o haz espino-talámico lateral. Es una modificación filogenética para mejorar la transmisión directa de impulsos dolorosos a niveles conscientes. Parece que se origina a nivel de las láminas I, IV, VI Y VII (Trevino, et al., 1973), cruzan la línea media a nivel de la comisura blanca anterior y ascienden por el cuadrante antero-lateral de la médula. Se proyectan, tras formar parte del lemnisco medial, a nivel de los núcleos sensitivos talámicos (VPL, la zona del cuerpo; ventral- póstero-medial (VPM), la zona de la cara) y de aquí al córtex sensorial post-rolándico; transmitiendo información sobre los aspectos discriminativos de la experiencia dolorosa.
2º Vía Paleoespinotalámica. Tiene su origen en las mismas neuronas tipo I y II que la anterior vía. Pero la diferencia es que dan numerosos colaterales a la formación reticular del tronco cerebral. Se forma una vía multisináptica que asciende hacia áreas en relación con el comportamiento (hipotálamo, núcleos intralaminares, parafascicular y centro mediano talámicos, así como circuito límbico). Su proyección es bilateral y parece que este sistema esta implicado en las cualidades motivacionales y afectivas del dolor (Baumann, 2002).
3º Sistema Arquiespinotalámico. Mucho menos diferenciado, parece ser una vía multisináptica ascendente a nivel de la substancia reticular central medular, hasta zonas diencefálicas y corticales similares al tracto paleoespinotalámico, incluyendo el sistema límbico (Kevetter, et al.,1982).
Además hay que considerar un sistema doloroso descendente que parece estar relacionado con la inhibición del dolor. Se descubrió a raíz de observar que la estimulación de la SGPA en ratas producía analgesia (Reynolds, 1969). Fenómeno que se denomino SPA (stimulation-produced analgesia) (Mayer y Hayes, 1975) y que también fue apreciado en el hombre (Richardson y Akil, 1977). Dicho sistema descendente inhibidor con acción sobre las astas posteriores esta vehiculizado por las vías retículoespinal, cordones posteriores y córticoespinal. Aunque, como veremos mas adelante, existen circuitos inhibidores a nivel de cada estación o relé de la vía dolorosa (asta posterior, tronco cerebral, tálamo…).
V. FORMACION RETICULAR DEL TRONCO CEREBRAL
Es difícil obtener una definición científica estricta de los criterios necesarios para designar a una determinada zona del SNC como ¨reticular¨ o no. Por exclusión, y a diferencia de los bien delimitados núcleos y haces de fibras, se encuentran zonas donde la substancia gris y blanca se entremezclan, las fibras forman haces en todas direcciones y las neuronas se encuentran distribuidas de forma difusa, con unas formas mal definidas de agrupamiento. Es posible que el conocimiento actual de la morfología y conexiones neuronales no haga apreciar una determinada organización que realmente existe.
La mayoría de los autores incluyen como formación reticular (FR) áreas localizadas profundamente a nivel de bulbo, protuberancia y mesencéfalo. Menos acuerdo hay para incluir regiones centrales de la sustancia gris medular, núcleos no específicos talámicos y ciertos núcleos hipotalámicos (Fig. 3).
La FR, por otra parte, se considera como lo más antiguo filogenéticamente, representando la ¨red nerviosa libre¨ sobre la que posteriormente han aparecido partes del SNC más circunscritas y altamente organizadas. Pero incluso los SNCs más primitivos poseen zonas difusas o bien altamente organizadas. Por lo que seria preferible mirar la FR como la evolución de estas zonas o elementos más difusamente organizados, siendo sus características generales las siguientes:
- a) Son grupos de neuronas y fibras colocadas profundamente y con una organización estructural difusa.
b) Las vías de conexión son anatómicamente difíciles o imposibles de definir y fisiológicamente son complejas y a menudo polisinápticas. c) Pueden ser reconocidos componentes de sistemas tanto ascendentes como descendentes. d) Ambos sistemas contienen elementos cruzados y no cruzados, obteniéndose al estimular respuestas ipsi y/o contralaterales. e) Intervienen en funciones somáticas y viscerales
En este sistema complejo hay oportunidades masivas para la convergencia o divergencia de la información. Además las neuronas son o excitadoras o inhibidoras, colinérgicas o aminérgicas, variando su proporción dependiendo de las regiones. Debiendo tener en cuenta que una de las numerosas funciones de la FR es la homeostasis a corto y largo plazo, con sus vías descendentes hacia centros autonómicos inferiores y sus vías ascendentes que llevan información visceral y somática hacia el hipotálamo y sistema límbico. En este sentido, podemos encontrar centros relacionados con los mecanismos de control cardiovascular, respiratorio, gastrointestinal, así como con las vías nociceptivas ascendentes, bilaterales ¨de dolor lento¨. En relación con este tipo de dolor se han identificado determinadas regiones:
- 1.- Núcleo reticular gigantocelular y región reticular lateral, a nivel del bulbo y protuberancia. Reciben proyecciones del haz espino-talámico, así como de las zona más profundas de las substancias gris medular (Willis, 1985).
2.- Núcleos reticulares del rafe magno y substancia gris periacueductal (SGPA), a nivel del mesencéfalo (Kerr, 1975). La estimulación de esta última en el hombre provoca sensaciones somáticas y viscerales acompañadas por reacciones emocionales intensas.
3.- La SGPA ventrolateral y la substancia gris periventricular (SGPV), lateral al III ventrículo, en la región de la comisura posterior (Reynolds, 1969), son las zonas cuya estimulación produce una analgesia más efectiva con un mínimo de efectos colaterales. Esta analgesia post-estimulación (APE) (Trevino, et al., 1973) puede durar varias horas tras el estimulo, sugiriendo una activación de un sistema multisináptico con un mecanismo similar a la analgesia por opiáceos (Hosobuchi, et al., 1977).
Ambas zonas efectivamente son ricas en receptores opiáceos; su estimulación produce liberación de endorfinas en LCR. Existe, por otra parte, tolerancia cruzada entre la APE y la analgesia opiácea, así como la APE puede ser revertida por la naloxona (Akil, et al., 1976).
VI.-TALAMO
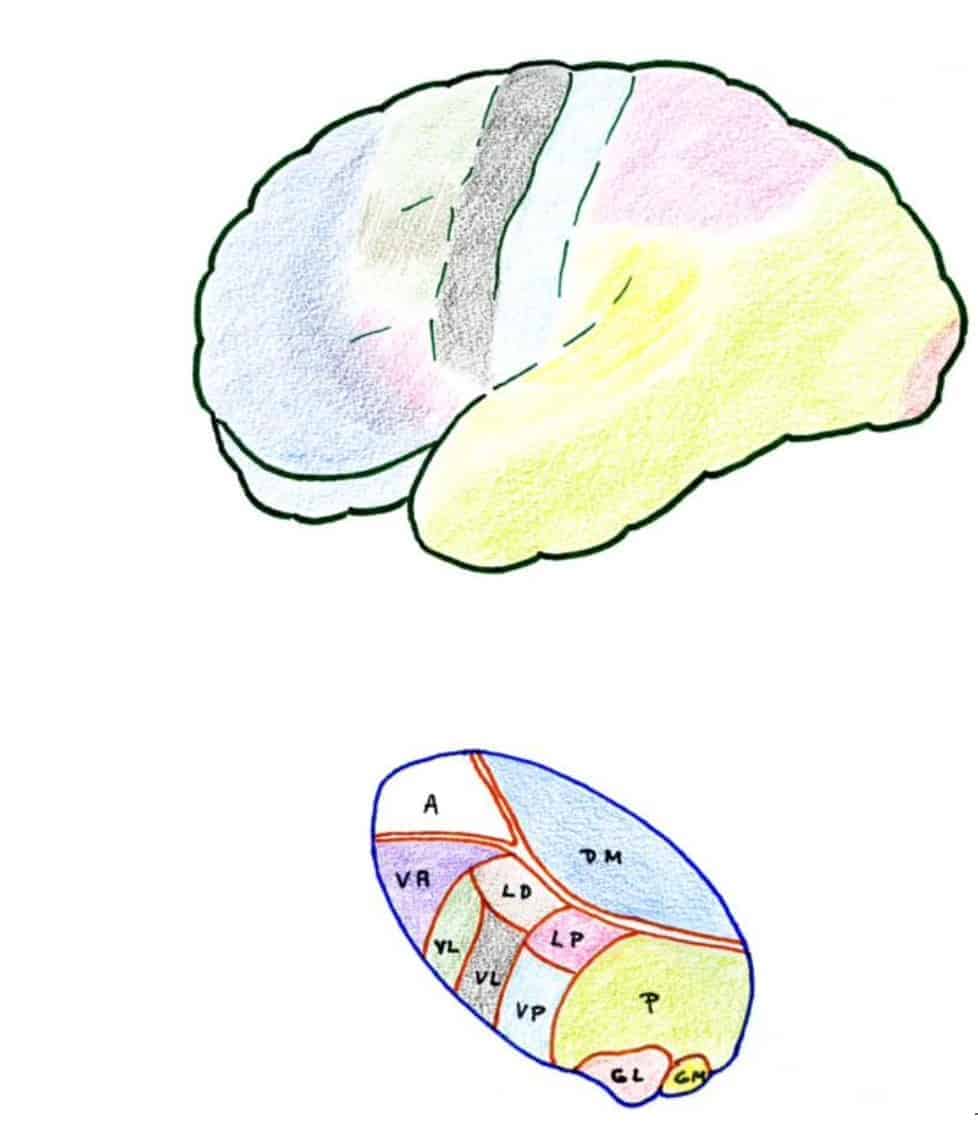
Las estructuras talámicas que reciben directamente proyecciones de la vía del dolor espinotalámica se corresponden con tres agrupaciones de núcleos (Mehler, 1962) (Fig. 4):
- A.- Complejo Ventrobasal. Pertenecen a este complejo los núcleos VPL (que recibe proyecciones somatosensoriales representativas del cuerpo) y el VPM (que recibe las proyecciones del área trigeminal). Las aferencias provienen en su mayoría de los núcleos de los cordones posteriores y complejo trigeminal, que caminan por el lemnisco medial. Las otras zonas que se proyectan en estos núcleos son: a) La capa marginal y núcleo propio de las astas posteriores (y la zona correspondiente del núcleo espinal del trigémino), cuyas aferencias alcanzan la parte más caudal de estos núcleos, manteniendo una representación somatotópica (Kerr, 1975). b) La substancia reticular mesencefálica (Bowsher, 1976).
La estimulación de la porción dorsal de este complejo, en el hombre despierto, provoca sensaciones táctiles no dolorosas (Tasker y Emmers, 1975). Sin embargo, a nivel de las zonas caudal y ventral, se producen sensaciones dolorosas localizadas (Hassler y Riechert, 1959). Por el contrario, lesiones de la región ventrocaudal produce cambios en la sensibilidad al dolor que posteriormente puede conducir a una hiperpatia (Richardson y Akil, 1977).
En resumen, estos núcleos VPM Y VPL parecen estar implicados en la localización e identificación de estímulos inocuos y nocivos que caminan preferentemente por la vía lemniscal.
B.- Complejo Posterior. Comprende una zona mal definida entre el cuerpo geniculado medial y el núcleo pulvinar. Recibe aferencias de los núcleos de los cordones posteriores medulares y de la vía espinotalámica, así como vías descendentes córtico-talámicas del cortex somatosensorial. Se proyecta el área cortical retroinsular.
Su estimulación produce sensaciones desagradables. La función de este complejo posterior en el dolor está aún mal entendida y multiforme, pareciendo que algunas células son inhibidas por la inyección sistémica de morfina (Shigenaga y Inoki, 1976).
C. Núcleos intralaminares. Reciben aferencias de la formación reticular, así como de la capa marginal del asta posterior medular y núcleo espinal del trigémino. Prácticamente no reciben proyecciones de la vía lemniscal.
Al igual que el complejo posterior, recibe información ipsi y contralateral (Albe- Fessard, et al., 1974). Su estimulación provoca sensaciones desagradables difusas y en ocasiones dolor no bien localizado. Una lesión a este nivel puede aliviar el dolor incoercible (Richardson y Akil, 1977) y sus células pueden también ser inhibidas por la administración de morfina.
VII. CORTEX
Constituye el nivel superior de la vía del dolor, pudiéndose diferenciar y destacar tres áreas somatosensoriales diferentes (Fig. 4):
- A.- Primaria: Se corresponde con la circunvolución postrolándica, incluyendo su extensión medial en el lóbulo paracentral. Recibe las proyecciones de los núcleos VPL y VPM. La estimulación produce sensaciones bien localizadas de tipo táctil, temperatura y rara vez dolor (Penfield y Jasper, 1954). Su extirpación puede producir una pérdida de la capacidad discriminativa sensorial y a veces mejora el dolor, aunque puede aparecer una hiperpatía posteriormente (White y Sweet, 1969).
- B.- Secundaria: Se encuentra a nivel del opérculo superior de la cisura de Silvio, por detrás de la cisura de Rolando y región retroinsular. Muchas de sus células responden a estímulos nocivos y su estimulación provoca sensaciones dolorosas localizadas (Whitsel, et al., 1969). Existen proyecciones reciprocas hacia el tálamo, a los núcleos VPM, VPL y mediales, y las lesiones a este nivel alteran la sensibilidad al dolor, no afectando la capacidad discriminativa somatosensorial (Treede, et al., 1999).
- C.- Terciaria: Se correspondería con las zonas del cíngulo e ínsula. Están en relación con el sistema límbico y las sensaciones viscerales. Conectan con los núcleos talámicos mediales y están en relación con el componente afectivo-emocional del dolor (Baumann, 2002).
Las técnicas de resección cortical han sido abandonadas, debido a los fracasos en cuanto a obtener alivio del dolor y las complicaciones posteriores que provocaban. Sólo han quedado como intervenciones antiálgicas la leucotomía y la cingulotomia. Aunque sus efectos sobre el dolor se deben más a su acción sobre la personalidad y el componente afectivo de sufrimiento que sobre el dolor como actividad sensorial (White y Sweet, 1969). Quedando aún en la obscuridad la función de la corteza cerebral ante el fenómeno doloroso.
VIII. VIAS DE MODULACION DEL DOLOR
A.- NEUROFISIOLOGICA
La experiencia muestra que muy rara vez un dolor crónico es reducido de forma repentina y duradera a cero tras algún tipo de intervención quirúrgica, de actuación física o conductual. Por lo general, tras un régimen adecuado, se consigue que esta persona vea reducido su dolor y actúe modificando o modulando su comportamiento a largo plazo, lo que le hace tener una vida más provechosa y productiva.
Se han hecho numerosos esfuerzos por explicar esta capacidad de modulación y modificación que se tiene sobre el dolor. Siendo Melzach y Wall (1965) quienes expusieron una teoría, que aún persiste aunque modificada, para explicar estos fenómenos a nivel del primer relé del sistema sensitivo doloroso. Esta teoría de control de la compuerta (gate control theory) básicamente es la siguiente:
Existe, a nivel segmentario medular, una interacción dinámica entre la entrada de información a través de las fibras gruesas mielínicas (A) y la entrada por las fibras finas (Aδ) y amielínicas (C). Dicha interacción se efectúa a nivel de las láminas II y III (substancia gelatinosa de Ronaldo [SGR]), donde existen neuronas que ejercen una inhibición presináptica de ambos tipos de fibras en sus sinapsis con las células T (transmisoras), presumiblemente localizadas en la lámina V, de las que salen directa o indirectamente las fibras espinotalámicas.
Por un lado las fibras gruesas envían colaterales que excitan a las interneuronas de la SGR, con lo cual se potencia la inhibición de las células T (se cierra la compuerta, impidiendo el paso de información dolorosa). Por el contrario, las fibras amielínicas envían información inhibidora a la célula de la SGR, reduciéndose la inhibición de las células T (abriéndose por consiguiente la compuerta que permite el paso de la información dolorosa).
Melzach y Casey (1968) modificaron esta teoría del comportamiento mediante otra teoría de ¨central control trigger¨ (control central de la puesta en marcha), que implicaba que la información transmitida por las fibras gruesas a través de los cordones posteriores puede activar mecanismos inhibitorios centrales, cuya acción descendente modularía la transmisión del dolor por las neuronas del asta posterior. Las células T pueden ser inhibidas o excitadas por información procedente del tronco cerebral, que utilizan los cordones posteriores como vía de transmisión (Iggo, 1976). Melzach, en 1975, sugiere además que ciertas formas de neuroestimulación podrían activar un mecanismo central predisponente (central biasing mechanism) que inhibe las señales dolorosas de origen patológico y cronificado. Este mecanismo, con base neurofisiológica o neurohumoral, retrasaría los procesos patológicas de fijación y correlación con antiguas experiencias, que se realizan simultáneamente a la recepción de la señal dolorosa (en la que se conjuntan las entradas sensitivas, vías inhibidoras del tronco cerebral, actividad del Sistema Nervioso Autónomo, situación de expectación y ansiedad del individuo, estructura de la personalidad etc.).
Ahora bien, lo mismo que se va conociendo cada vez mejor la existencia de un sistema modulador a nivel del primer relé en el asta posterior medular, hay sin embargo otros sistemas moduladores más complejos y menos comprendidos que se sitúan a niveles superiores del SNC. Como ejemplo, sólo citaremos el hecho de que la estimulación a nivel del núcleo VPL (Shealey, 1967) o del brazo posterior de la capsula interna (vía talamocortical de aferencias especificas) (Adams, et al., 1974), puede producir analgesia. Explicándose este fenómeno por un efecto inhibidor de estas estructuras sobre otros núcleos del tálamo o bien sobre el córtex (Bowsher, 1976). Aunque hoy día aún no se conocen bien las convergencias a nivel talámico entre el sistema específico lemniscal y el extralemniscal, ni desde el punto de vista anatómico ni fisiológico.
B.- NEUROQUÍMICA
En 1975 Hughes et al., aislan dos pentapéptidos endógenos de acción morfino- mimética: metionina y leucina-encefalina. Posteriormente se identifican péptidos mayores, endorfinas, con la misma acción y a numerosos niveles de SNC (Bloom, etb al., 1976; Guillemin, 1976). Siendo las SGPA y SGPV unas de las áreas con mayor abundancia en receptores opiáceos endógenos y en la que la analgesia producida por su estimulación (APE) tiene consecuencias conductuales similares a las obtenidas tras la administración de morfina.
Las encefalinas y endorfinas tiene muchos lugares potenciales en los que, o bien modulan, o bien sirven de intermediarios activando otros sistemas. Y así, como ejemplo, a nivel de la zona marginal y SGR existen terminales encefalinérgicas; recibiendo también, al parecer, estas mismas neuronas numerosas proyecciones de terminales de aferencias nociceptivas primarias cuyo neurotransmisor es la sustancia P. Tanto la morfina como las encefalinas producen una inhibición de la liberación de la sustancia P, así como reducen la respuesta de las neuronas a la estimulación dolorosa de sus respectivos órganos periféricos. Aunque, por otro lado, tanto la morfina como las encefalinas pueden actuar a este nivel medular activando un sistema serotoninérgico descendente bulboespinal, de inicio a nivel de los núcleos del rafe, que reciben su información de la SGPA Tanto la estimulación eléctrica de la SGPA como la inyección de opiáceos a este nivel van a producir el mismo efecto analgésico, que puede ser bloqueado mediante la administración sistémica de naloxona o mediante lesiones, bien a nivel de los núcleos del rafe como a nivel de la vía descendente en el fascículo dorsolateral de Lisauer (Akil, et al., 1979).
Sin embargo, los mecanismos son aún más complejos dado que, por ejemplo, los mismos impulsos nociceptivos pueden (a través de colaterales hacia el núcleo reticular gigantocelular y de aquí a la SGPA) inhibir (vía funículo dorso lateral) los impulsos que desde la periferia llegan a las células de la lamina II y V (Basbaum y Fields, 1978). De forma que existen mecanismos de retroalimentación negativos, mediados por endorfinas y utilizando vías serotoninérgicas.
IX. TEORIA DE LA COMPUERTA
Sin duda, el aumento de los conocimientos neuroendocrinos ha llevado a una mayor comprensión de fenómenos que no eran bien explicados al aplicar exclusivamente la teoría del control de la compuerta. Mas, a pesar del todos los recientes avances, hemos de admitir que nuestro conocimiento aún es bastante grosero y no es posible obtener una idea clara del conjunto. Y, por el momento, quizás sea mejor tener una idea más simple de lo que puede ocurrir a nivel de cada relé de la vía dolorosa (asta posterior, tronco cerebral, tálamo…), que nos pueda servir para explicar de una forma nítida los efectos positivos de la neuroestimulación.
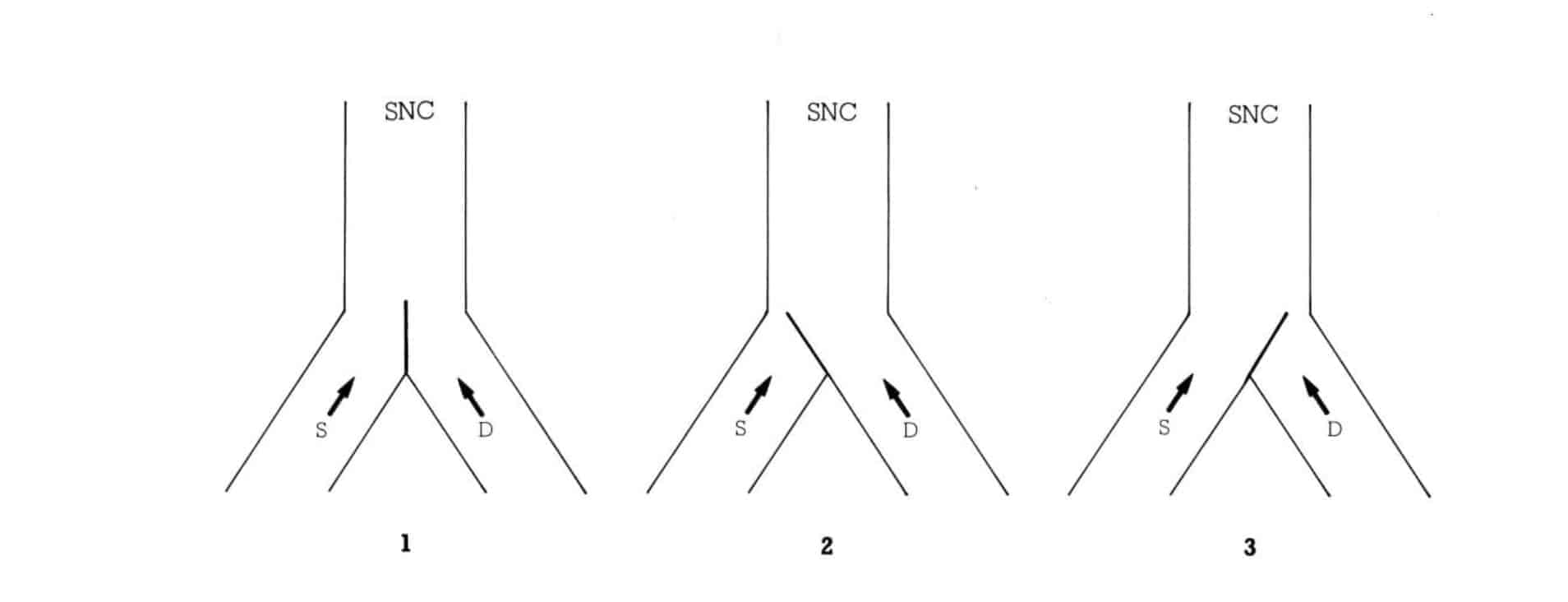
En este sentido, podemos figurarnos que hacia niveles superiores cerebrales
(C) llega información sensitiva (S) y dolorosa (D) (Fig. 6). Si por cualquier razón aumenta esta última, la compuerta girará hacia la izquierda, impidiendo el paso de información sensitiva (prestamos mayor atención al dolor, al estimulo nociceptivo que se ha producido).
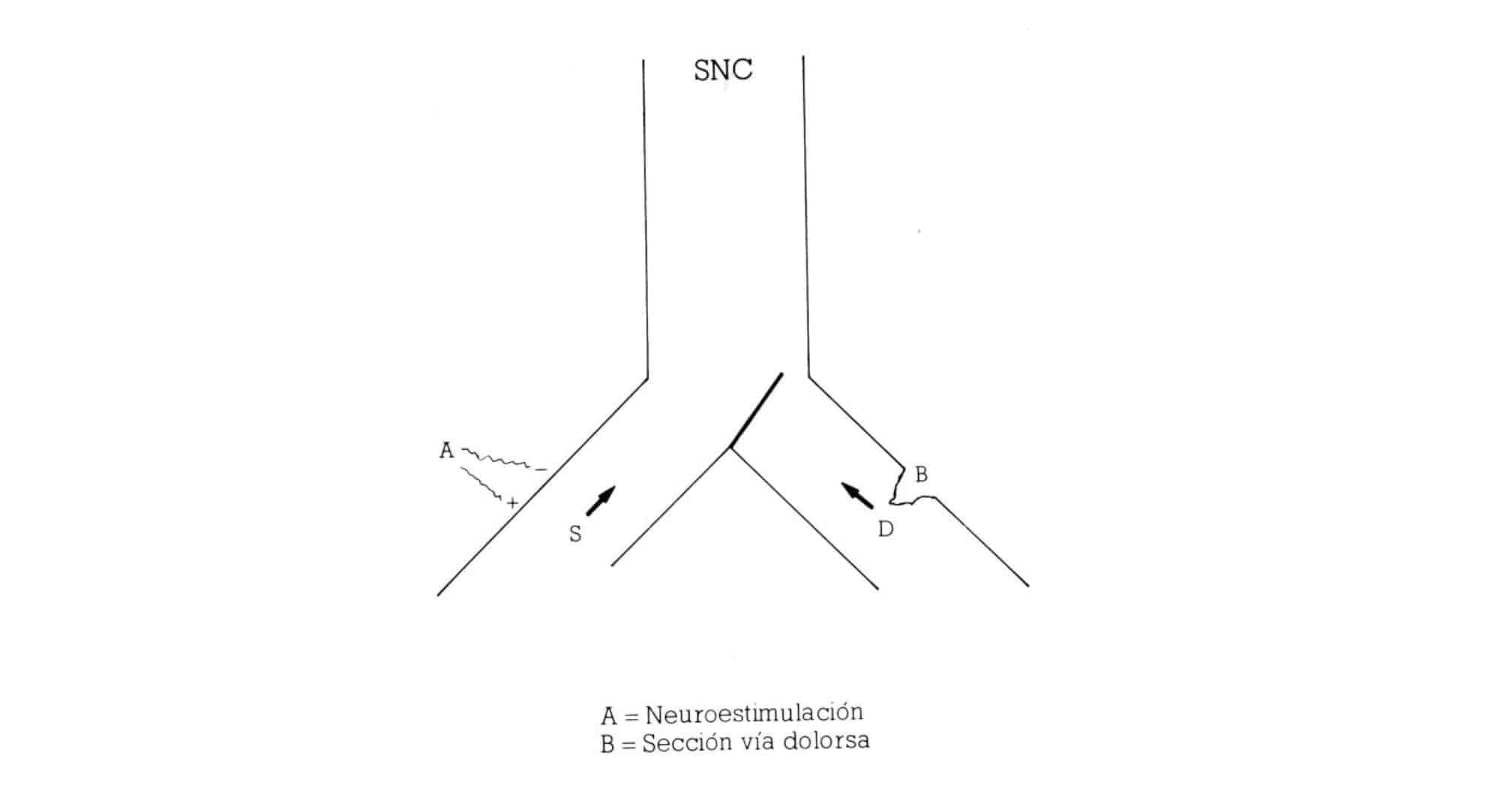
Si esta información se mantuviera constante, se cronificara, nosotros podríamos reducirla de dos formas (Fig. 7): Inhibiendo las aferencias de la misma vía dolorosa (por medios farmacológicos, instrumentales o incluso quirúrgicos) o actuando sobre la vía sensitiva aumentando sus aferencias. Esto último es posible hacerlo de una forma natural (por ejemplo, el hecho de frotarse la piel tras recibir un golpe, amortigua el dolor) o por medio de la neuroestimulación.
EL DOLOR, DESDE EL PUNTO DE VISTA CLÍNICO
TIPOS DE DOLOR
Se podrían diferenciar o clasificar varios tipos de dolor, que exponemos a continuación de forma muy sumaria, aunque después los explicaremos más ampliamente:
A.- De acuerdo con su duración: AGUDO o CRONICO
El dolor agudo es fisiológico. Avisa del daño tisular y es transitorio y reversible. Produce respuestas coordinadas de defensa, como el reflejo de retirada, las respuestas autonómicas de aumento de la frecuencia cardíaca y tensión arterial, con activación del eje hipotálamo-hipofisario, a la vez que inmoviliza para favorecer la reparación tisular.
El dolor se puede hacer crónico, por el mantenimiento en el tiempo del estímulo nocivo. O por alteración de los mecanismos implicados en la generación y desaparición del dolor. De manera que se perpetúa ya, no como un síntoma de la causa o enfermedad que lo produjo, sino como una enfermedad en sí mismo. Aunque se haya solventado el problema que lo generó. Bonica (1990) establece un plazo de 3 meses para diferenciar el dolor agudo del crónico.
Pero quizás una de las mejores descripciones del dolor agudo y crónico sea la de Hendler (1982). Distingue 4 estadíos:
- I.- Agudo.- Hasta 2 meses del inicio.
Desde el punto de vista clínico es el dolor “normal”. No implica ningún tipo de trastorno psicológico. Cede a los analgésicos. La persona espera curarse.
II.- Subagudo.- De 2 a 6 meses del inicio.
La persona comienza a tener distress, somatiza el dolor. Inicia ansiedad e irritabilidad.
Aparece insomnio, aislamiento social. Cada vez más preocupado por el dolor, que toma un importante protagonismo en su vida. Disminuye la actividad sexual.
El paciente toma sedantes y analgésicos y espera y confía en que ceda el dolor.
Las vías en ambos estadios son las del dolor fisiológico, por exceso de nocicepción (Fig. 3).
III.- Crónico.- De 6 meses a 8 años
El paciente presenta un cuadro depresivo y angustia. Se va haciendo, por un lado, hostil hacia médico y cuidadores. Y, por otro lado, dependiente de sus tratamientos. Aunque ya experimenta fracasos terapéuticos
El paciente abandona de forma progresiva su vida normal familiar, social. Deja el trabajo.
IV.- Hipercrónico.- 3 a 12 años
El paciente aprende a convivir con el dolor, aunque no lo acepta. Deja el tratamiento, porque confirma que no tiene eficacia y da igual. Lo que le permite mejorar los efectos adversos.
El paciente va recuperando la familia, la vida social y el trabajo. Mejora de la depresión y el insomnio.
Las vías de estos dos últimos estadios son la paleo espino-talámica, sustancia reticular, con implicación del hipotálamo y el sistema límbico (Fig. 3).
B.- De acuerdo con los mecanismos implicados: NOCICEPTIVO y NEUROPÁTICO.
El primero se produce por excepto del estímulo nociceptivo en los receptores. El dolor agudo es siempre de este tipo. En teoría, no hay ninguna lesión o malfunción del complejo sistema que soporta el dolor como función fisiológica.
El segundo se debe a una lesión del sistema nervioso periférico o central, que daña la estructura dinámica y, por consiguiente, el equilibrio que sustenta el dolor como “sistema” similar al sistema extrapiramidal, de lo que hablamos anteriormente.
Una de las características principales es que las aferencias sensoriales normales están disminuidas o abolidas. Hay otras denominaciones, para definir el mismo tipo de dolor, que provocan confusión. Una de ellas es la de Dolor por Desaferentización, que define la principal característica de este tipo de dolor, que acabamos de referir. Un ejemplo paradigmático es el Miembro Doloroso Fantasma. Otra denominación es la de Dolor Central, cuando la lesión que provoca el dolor afectó a estructuras del sistema nervioso central. Como ejemplo paradigmático, el Síndrome de Dejerine o Dolor Talámico.
C.- Por la expectativa de vida: DOLOR BENIGNO y MALIGNO
Está en relación con las características de la enfermedad que lo produce. Cuando es un proceso maligno (cáncer) o benigno. Esto tiene una implicación muy importante para diseñar el mejor tratamiento. Aunque hoy día se están consiguiendo prolongadas expectativas de vida.
Para diseñar el tratamiento a un paciente determinado es muy importante encuadrarlo en el siguiente esquema clínico:
- Si el dolor es agudo o crónico
- Si el dolor es de causa benigna o maligna
- Si es de tipo nociceptivo o neuropático
DOLOR POR EXCESO DE NOCICEPCIÓN
Todos los tejidos (excepto el sistema nervioso) están inervados por nociceptores, encargados de localizar y cuantificar la intensidad de los estímulos que puedan ocasionar una lesión tisular (traumatismos, infecciones-inflamaciones, distensiones viscerales, infiltración neoplásica…). A lo que hay que añadir los termoreceptores y mecanoreceptores que, pasado un umbral, también darán señales de riesgo.
Pero, además de los estímulos físicos, los nociceptores también responden al medio químico extracelular alterado por las lesiones celulares que ocasionan estos estímulos. Sobre todo a mediadores inflamatorios (bradiquinina, histamina, serotonina…). Esto puede llegar a provocar una respuesta de las neuronas nociceptivas: a) Alodinia, que reaccionan ante estímulos por debajo del umbral del dolor; b) Hiperalgesia primaria (aumento de la sensación de dolor por encima de lo que corresponde al estímulo doloroso recibido) (Baumann, 2002).
Las principales vías nociceptivas (Fig. 3) se pueden resumir en:
VIAS ASCENDENTES
A.- Componente sensitivo-discriminativo del Dolor
- Ia.- Espino-Talámico
– Dolor-Calor
– Decusación periependimaria
– Distribución somatotópica - Ib.- Cordones Posteriores
– Tacto, vibración, discriminación,
– Propiocepción
– Distribución somatotópica - II.- Tálamo
– VPM, VPL y Po (Complejo Posterior) - III.- Córtex sensitivo primario y secundario
B.- Componente afectivo-emocional (desagradable)
- Ia.- Tracto Espino-Reticular
– Substancia reticular medular
– Láminas V-VIII
– No localiza dolor
– Actúa sobre mecanismos viscerales autonómicos - Ib.- Tracto Espino-Mesencefálico
– Substancia Gris Periacueductal
– Distribución somatotópica - Ic.- Tracto Espino-Talámico ventral
– VPL y Po (Complejo Posterior) - Id.- Sistema ascendente multisináptico
- II.- Hipotálamo
- III.- Tálamo medial IV.- Sistema límbico
VIAS DESCENDENTES
Acción moduladora, inhibidora
- Ia.- Cordones posteriores
– Córtex cerebral
– Diencéfalo - Ib.- Tracto Retículo-espinal
– Viene de la Substancia Gris Periacueductal
EJEMPLOS DE SINDROMES DE DOLOR CRONICO POR EXCESO DE NOCICEPCIÓN:
- – Dolor Lumbar. Failed Back Syndrom
– Dolor isquémico. Angina de pecho
– Coccigodinia
– Síndromes miofasciales. Fibromialgia.
– Postquirúrgico (cirugía torácica…)
– Dolor por cáncer
– ….
DOLOR NEUROPATICO
Desde el punto de vista clínico, hay un tipo de dolor crónico que no cumple los cánones del dolor por exceso de nocicepción. Que tiene tres particularidades que lo diferencian: las características del dolor, el hecho de tener un antecedente previo claramente relacionado de haber sufrido una enfermedad previa y que esta afectación previa ha incidido directamente sobre alguna de las estructuras del sistema nervioso…
Pero no hay un consenso sobre cómo denominarlo. Hay tres denominaciones más o menos consensuadas: dolor neuropático, dolor por desaferentización y dolor central.
Yezierski (2002) describe muy bien la secuencia histórica del Dolor Central. Las primeras alusiones a este tipo de dolor se recogen ya hace 200 años. A propósito del síndrome de Wallenberg (Marchet, 1811) y otras afectaciones vasculares a nivel de tronco cerebral y tálamo. Es clásico el trabajo de Dejerine, definiendo el síndrome talámico en 1906. De manera que, a partir de 1914, aparece por primera vez el término de Dolor Central (Behand, 1914; Holmes, 1919, Riddoch, 1938).
Las características del dolor son su persistencia, aparición espontánea, intermitente, lancinante, quemante, acompañado de hiperestesia, hiperalgesia, alodinia, e hiperpatía, junto con reacciones motoras y autonómicas exaltadas. Y se diferenciaban dos dianas o lesiones diferentes dentro del sistema nervioso: nervios periféricos y estructuras del SNC (médula-encéfalo). Al primero le denominaron dolor neuropático y al segundo dolor central (Bonica, 1967). De manera que, en 1994, la IASP (International Association for the Study of Pain) define el Dolor Central como el asociado a una lesión primaria o disfunción del SNC (Merskey y Bogduk, 1994).
Tasker, et al., en 1980, proponen el nombre de Dolor por Desaferentización al dolor asociado a lesión de estructuras del sistema nervioso que van desde las raíces medulares y plexos (cuadros de anestesia dolorosa, miembro fantasma doloroso, neuralgia postherpética, avulsión del plexo braquial …), a lesiones medulares y encefálicas (Tasker, 1989, 1991).
Hay autores que prefieren separar el dolor causado por lesiones del sistema nervioso periférico del dolor por lesiones del SNC (Bonica, 1991).
El resultado es que, aunque hoy predomina el concepto de dolor neuropático, la confusión o la simultaneidad con el concepto de dolor por desaferentización continúa (Steel y Burchiel, 2002).
Como síndromes específicos de dolor central están las referidas lesiones talámicas tras ictus vascular, las lesiones medulares o la Esclerosis Múltiple.
De especial interés a destacar es que, dentro de grupo de síndromes de dolor por desaferentización, están los ocasionados por las propias técnicas quirúrgicas antiálgicas (cordotomía, tractotomía mesencefálica, lesiones talámicas…).
Es imposible encontrar unanimidad, ni un nombre que diferencie y unifique los numerosos síndromes que se encuentran en el espectro del dolor no nociceptivo. Pero estos tres nombres, central, neuropático y por desaferentización siguen siendo útiles.
A diferencia del dolor por exceso de nocicepción, el dolor neuropático y el dolor central no responden a los opiáceos (Hammond, 1991). Pero tienen algún efecto los fármacos que aumentan la transmisión dopaminérgica, así como los diferentes fármacos antiepiléticos por su acción gabaérgica (clonazepan, ácido valproico…), antiglutaminérgica (lamotrigina), así como los fármacos antidepresivos (Yezierski, 2002).
Definición
Quizás el dolor neuropático se debería utilizar más en los síndromes con afectación del sistema nervioso periférico y el término de dolor central a los síndromes de afectación del SNC. Dejando el término más complejo de desaferentización como adjetivo agravante de ambos, cuando exista una clara falta de aferencias sensitivas en el territorio álgico.
EJEMPLOS DE SINDROMES DE DOLOR NEUROPATICO Y CENTRAL:
- – Neuralgia postherpética
– Avulsión de plexo braquial
– Miembro doloroso fantasma
– Distrofia simpática refleja
– Causalgia
– Lesión medular
– Síndrome talámico
– Dolor por Cáncer
– …..
OTROS SINDROMES DOLOROSOS
El dolor cráneo-facial abarca un gran número de entidades que pueden no entrar en la clasificación anterior.
Entre ellas están:
- – Cefaleas y Migrañas
– Neuralgia Esencial del Trigémino
– Neuralgia no Esencial del Trigémino
– Neuralgia Facial Atípica
– Neuralgia del Glosofaríngeo
– Neuralgia Suboccipital de Arnold
– Otras Neuralgias
– Dolor oro-facial
– …
PROCEDIMIENTOS NEUROQUIRURGICOS
INTRODUCCION
Una vez revisados los principales conceptos de fisiopatología y clínica del dolor intratable o no controlado con tratamiento médico adecuado, es importante hacer una revisión de los principales procedimientos quirúrgicos. Sus indicaciones, resultados y efectos adversos.
De forma que tengamos una idea clara de las posibilidades quirúrgicas. Así podremos tener una visión más global del tratamiento que podemos ofrecerle a un paciente determinado, desde el tratamiento médico más apropiado, pasando por las técnicas anestésicas y finalizando por los abordajes quirúrgicos.
Si tenemos esta visión global, el paciente tendrá desde el principio un plan de tratamiento escalonado y multidisciplinario.
HISTORIA DE LA NEUROCIRUGIA DEL DOLOR
Por su relevancia y frecuencia, la neuralgia del trigémino destaca en la historia del tratamiento quirúrgico del dolor.
En 1891 Victor Horsley propuso la avulsión del ganglio de Gasser para el tratamiento de la Neuralgia del Trigémino. Esta intervención fue mejorada en sus resultados por Cushing y, posteriormente, por Frazier. Este tipo de intervenciones se ha venido realizando hasta los años 70 con secciones selectivas de una o varias ramas del trigémino.
Dandy en 1925 propone la sección completa o parcial de la raíz del Trigémino, por vía suboccipital: Esta intervención se siguió realizando hasta los años 90 (Young y Wilkins, 1992). Incluso hoy día hay neurocirujanos que proponen la sección selectiva, en caso de que no se vea una clara compresión vascular.
A mediados de los años 40 Spiegel y Wycis (1947) construyen y aplican la primera gruía estereotáctica para el tratamiento de diversas afecciones del SNC, como la epilepsia, trastornos psicóticos y el dolor, mediante la lesión de diferentes dianas en el tálamo.
Edgar Moniz, en 1949, recibe el Premio Nobel por su propuesta de tratamiento de graves trastornos psicóticos, que él denominó Psicocirugía. Muy en relación con este campo están las propuestas de tratamiento del dolor incoercible mediante lesiones en diferentes dianas corticales y subcorticales (Pedrosa y Sola, 2003; Hernando, Sola, et al, 2004):
- • Spiegel y Wicis, 1947.- Talamotomía dorsomedial
• Talairach y Leksel, 1947.- Brazo anterior cápsula interna
• Scoville, 1940; Jow y Witty, 1953.- Cingulotomía anterior
• Knight, 1964.- Tractotomía subcaudada
• Kelly, 1973.- Leucotomía límbica
A nivel más inferior destacan las siguientes propuestas de procedimientos ablativos:
- • Abbe1886.- Rizotomía espinal
• Leriche, 1913.- Simpatectomía
• Martin y Spillen, 1912.- Cordotomia percutánea
• Armour, 1927.- Mielotomía
• Spiegel y Wycis 1953.- Mesencefalotomía
En cuanto a los procedimientos de neuromodulación, habría que destacar los siguientes hitos:
- • Richardson y Akil, 1977.- Estimulación substancia gris periacueductal y periventricular
• Hosobuchi y Adams, 1977.- Estimulación núcleos talámicos sensoriales
• Penn y Pasce, 1987.- Morfina intratecal
A continuación revisaremos las técnicas neuroquirúrgicas más destacables, tanto ablativas como neuromoduladoras. Con sus indicaciones, resultados y efectos adversos.
TECNICAS ABLATIVAS
No tienen gran predicamento debido a que presentan varios aspectos negativos:
- A) Morbilidad y complicaciones inherentes al procedimiento quirúrgico.
B) Generar nuevos déficits, que pueden llevar a la aparición de nuevo dolor por desaferentización.
C) Recurrencia del dolor a largo plazo en procesos dolorosos benignos (Steel y Burchiel, 2002).
En el dolor provocado por procesos malignos, que no responde a tratamiento con opiáceos, incluso intratecales, se puede plantear una actuación ablativa. Siempre considerando la expectativa de vida. De manera que los pacientes que tengan una expectativa menor de 3 meses no se deben considerar candidatos, por el alto riesgo de morbilidad-mortalidad (Loeser, 1990). En el otro extremo están los pacientes con larga expectativa de vida. Que pueden ser asimilados al dolor benigno y en los que un procedimiento ablativo puede ocasionar aparición de dolor por desaferentización hacia los dos-tres años post-tratamiento.
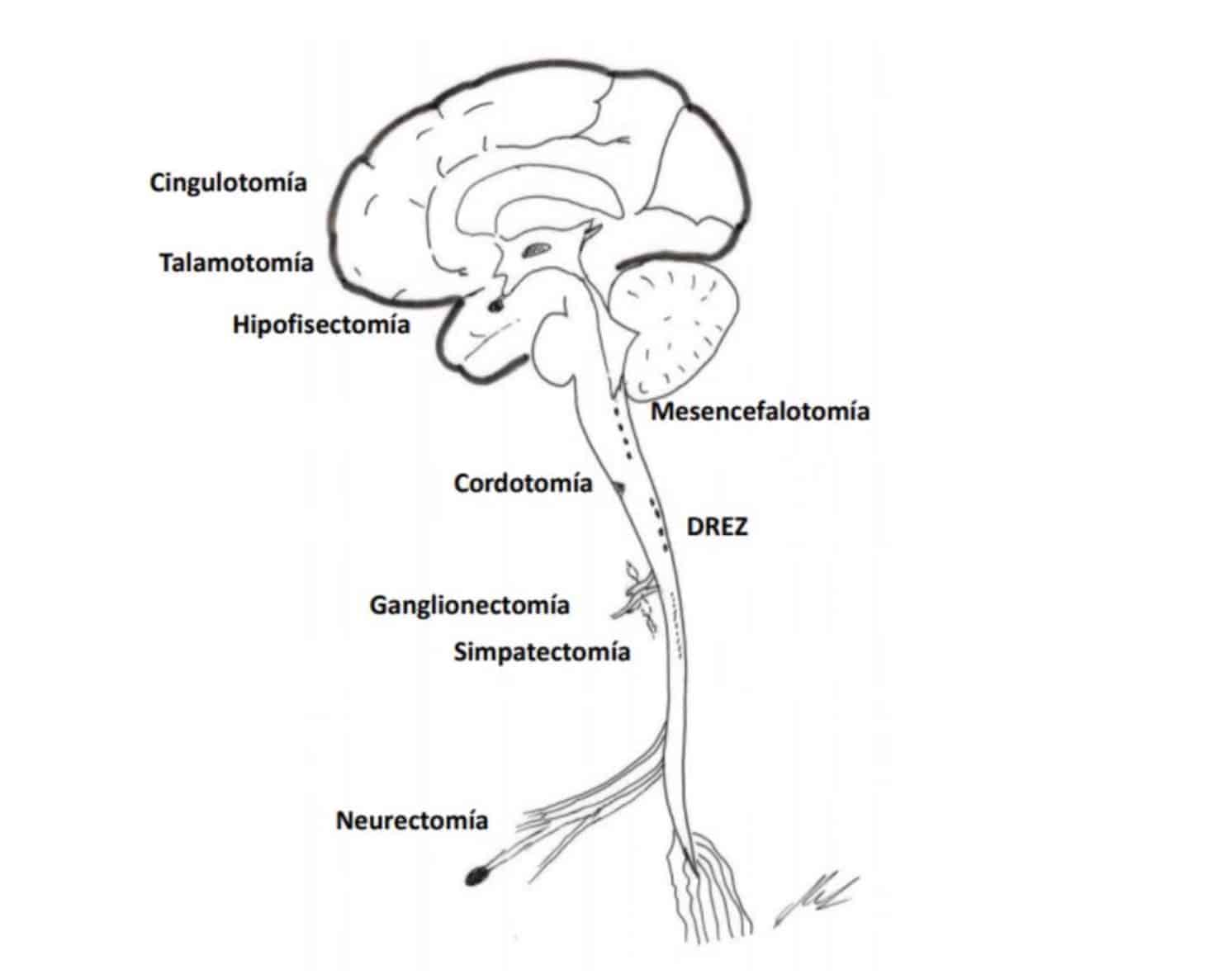
Revisamos a continuación los principales procedimientos quirúrgicos ablativos (Fig. 8):
1.- NEURECTOMÍA PERIFÉRICA.
No hay indicación actualmente para realizar este procedimiento. Provoca déficit sensitivo y motor, puede llevar a mayor dolor por desaferentización e incluso provocar un neuroma.
Otra situación es el dolor provocado por una lesión directa sobre un nervio periférico. Podría estar indicado tratar el neuroma doloroso o la liberación del nervio.
En la neuralgia suboccipital de Arnold se podría plantear esta alternativa, en casos muy seleccionados, en que se sospeche que hay atrapamiento y se pretenda solamente liberar el nervio.
2.- RIZOTOMÍA Y GANGLIONECTOMÍA.
Abbe, en 1896 propuso la sección intradural de la raíz dorsal. Scoville, en 1966 propone su sección extradural y, finalmente, Uematsu, en 1974 (1988) utiliza una técnica percutánea para realizar la rizotomía con radiofrecuencia.
Las técnicas a cielo abierto se han abandonado. Han sido sustituidas por técnicas percutáneas de lesión selectiva por radiofrecuencia.
Los mejores resultados se darían en el dolor maligno, con afectación del plexo braquial o invasión de la pared torácica, así como en la localización pélvica. En dolor crónico benigno podría ser útil en casos escogidos de neuralgia suboccipital, en fracturas torácicas y en el síndrome de espalda fallida (Taha, 2002).
Tienen los inconvenientes ya referidos de recurrencia y el riesgo de provocar a largo plazo dolor por desaferentización.
en resumen
PRINCIPALES INDICACIONES DE LA RIZOTOMIA PERCUTÁNEA
- Dolor por Cáncer (plexo braquial, pared torácica, pelvis…)
- Neuralgia suboccipital
- Síndrome de dolor lumbar postquirúrgico (failed back syndrom)
3.- SIMPATECTOMÍA
Leriche (1939), en su libro sobre el tratamiento del dolor, propone todo un cuerpo de doctrina sobre este tipo de abordaje quirúrgico. Posteriormente se han llegado a realizar las diferentes técnicas de simpatectomía de una forma menos invasiva y entran dentro del campo de las técnicas percutáneas, con indicación en cuadros como la causalgia, distrofia simpática refleja o los trastornos vasculares- isquémicos.
4.- LESIÓN EN LA ZONA DE ENTRADA DE LA RAÍZ DORSAL (DREZ)
Fue propuesta por Sindou (1972, 1995, 2002). Esta zona incluye la porción medial de la raíz dorsal, el tracto de Lisauer y las capas I a V del asta posterior (Fig. 9). Como hemos visto al comienzo de esta lección, esta zona es el primer relé del dolor, donde confluyen las actividades excitatoria e inhibitoria en la transmisión de la señal dolorosa.
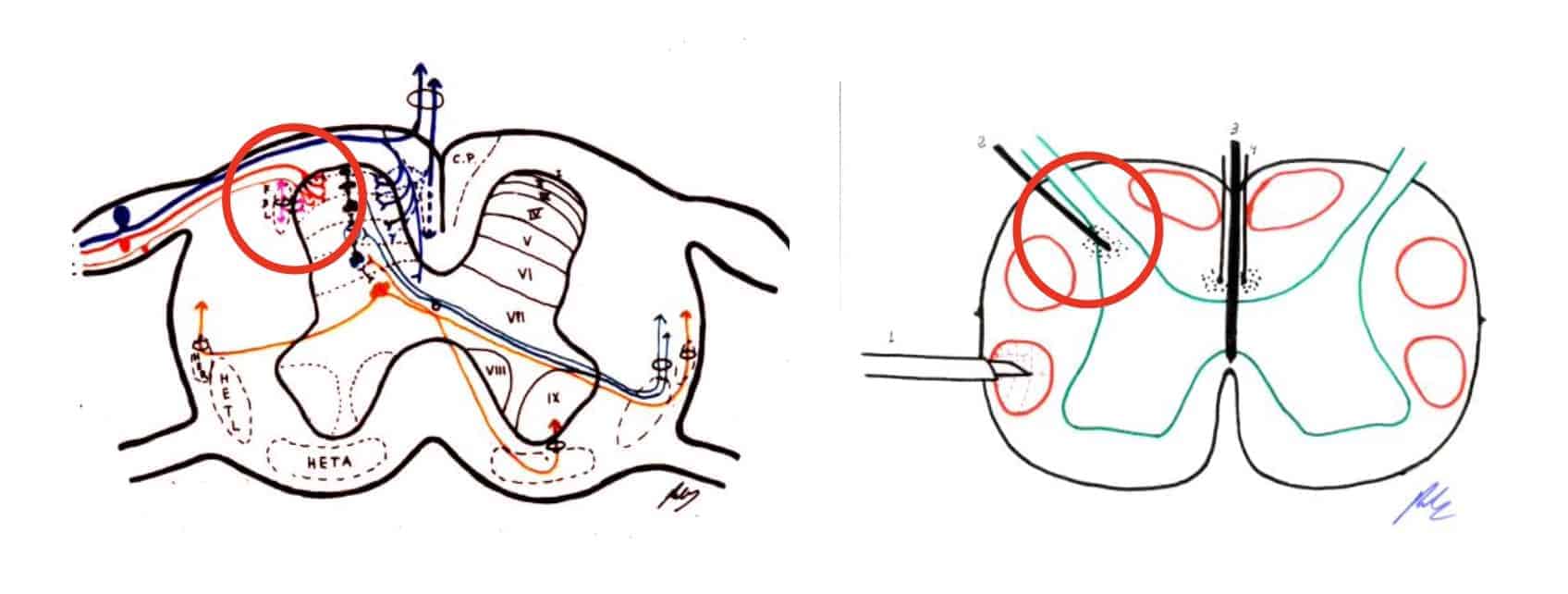
La lesión de esta zona (con microcoagulación bipolar), en patologías en las que hay una clara afectación (arrancamiento del plexo braquial, por ejemplo), puede llevar a una reestabilización de este relé.
Nashold (1976, 1979) modificó la técnica utilizando radiofrecuencia. Las principales indicaciones son la avulsión del plexo braquial, otras afectaciones del plexo (síndrome de Pancoast), lesiones medulares y lesiones de nervios periféricos (amputación, neuralgias postherpéticas).
Sindou (1994) mejora el abordaje quirúrgico, añadiendo un control neurofisiológico intraoperatorio.
Las mejores indicaciones, por sus resultados sobre el dolor y baja incidencia de morbilidad son el síndrome de Pancoast y otras invasiones bien delimitadas a nivel de la pared torácica, región perineal, plexo y raíces lumbo-sacras.
Por otra parte, éste es el único procedimiento ablativo que se puede plantear en dolores por desaferentización. Especialmente en avulsiones del plexo braquial, en lesiones medulares (con dolor claramente metamérico), causalgia por lesión de nervios periféricos y en casos muy seleccionados de neuralgia occipital e hiperespasticidad con dolor. En la neuralgia postherpética se consigue controlar la alodinia, pero permanece le sensación quemante y punzante.
en resumen
PRINCIPALES INDICACIONES DE LA LESION DEL DREZ
- Dolor por Cáncer (afectación de plexo braquial-Pancoast)
- Avulsión plexo braquial
- Lesiones medulares incompletas
- Neuralgia postherpética
5.- CORDOTOMÍA
La sección de la vía espino-talámica fue propuesta por Spiller y Martin en 1912. Posteriormente se desarrollaron técnicas percutáneas, que disminuyeron la morbilidad (Tasker, 1995).
Su indicación fundamental es en el dolor maligno, a nivel de la parte inferior del cuerpo y preferiblemente unilateral. La principal desventaja es la aparición de dolor por desaferentización hasta en un 20% de los casos, hacia los dos años después del tratamiento (Figs 10 y 11) .
La administración de mórficos ha disminuido o hecho desaparecer esta técnica, por otro lado, muy útil y que valdría la pena reponer en el armamentario neuroquirúrgico.
Pero las recientes revisiones de las series publicadas muestran su eficacia (Javed, et al.,m 2020). Todas muestran buenos resultados. Incluso se habla de aumento de eficacia de la morfina intratecal (Bentley, et al., 2014).
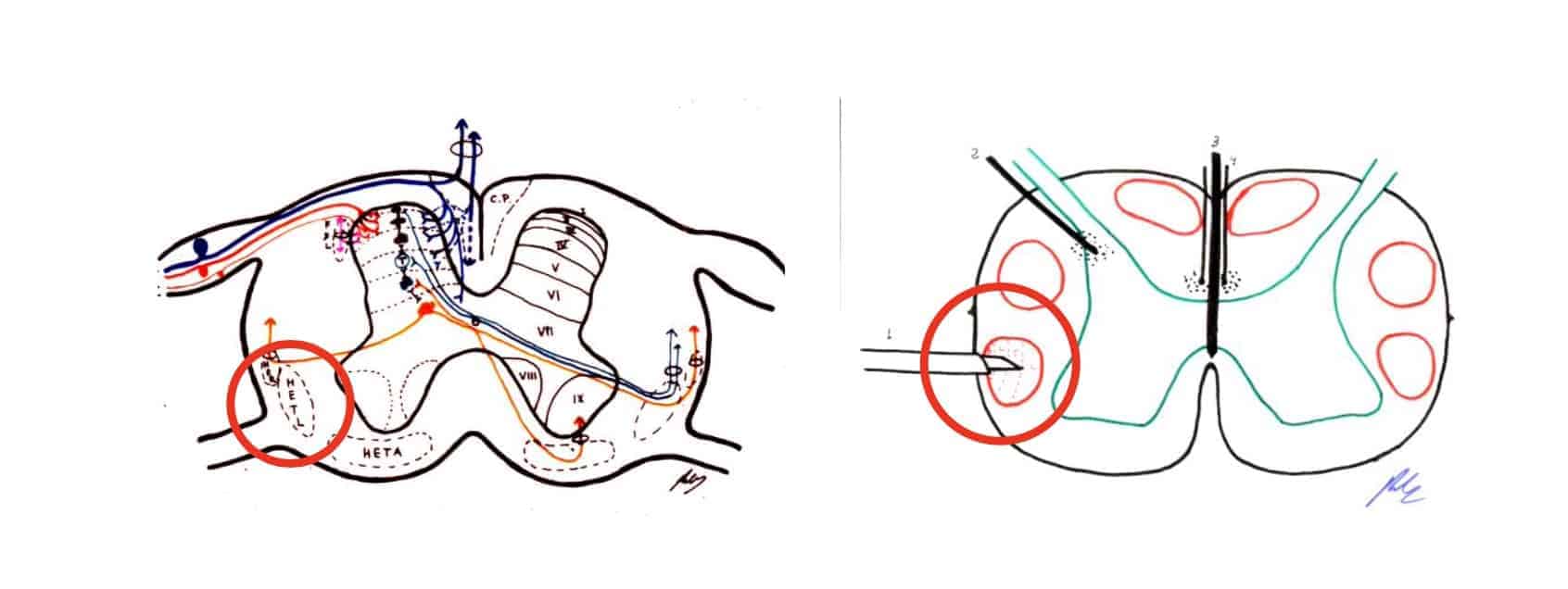
en resumen
PRINCIPALES INDICACIONES DE LA CORDOTOMIA PERCUTÁNEA
- Dolor por Cáncer. Localización unilateral baja (pelvis, extremidades inferiores
- Disminuye la dosis de mórficos<
/ul>
6.- MIELOTOMIA
A.- MIELOTOMIA COMISURAL
En dolores más centrales, la cordotomía anterolateral bilateral plantea muchos efectos adversos. Y más a nivel cervical. Por lo que una posibilidad es la realización de una incisión medial a nivel medular, para seccionar el cruce de la vía espinotalámica. Esto fue realizado por primera vez por Armour, en 1927 y por Leriche en 1928 (Leriche R. 1939).
La idea es seccionar no solamente la comisura blanca posterior, sino también la comisura blanca posterior (Sourek, 1969). Aunque tiene buen resultado frente al dolor, hay numerosos efectos colaterales, como trastornos de la marcha, trastornos de la sensibilidad profunda, por afectación de los cordones posteriores o paresias. No hay, sin embargo trastornos de esfínteres, como en la cordotomía bilateral (Adams, et al., 1982) (Fig. 12).
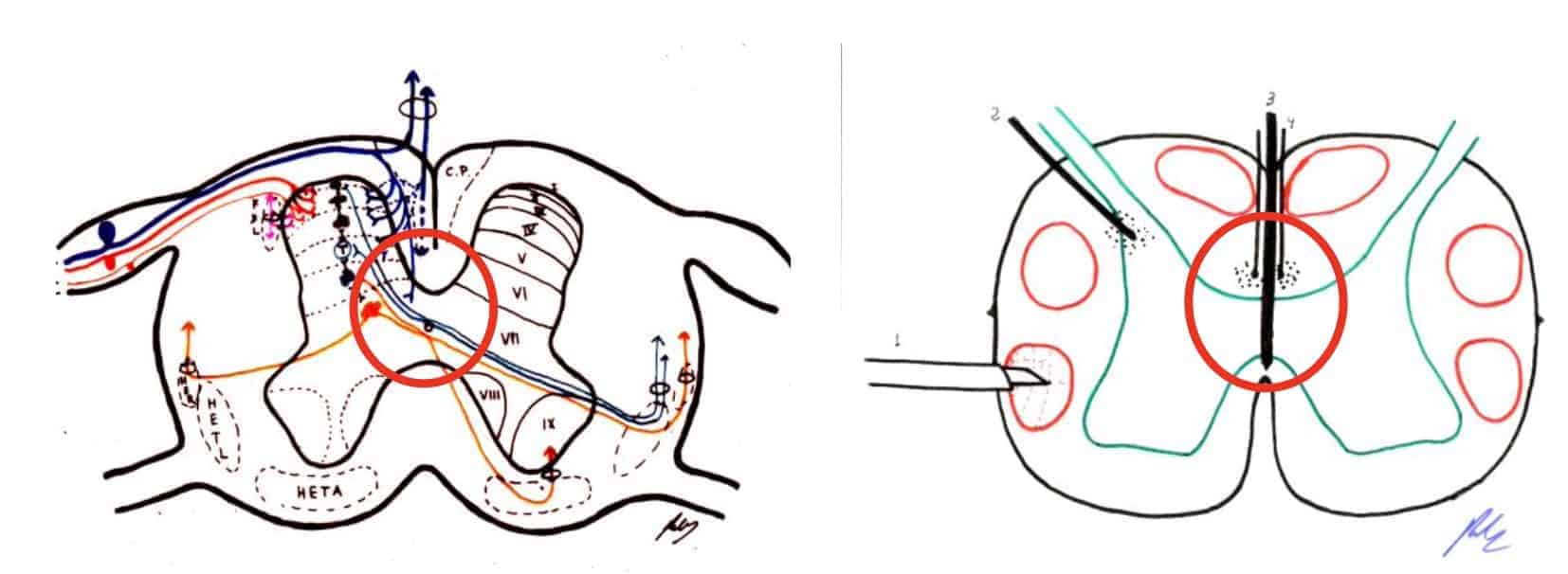
B.- MIELOTOMIA EXTRALEMNISCAL
Con el fin de controlar el dolor de localización superior, en cuello y extremidades superiores, Hitchcock (1970), propuso la realización de una lesión térmica percutánea a nivel cervical (C1), a una profundidad de 5mm de la pared posterior medular. Dada su capacidad de obtener alivio del dolor muy por debajo de la lesión, le hace proponer la hipótesis de que con esta lesión se secciona una vía multisináptica medial diferente al haz espinotalámico. Los mismos resultados positivos son publicados por Schvarcz en 1984.
Estos procedimientos han caído en desuso, por las complicaciones y por la efectividad de tratamiento con opiáceos. Pero habría que llamar la atención sobre el posible efecto beneficioso en dolores viscerales pélvicos que no respondan al dolor, dado que una mielotomía puntual a nivel torácico puede tener un buen resultado, sin efectos adversos ( Nauta, 2002) (Fig. 12).
en resumen
PRINCIPALES INDICACIONES DE LA MIELOTOMIA
- Dolor por Cáncer (afectación de pelvis bilateral)
7.- PROCEDIMIENTOS A NIVEL DEL TRONCO CEREBRAL
I.- A NIVEL DEL COMPLEJO TRIGEMINAL.
Hay 3 tipos de lesiones, muy semejantes o en continuidad:
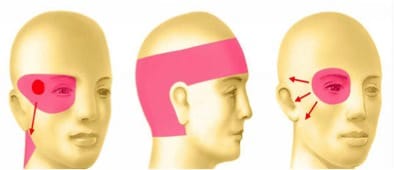
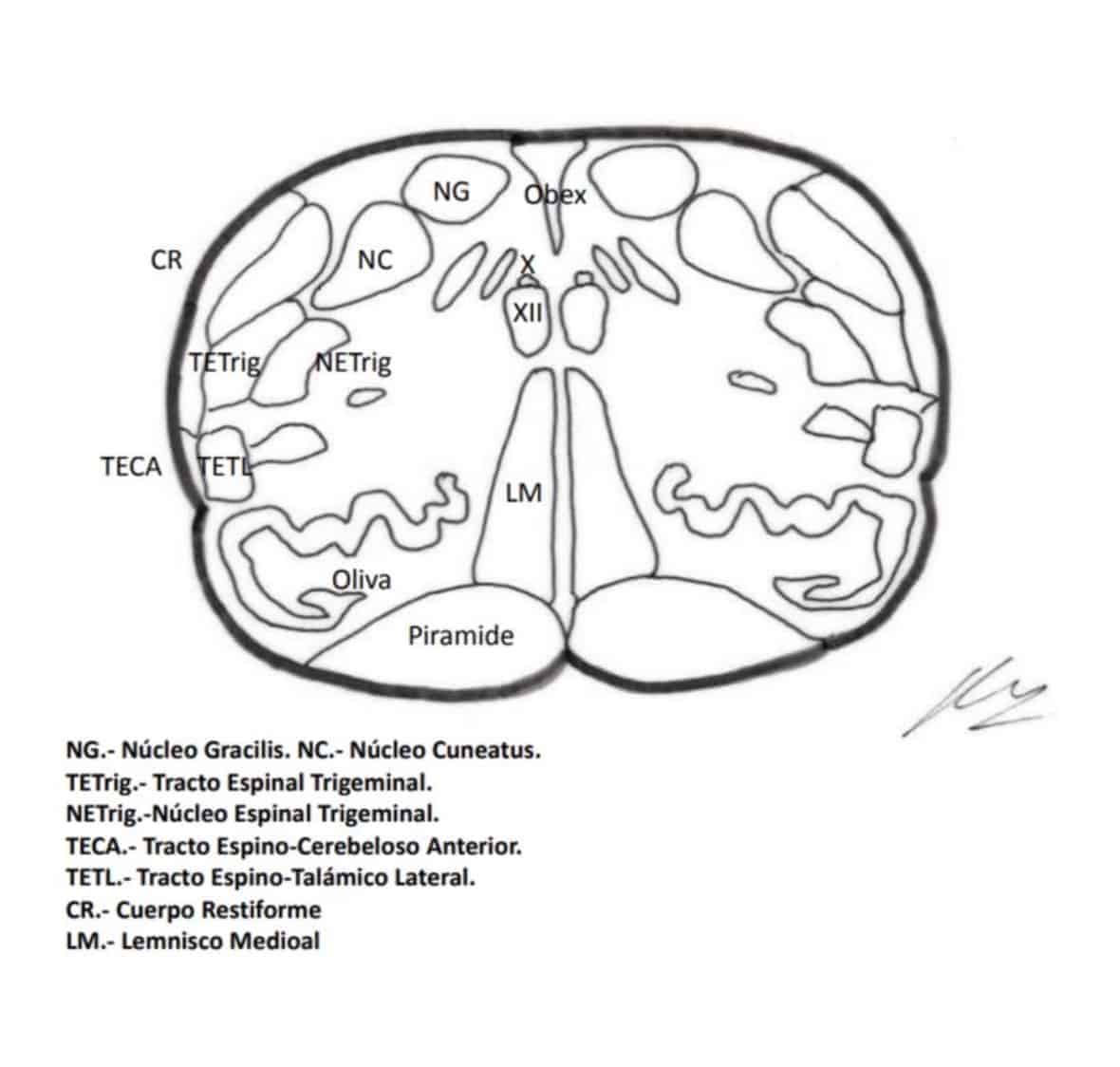
A.- Tractotomia trigeminal.- Sjöqvist propuso en 1938 seccionar el tracto trigeminal, justo antes de entrar en el núcleo caudal. Es una sección transversa, a unos 8mm por debajo del obex (Fig. 13).
El tracto trigeminal también lleva aferencias nociceptivas de los pares craneales 7, 9 y 10. Genera hipoalgesia ipsilateral en la cara, boca, pabellón auricular, parte posterior de la lengua y faringe. Hitchcock, en 1970, describe una técnica percutánea.
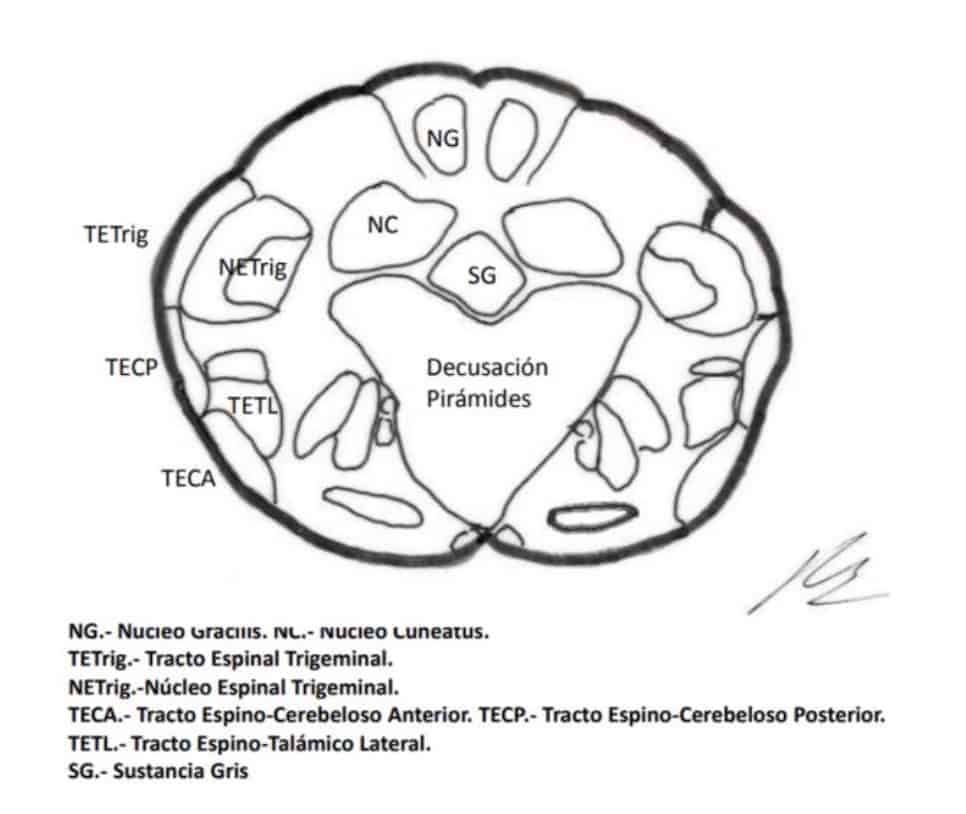
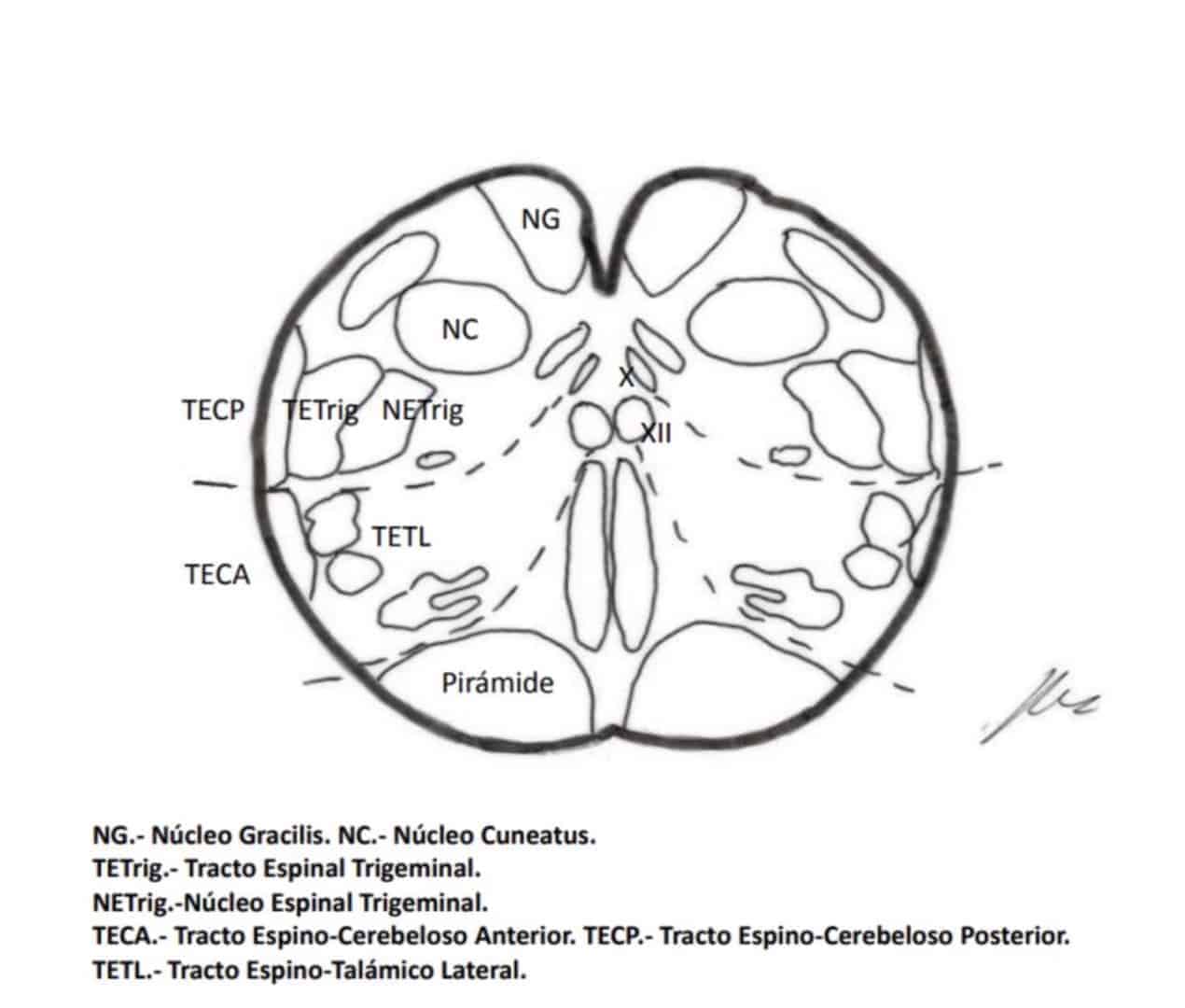
B.- Nucleotomía trigeminal.– Schvarcz, desde 1970, lesiona el polo superior del núcleo caudal. El núcleo caudal, en su porción inferior, se continúa con el asta posterior medular a nivel cervical (Fig. 14).
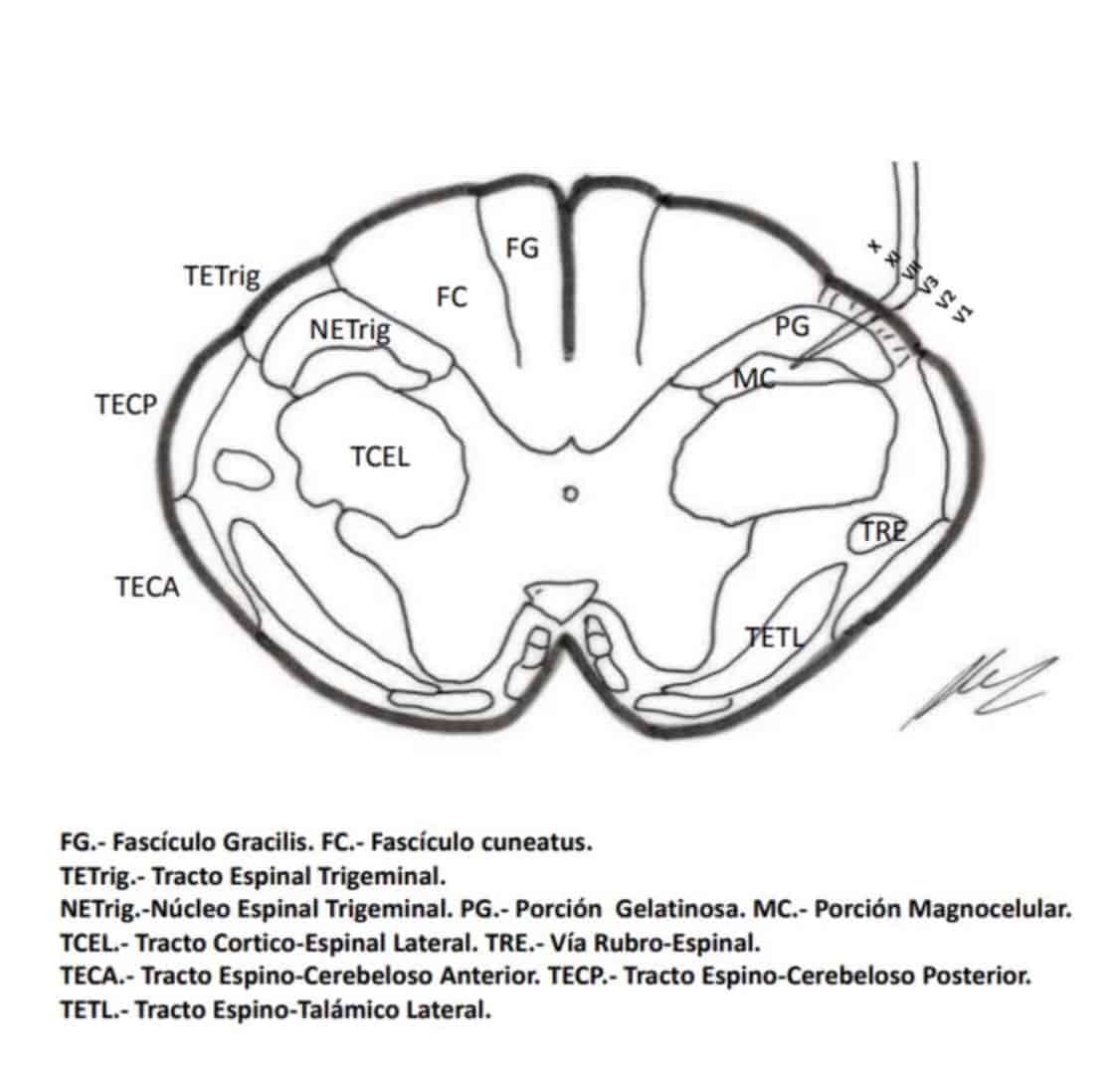
C.- DREZ del núcleo caudal.– Es la lesión de toda la sustancia gelatinosa del núcleo caudal. La propone Nashold en 1992, a cielo abierto. Supone la destrucción del núcleo desde C2 a 5mm por encima del obex (Figs. 14 y 15).
Este tipo de intervenciones se parecen mucho a la propuesta de la lesión DREZ. Estarían indicadas en el tratamiento de afecciones graves por desaferentización, como anestesia dolorosa de la cara y la neuralgia postherpética (Bernard, Nashold, et al, 1987).
Las técnicas han sido descrita en detalle por El-Naggar y Nashold en 1995 Gorecki y Rubin, en 2002.
Young (2002) comenta que, en su experiencia, este tipo de técnica debe quedar reservada solamente como último recurso y en manos experimentadas, dadas las posibilidades de complicaciones y el bajo índice de resultados excelentes sobre el dolor.
en resumen
PRINCIPALES INDICACIONES DE LA TRACTOTOMIA- NUCLEOTOMIA-DREZ TRIGEMINAL
- Dolor por Cáncer orofacial
- Dolor por desaferentización, a nivel orofacial (Anestesia dolorosa, postherpético, postquirúrgico trigeminal)
II.- MESENCEFALOTOMIA ESTEREOTACTICA
El objetivo es seccionar las aferencias en la vía espinotalámica por encima de la extremidad superior y cara. Como una cordotomía superior (Walker, 1942).
En los inicios tuvo una inaceptable morbilidad y mortalidad. Posteriormente se refinó la técnica mediante abordaje estereotáctico (Spiegel y Wycis, 1953).
Y, finalmente, mediante la lesión de la vía paleo-espino-reticular más que la vía espinotalamica (Fig. 16). Dado que la complicación más frecuente e invalidante, de importantes disestesias, se debía a la lesión del lemnisco medial próximo.
En este sentido, también Spiegel, en 1954, mostró en gatos que la estimulación de la sustancia reticular periacueductal producía respuestas emocionales al dolor.
Sugiriendo que la interrupción de la sustancia reticular extralemniscal podría ser beneficioso. Y en 1964 propuso la lesión de los núcleos mediales talámicos, donde se proyecta la vía polisináptica reticular extralemniscal.
Nashold propuso la lesión a la zona lateral de la sustancia gris periacueductal y la formación reticular medial, respetando el haz espino-talámico: mesencefalotomía extralemniscal. Con el objetivo de tratar también el componente emocional del dolor. Amano, en 1998 propone hacer la lesión algo más inferior, para evitar lesionar los núcleos óculo-motores (Figs. 16 y 17).
La principal indicación podría seguir siendo el dolor oncológico incontrolable a nivel oro-facial (Kim 2014).
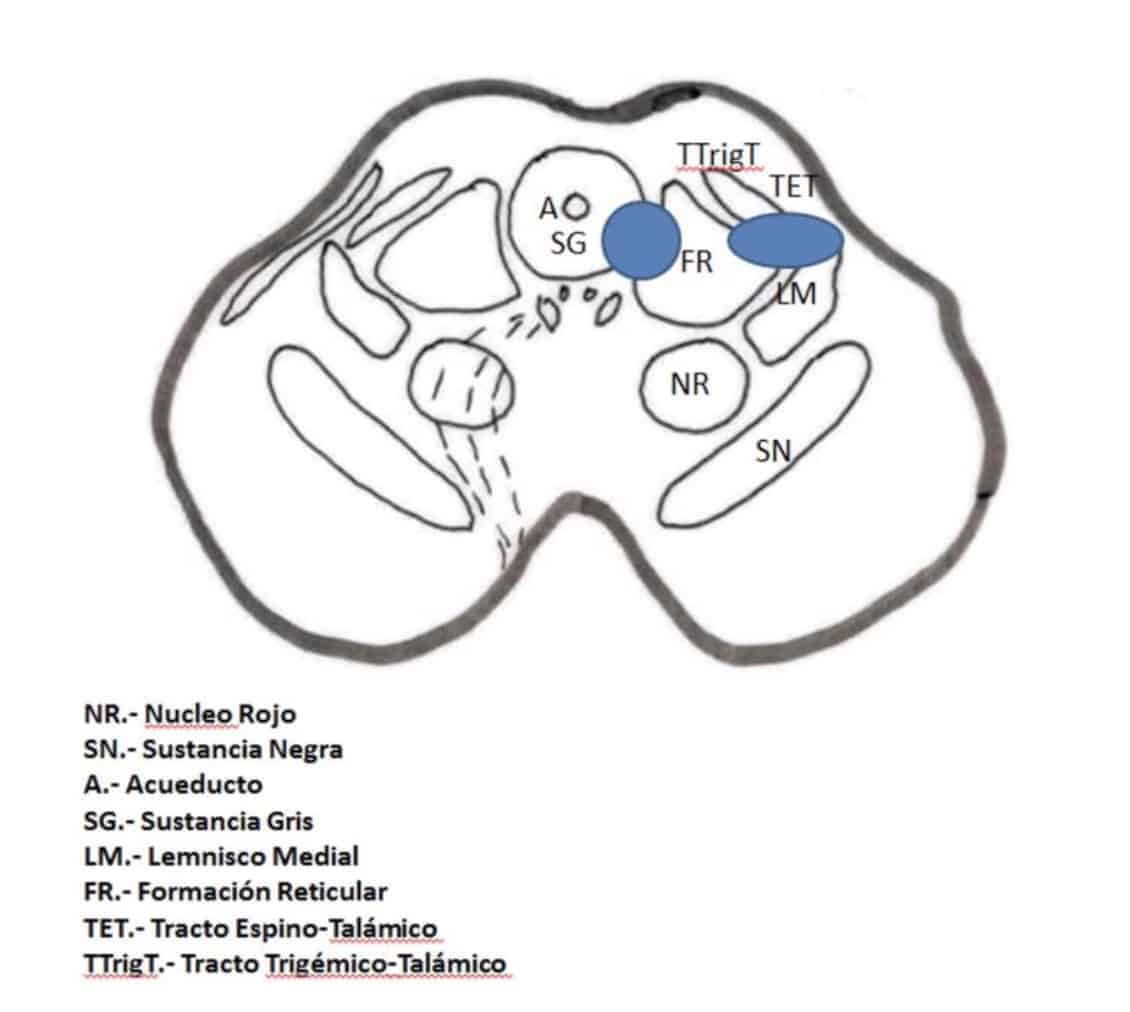
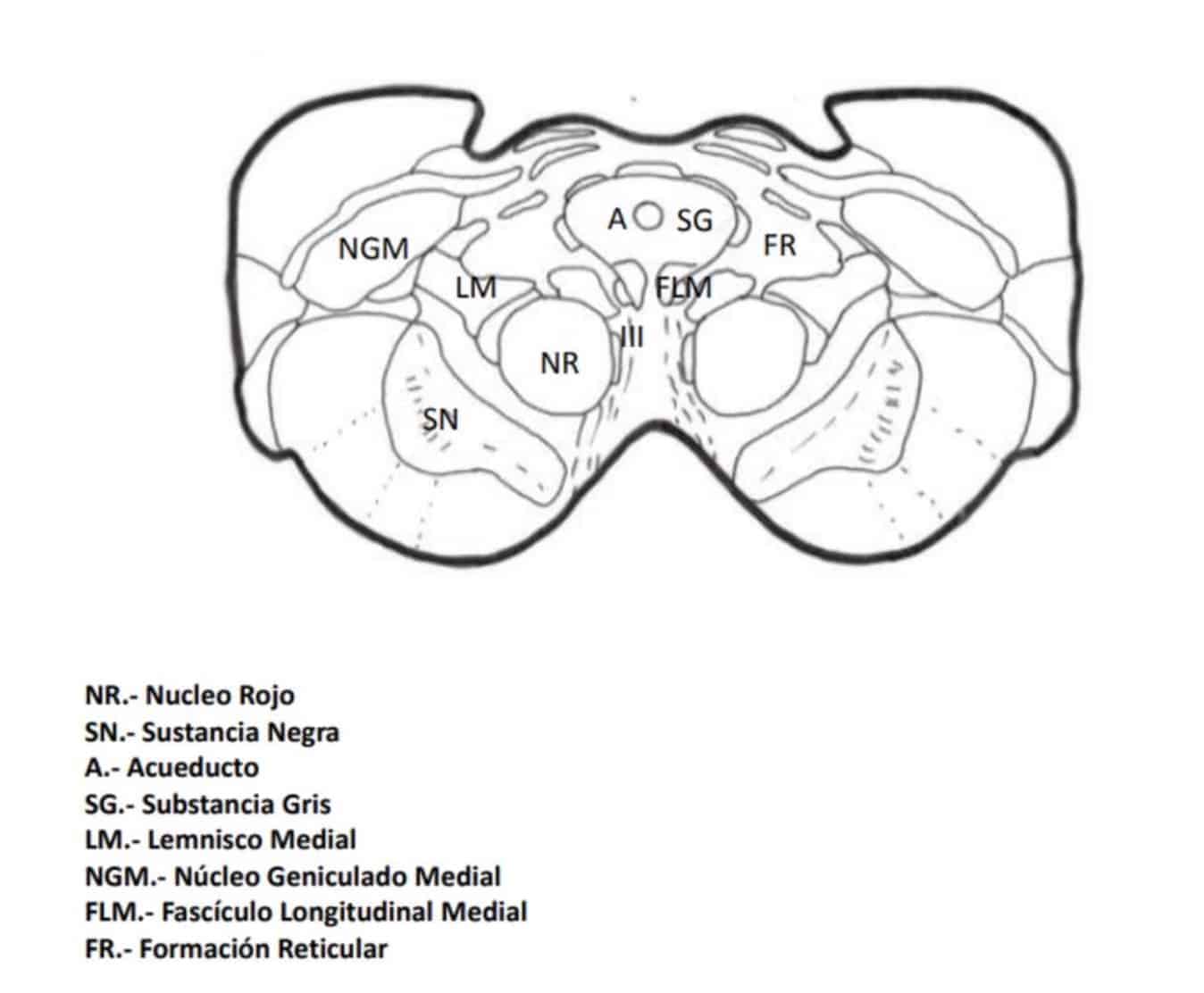
en resumen
PRINCIPALES INDICACIONES DE LA MESENCEFALOTOMIA
- Dolor por Cáncer orofacial (¿)
8.- LESIONES CORTICO-SUBCORTICALES
A.- Talamotomía medial.
Propuesta por Spiegel y Wycis en 1947. Hay autores, como Gildenberg, que la prefieren a la mesencefalotomía.
Una de las dianas propuestas es el núcleo intralaminar central-lateral (Jeanmonod et al. 2002). Y Young et al. propusieron en 1995 la utilización de la Gamma Knife para realizar la lesión (Fig. 5).
Tasker (2002) opina que esta técnica, aunque tiene menos morbilidad que la mesencefalotomía, es menos efectiva en el dolor nociceptivo.
en resumen
PRINCIPALES INDICACIONES DE LA TALAMOTOMÍA
- Dolor por Cáncer orofacial (¿)
B.- Cingulotomía
Cingulectomia significa la resección, a cielo abierto, de los 4cms. Anteriores del giro cingulado (área 24 de Brodman) (Fig 18). Probablemente interrumpe las conexiones, incluyendo el fascículo del cíngulo. Le Beau fue el primero en llevarla a cabo (1952).
La Cingulotomía significa la sección del fascículo del cíngulo, localizado por debajo del córtex cingular (Abdelaiz y Cosgrove, 2002). Tiene conexiones con el lóbulo frontal, temporal (a través del fascículo uncinado) y el sistema límbico. La primera intervención con abordaje estereotáxico fue realizado por Foltz y White (1962).
El objetivo principal es corregir también el trastorno afectivo asociado al dolor crónico (ansiedad, depresión, sufrimiento, labilidad emocional).
La cingulotomía ha de ser bilateral para conseguir los mejores resultados. Pero no tiene efecto sobre la percepción somática nociceptiva (Sweet, 1980).
En ocasiones es preciso repetir la intervención para ampliar la lesión, si el resultado fue bueno, aunque transitorio (Ballantine et al., 1995).
La cingulotomía puede ser una opción a considerar en pacientes con dolor maligno, con afectación oro-facial y componente afectivo (Viswanathan, 2013). Patel et al. (2015) proponen su realización con las nuevas tecnologías de laser y estereotaxia sin marco.
en resumen
PRINCIPALES INDICACIONES DE LA CINGULOTOMIA
- Dolor por Cáncer orofacial (¿)
- Otros dolores por cáncer, con gran componente afectivo
C.- Hipofisectomía
Fue propuesta para tratar el dolor en pacientes con metástasis múltiples (Perrault, et al., 1952). El objetivo era frenar la progresión de las metástasis al modificar el nivel hormonal (Luft y Olivecrona, 1953).
En 1995 Talairach y Tournoux proponen la hipofisectomía química o tras implantar semillas radioactivas.
A partir de los años 70 se va decantando el tratamiento del dolor como indicación de la hipofisectomía en los pacientes con metástasis diseminadas en cáncer de mama o próstata (West, et al., 1979).
El avance en el tratamiento médico del dolor ha dejado esta técnica obsoleta desde los años 80 (Polin, et al., 2002). Aunque habría que tener en cuenta la posibilidad de realizar esta técnica con éxito mediante radiocirugía (Sloan, 1996; Hassenbusch, 2002).
TECNICAS DE NEUROESTIMULACION ANALGESICA
INTRODUCCION
Este último tipo de actitud terapéutica se hace más atractivo, dado que no se produce una lesión definitiva y, por tanto, la situación nueva creada es reversible en cualquier momento. Y aunque aún no se ha conseguido, por lo general, la misma efectividad que las técnicas lesivas, los esfuerzos por mejorar los conocimientos y fundamentos fisiopatológicos de la Neuroestimulación Analgésica, así como los avances tecnológicos y sus formas de aplicación, han dado un gran impulso a una terapéutica que probablemente fue una de las primeras en aplicarse en los orígenes de la Medicina.
Los peces productores de descargas eléctricas (torpedos, anguilas, etc) eran conocidos ya por los antiguos egipcios que, al parecer, utilizaban terapéuticamente los efectos de entumecimiento que provocaba su contacto (Kellaway, 1946). Llamando la atención que el torpedo se denominara en griego νάρκη, palabra de la que se deriva el verbo ναρκάω (entumecer, adormecer) y ναρκωσις (narcosis) que ya aparece en los escritos de Hipócrates y Galeno.
Sin embargo, no se encuentra un documento escrito acerca de la utilización de las descargas eléctricas de estos tipos de peces hasta el año 46 d.JC, en que Scribonius Largus las recomienda para el tratamiento de las cefaleas y de la gota. Siendo, por tanto, la primera alusión escrita de la utilización de la neuroestimulación transcutanea para el tratamiento del dolor; refiriendo Scribonius Largus que el efecto de la descarga era lentamente progresivo y que el adormecimiento podía persistir incluso después que se interrumpiera el contacto con el pez. Este efecto entumecedor ha sido descrito a lo largo de los siglos en diferentes tratados médicos, llegándose a encontrar su aplicación en ciertas tribus primitivas (Kellaway, 1946).
Desde que William Gilger (1544-1603), médico de la corte de Inglaterra, describiera por primera vez fenómenos de imantación y creara la palabra electricidad, se tardó un siglo en inventarse la primera máquina, gracias a Otto de Guericke, capaz de producir electricidad estática por frotamiento de una esfera de azufre. Y otros 100 años más para la aparición de máquinas electrostáticas con fines médicos, realizadas por Kratzenstein y Krugger, en 1744, y Jakob Hermanna Klyn, en 1746. Richard Lovett, en 1756, publica el libro “Subtil Medium Proved”, que fue el primero sobre aplicaciones médicas de la electricidad. Aunque John Wesley, fundador del Metodismo, fue en esta época el gran defensor de la electroterapia, describiendo sus indicaciones en el libro “The Desideratum”, publicado en 1769, recogiéndose las cefaleas, ciáticas, dolor pleurítico, angina de pecho y dolor de tipo isquémico como procesos a aliviar con dicha terapia. Pero a finales del siglo XVIII decae el uso de la electricidad al no dar los resultados esperados, cayendo la electroterapia en desconsideración.
El descubrimiento de Galvani y, sobre todo, la invención de la pila eléctrica por Volta, en 1800, causan una revolución en la física y se vuelve a impulsar el desarrollo de aparatos de electromedicina. Destacando en este campo Duchenne de Bolulogne (1825), que adquiere gran experiencia y diferencia los efectos fisiológicos y aplicaciones de los diferentes tipos de corriente eléctrica. Posteriormente Hermel, en 1844, cita su experiencia en electropuntura, Sarlandiere aplica corriente eléctrica a las agujas de acupuntura y se van definiendo las indicaciones de la electroterapia, estando el tratamiento del dolor en lugar preminente (Stillings, 1975).
No obstante, de nuevo vuelve a decaer el entusiasmo y así, a principios del siglo XX, sólo destacan los intentos de hacer pasar corriente eléctrica a través del cerebro con el deseo de producir efectos narcóticos. Pero, exceptuando el tratamiento electroconvulsivo (electroshock) de Cerletti y Bini, en 1938, la electroterapia no ocupa un lugar de prestigio en la terapéutica médica durante los primeros 70 años, aunque se mantuvo su aplicación a nivel de investigación básica (Pfeiffer, 1968).
Más recientemente, la neuroestimulación volvió a tener un auge inusitado, debido con toda probabilidad a dos hechos fundamentales (Siegfried, 1977). En primer lugar, Hess (1932) en sus trabajos publicados en los años 30 llamó la atención sobre la posibilidad de producir manifestaciones motoras y emocionales mediante estimulación eléctrica cerebral. Y, en segundo lugar, en 1965 Melzach y Wall publican su teoría de la compuerta sobre el dolor que, de forma inmediata, produce las primeras aplicaciones terapéuticas. Así, Wall y Sweet, en 1967, refieren los resultados positivos de la estimulación eléctrica a nivel de los troncos nerviosos periféricos; técnica que se basa en la teoría de poder bloquear las aferencias dolorosas mediante estimulación eléctrica o táctil, que ponga en funcionamiento las fibras de conducción rápida Aβ. De forma prácticamente simultánea Shealy, en 1967, refiere casos de implantación de electrodos a nivel de cordones posteriores medulares, donde se encuentra la mayor concentración de fibras mielínicas de conducción rápida.
Tras observar que la estimulación que precedía a la lesión de los núcleos sensitivos del tálamo (VPL-VPM) producían parestesias que enmascaraban el dolor, Mazars, en 1961, menciona el efecto beneficioso mantenido, o incluso curación, obtenido tras estimular sólo durante pocos días. Reynolds, en 1969, describió el efecto analgésico de la estimulación de la sustancia gris central en la rata y, en 1973, Richardson y Akil comunican las primeras implantaciones de electrodos en el hombre, a nivel de la sustancia gris periacueductal (SGPA) y periventricular (SGPV). El descubrimiento de receptores morfínicos a nivel cerebral (Goldstein, 1976) y de péptidos endógenos con acción morfinomimética, dan una nueva dimensión a la neuroestimulación (Adams, 1976; Hosobuchi, 1977).
La neuroestimulación, neuromodulación o el término anglosajón, menos aceptado, de “neuroaugmentation”, comenzaron a aplicarse, con mayor o menor éxito, no sólo como terapéutica para determinados tipos de dolor incoercible, sino también para otros tipos de problemas como la espasticidad (Cook, 1973) o la epilepsia (Cooper, 1973).
Ciñéndonos al tratamiento del dolor, la aplicación de la estimulación eléctrica en determinadas zonas del sistema nervioso está consiguiendo resultados positivos claros. Y se van decantando sus indicaciones debido, tanto a los mayores conocimientos de neurofisiología, como a los indudables avances tecnológicos. Su futuro a medio plazo parece prometedor, en cuanto a ofrecer una alternativa no muy agresiva de modificación de la respuesta del sistema nervioso mismo ante el dolor. Pero es imposible predecir si otros tipos de terapia (farmacológica, fundamentalmente), que de igual forma están sufriendo un considerable avance, no podrán superar o modificar esta alternativa terapéutica.
De forma resumida expondremos las bases tecnológicas, técnicas de aplicación e indicaciones y resultados de los diferentes tipos de neuroestimulación. Remitiendo a los interesados en obtener una visión mas detallada a la bibliografía especializada que iremos citando en el texto.
I.- NEUROESTIMULACIÓN ELÉCTRICA TRANSCUTÁNEA (NET)
La denominación anglosajona de TENS (transcutaneous electrical nerve stimulation) (Sluka, 2009) describe el proceso de hacer pasar una corriente eléctrica a través de la piel, con la finalidad de modificar las respuestas del sistema nervioso. Dado que intenta que su efecto sea analgésico, las estructuras sobre las que pretende actuar son las fibras gruesas sensitivas de los nervios periféricos.
Hay aun cierto escepticismo acerca del uso, inocuidad y efectividad de la NET. Sin embargo, la corriente eléctrica que se genera es extremadamente segura y controlable, habiéndose sofisticado los sistemas que han pasado las pruebas exigidas por los organismos del tipo del FDA americano o la Comunidad Europea, quedando su aplicación restringida y controlada por el médico.
No es la finalidad de este capitulo describir técnicamente todas las posibilidades existentes en el mercado, sino dar algunos principios generales. Como en otros campos de la terapéutica, el mejor producto es el que mejor conozcamos; aconsejando en este caso que, por un lado, hemos de conjugar una buena información científica en cuanto a sus aplicaciones y, por otro lado, hemos de disponer de un buen soporte técnico por parte de la empresa manufacturadora de estos aparatos.
A.- Bases tecnológicas. El concepto y misión de la NET es realizar una estimulación por vía transcutanea de las fibras propioceptivas del tacto, que poseen gran velocidad de conducción, con un mínimo de respuestas de las fibras motoras aferentes. Para conseguir este objetivo se han diseñado diversos tipos de estimuladores electivos miniaturizados que constan esquemáticamente de un generador de impulsos y electrodos de contacto cutáneos.
1.-Generador de Impulsos: Es portátil, de fácil manejo para el paciente y alimentado por lo general por baterías de tipo alcalino que además de ofrecer mayor comodidad que una conexión a la red, ofrece una total seguridad eléctrica.
No existe un punto de vista estándar acerca de los parámetros de estimulación más efectivos. Ni se conoce bien el mecanismo de acción del potencial eléctrico que aplicamos y que va a provocar la aparición de un potencial evocado en las estructuras nerviosas periféricas. Como es bien sabido el potencial de reposo del exterior de la membrana de la fibra nerviosa periférica es positivo. Si aplicamos un estimulo adecuado puede sobrepasarse la capacidad de la bomba de sodio y provocar una entrada masiva de éste, lo que invertiría el potencial de membrana y generaría, siguiendo la ley del todo o nada, un potencial de acción que va a ir caminando a lo largo de la fibra nerviosa por su inercia metabólica. Este concepto es importante, en el sentido de que en la clínica, al aumentar la intensidad del estímulo eléctrico y notar el paciente una sensación más potente, no quiere decir que se haya generado un potencial de acción más intenso, sino que se provoca un potencial de acción en un número cada vez mayor de fibras nerviosas.
El estimulo eléctrico se irradia a través de la piel hasta que alcanza la estructura nerviosa, aumentando la despolarización de la membrana a nivel del electrodo negativo. Las primeras fibras que se alteran son las gruesas mielínicas de alta velocidad de conducción. Si se aumenta la intensidad de estimulación puede ponerse en marcha un potencial de acción en las fibras amielínicas de más alto umbral y velocidad de conducción más lenta que conducen sensaciones dolorosas. Esto ya es contraproducente, debiendo adaptarse por consiguiente la energía transmitida al paciente, eligiendo un estimulo adecuado para las fibras que queremos reclutar que, de acuerdo con la teoría del control de la compuerta, son las fibras gruesas mielínicas aferentes. Para esto hay varias formas:
- NET de alta frecuencia: La frecuencia de estímulos varia de 50 a 100 Hz (la más adecuada suele ser alrededor de los 80 Hz). La anchura de pulso suele ser menor de 200 microsegundos (alrededor de 60 μseg.) La amplitud de la onda, alrededor de 50-60 mA, va aumentándose en el potenciómetro hasta que el paciente comienza a sentir hormigueo o sensación tenue de corriente. La amplitud mas efectiva es el término medio entre la necesaria para el inicio de la sensación y la que provoca dolor o contractura muscular.
- La frecuencia del estimulo es de 1 a 4 Hz. La anchura de pulso es de 200-300 microsegundos y la amplitud más alta, hasta producir clara contractura muscular, dentro de los niveles de tolerancia del paciente.
Intenta poner en marcha un mecanismo similar a la acupuntura. Las sesiones son de menor duración al producirse fatiga muscular, apareciendo analgesia con mayor retraso, al parecer debido a un mecanismo de la liberación de endorfinas.
NET de estimulación intensa y breve. La frecuencia es de 150 Hz o mayor, la anchura de pulso es igual a 150 microsegundos y la amplitud se va aumentando hasta producir fasciculaciones musculares. Se efectúa en sesiones de estimulación de menos de 15 min. de forma seriada, con 2-3 min. de reposo entre ellas. Como el anterior tipo de estimulación está reservada por lo general a aplicaciones en ambientes clínicos y bajo control directo del personal sanitario.
En los tres tipos de estimulación, la onda puede adoptar una forma variable: A) Rectangular asimétrica bifásica, B) Rectangular simétrica bifásica y C) En espiga. Y pueden ser generadas de forma continua o en trenes de impulsos. No hay trabajos que claramente indiquen cual es la mejor forma de onda y administración de estímulo. Siendo recomendable utilizar estimuladores que al menos ofrezcan dos tipos de onda (A y C son los más utilizadas), porque ocasionalmente hay pacientes que cambiando el tipo de onda notan mayor alivio de su dolor. Debiendo tener en cuenta, en el ajuste del estimulo a cada paciente concreto, que mientras menor energía precisemos (menos amplitud, frecuencia y anchura de pulso) para obtener el mismo efecto beneficioso analgésico, mayor duración de éste conseguiremos y más tardarán en aparecer fenómenos de tolerancia.
Son más recomendables aquellos sistemas que son capaces de aportar una corriente de intensidad constante y no aquellos que ofrezcan un voltaje constante, ya que al ir variando la calidad del electrodo y la resistencia de la piel serian necesarios en este último caso correcciones continuas, aparte de que el paciente puede notar, de forma mas o menos bruscas, sensaciones desagradables y sufrir microquemaduras a nivel de los puntos de contacto de los electrodos.
Por lo general, la aplicación suele realizarse en sesiones de 20-30 min., varias veces al día, dependiendo de múltiples factores como tipo de dolor, localización, actividad del paciente etc.
NET de baja frecuencia.
2.- Electrodos. Su composición suele ser carbón siliconado, ofreciendo una estructura flexible con una amplia superficie de contacto (superior a 4 cm2), para evitar irritaciones de la piel. No suelen plantear problemas de alergia y es preciso aplicar un gel que haga de interfase conductora entre la piel y electrodo, no llegando la impedancia total del sistema a 800 ohmios. No obstante, se aconseja cambiarlos cada pocos meses, aunque no exista deterioro visible.
B.-Técnicas de aplicación. El obtener niveles de una adecuada estimulación analgésica en cada paciente requiere minuciosidad y perseverancia. En nuestra experiencia la colaboración del personal de enfermería con formación previa en estos problemas resultó imprescindible, siendo la única forma de poder atender un volumen importante de pacientes en régimen ambulatorio.
Los territorios a estimular pueden ser: a) A nivel de la zona dolorosa, buscando un punto gatillo que desencadene el dolor. Pudiéndonos ayudar de las tablas de Travell y Rinzler citadas por Melzak (1977). b) Eligiendo un trayecto nervioso que recoge la sensibilidad de la zona dolorosa. (Sluka, 2009). c) Seleccionando puntos de acupuntura correspondientes a las diferentes cartas (Fox, 1976).
C.- Mecanismo de acción de la NET. Existen varias teorías, que de forma resumida expondremos a continuación:
- 1.- Producción de un bloqueo periférico del estimulo doloroso, utilizando un mecanismo antidrómico (Campbell, 1973).
2.- Teoría del ¨control de la compuerta¨ de Melzach y Wall (1965).
3.- Teoría del ¨control central de la puesta en marcha¨ de Melzach y Casey, que implicaría ya una subida de la información por los cordones posteriores y puesta en marcha de un mecanismo inhibitorio central que, por vía descendente, actuaría a nivel de la entrada del estimulo doloroso en el asta posterior.
4.- Por reducción del tono simpático (Owens, 1979), cuyo efecto beneficioso sobre el dolor se sobreañadiría a los otros efectos directos sobre la transmisión nerviosa de la sensación dolorosa.
5.- Fox y Malzach (1976) sugieren que tenga un mecanismo de acción similar a la acupuntura.
D.- Indicaciones y resultados. La NET fue diseñada al principio como método para predecir el éxito o el fracaso de estimuladores implantables y pronto fue aceptada como una modalidad de tratamiento, siendo numerosos los síndromes y tipos de dolor descritos que se favorecen con su aplicación (Ebershold, 1975; Long, 1974).
Sin embargo las indicaciones de la NET llegaron a ser tan peregrinas y variadas como el perder peso, aumentar el busto, revitalización de órganos etc. Lo que hizo que perdiera categoría científica. Afortunadamente se ha conseguido recuperar gracias a que ha ido extendiendo el concepto de que es un instrumento que debe de estar sólo al alcance de personas especializadas e incluidas dentro de Unidades de Dolor hospitalarias.
Las aplicaciones son múltiples y son analizadas de forma exhaustiva por Manheimer (1987) y Carrol (1988). Aunque de forma más esquemática podríamos apuntar: a) En el dolor agudo puede, en muchos casos, sustituir y coadyuvar en la medicación, siendo útil en un 80% de los casos (Shealey, 1974). b) En los diferentes tipos de dolor crónico puede ser el primer elemento a intentar, junto con medidas de tipo psicológico y de terapia física apropiadas (Gildenberg, 1984). Por regla general la NET va a aportar un beneficio a largo plazo no mayor del 50% y solo en un 33% de los casos en que se utiliza como única terapia (Long, 1974).
Es nuestra propia impresión que, dado los resultados tan variados e incluso contradictorios de los diferentes estudios publicados, así como el diferente nivel cultural e idiosincrasia de los pacientes que podemos tratar, sólo la propia experiencia irá delimitando las aplicaciones de las indicaciones de aplicación de la NET.
II. ESTIMULACION DE NERVIOS PERIFERICOS
Fue utilizada por primera vez por Wall y Sweet (1967). Su principio de actuación es similar a la NET, excepto que se utilizan electrodos más finos, adaptados al nervio periférico, y se requiere una técnica quirúrgica para implantación tanto de los electrodos como del estimulador subcutáneo.
Con relativa rapidez se extendió su aplicación (Campbell, 1976; Sweet, 1976). Pero la fibrosis que se va produciendo provoca una perdida progresiva del efecto analgésico, precisando el aumento de la intensidad del estimulo, con riesgos de lesión nerviosa (Nielson, 1976).
Prácticamente su indicación esta restringida al dolor neuropático por lesiones traumáticas localizadas e incompletas de nervios periféricos, que responden bien a un test previo percutáneo, presentando aproximadamente un 50% de buenos resultados, sin que haya estudios randomizados (Nashold, 1979; Stanton-Hicks, 2009).
Como posibles complicaciones están la infección, la mayor dificultad quirúrgica que otras técnicas no invasivas y la posibilidad de lesión nerviosa peroperatoria o por la fibrosis posterior.
Dentro de este tipo de tratamiento, habría que tener en cuenta dos modalidades con resultados aceptables. En primer lugar, la estimulación crónica del ganglio de Gasser para los dolores faciales atípicos (Meyerson, 1980; Taub, 1997), cuyos resultados a medio plazo parecen bastantes aceptables. Estos dolores faciales atípicos, hasta esa fecha, no tenían otra alternativa de tratamiento, dado que la cirugía a nivel del trigémino (termocoagulación del ganglio de Gasser o descompresión) no obtiene claros beneficios. Aunque más recientemente pueden ser tratados mediante estimulación cortical, como veremos más adelante, con igual o mayor eficacia. Pero es un método a tener en cuenta en caso de fracaso de esta última alternativa.
En segundo lugar, merece mención la estimulación suboccipital (Fig. 19) o a nivel de las raíces C1-C3 (Fig. 20) para el tratamiento de algunos tipos de cefaleas, por su acción directa sobre la región occipital (Weiner, 2006) o sobre el tracto trigeminal (Popeney, 2003).
Las indicaciones principales estarían dentro del espectro de las cefaleas crónicas citadas en el International Headache Society ICHD II Compendium (síndromes migrañosos, cefaleas tensionales, cefaleas en racimo, neuralgias craneales), que no responden a tratamiento médico, obteniéndose hasta un 70% de buenos resultados (Weiner, 2009).
La técnica de implantación es mediante métodos mínimamente invasivo, percutáneo, insertando el electrodo a nivel de la lámina de C1. El electrodo y el generador de impulsos es similar a los de la estimulación del nervio periférico, pudiendo ser sistemas transmisor-receptor, totalmente implantables o recargables.
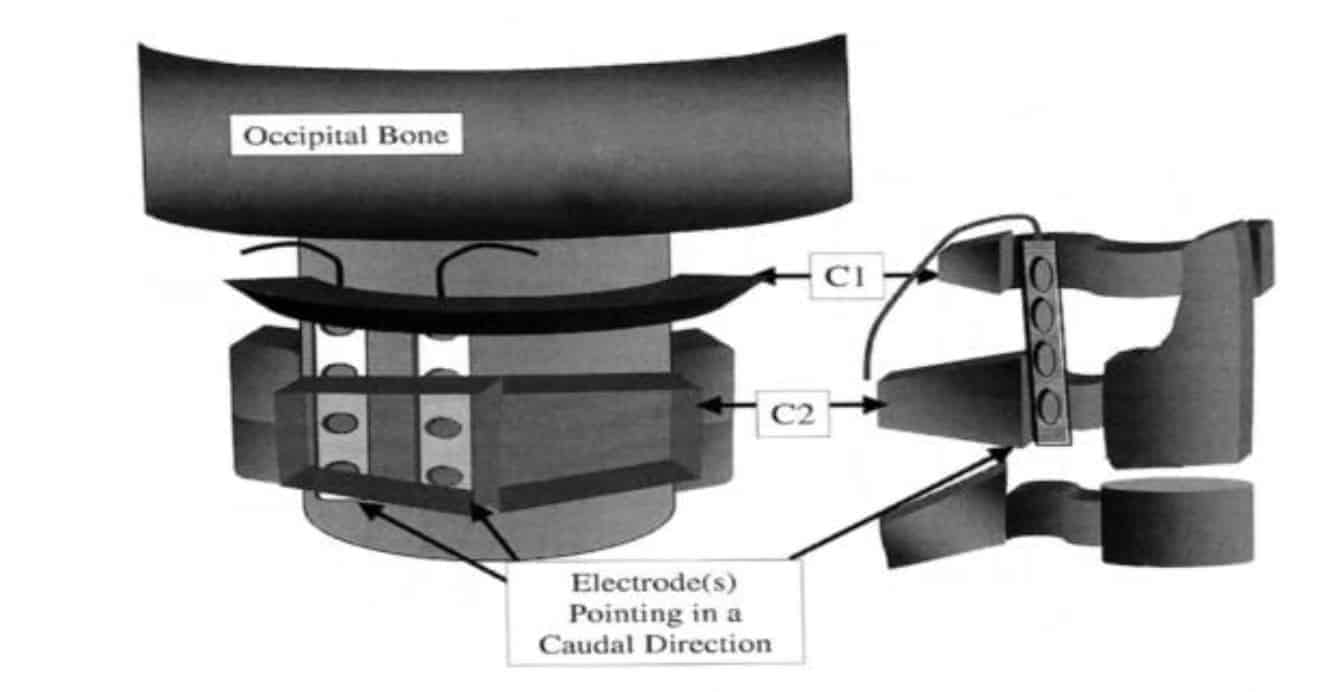
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACIÓN DE NERVIOS PERIFERICOS
- Lesiones traumáticas incompletas de nervios periféricos
- Neuralgia Facial Atípica (Ganglio de Gasser)
- Algunas Cefaleas (Suboccipital)
III. ESTIMULACION MEDULAR CRONICA ANALGESICA (EMCA)
Basadas en las teorías de Melzach y Wall (1965), Shealey et al. (1967) realizaron las primeras implantaciones de electrodos directamente sobre los cordones posteriores medulares. A continuación, debido a problemas de aracnoiditis, fístulas de LCR. y dificultades de fijación, se fue trasladando el lugar de fijación al espacio subdural (Nashold, 1972) y epidural (Sweet, 1974); precisando todas las técnicas de implantación la realización de laminectomia.
Gracias a los avances tecnológicos se mejoraron la calidad y tamaño de los electrodos, lo que hizo posible su colocación epidural mediante técnica percutánea, descrita originalmente por Dooley (1976) y rápidamente extendida.
El hecho de haber conseguido un procedimiento antiálgico de fácil colocación, prácticamente sin riesgo y que no producía alteraciones permanentes del sistema nervioso, hizo que al comienzo existiese una euforia y posterior declinar de los ánimos, al observar que los resultados a largo plazo no eran tan satisfactorios. Sin embargo, la continua mejora de los pacientes ha ido sedimentando los conocimientos e indicaciones, haciendo que en la actualidad la EMCA sea una técnica muy valida para el tratamiento de ciertos dolores incoercibles.
A. Técnicas de implantación
La implantación del sistema electrodos-estimulador es muy sencilla, aunque hemos de tener en cuenta varias fases fundamentales:
1.-Selección adecuada del paciente.- De acuerdo con las indicaciones actuales de la EMCA, que veremos porteriormente de forma concisa, sin alteraciones de la personalidad que la contraindiquen y con la clara comprensión y aceptación por parte del paciente y entorno familiar de este tipo de tratamiento.
2.-Test previo con NET.- Propuesto en 1972 por Hosobuchi et al. Tiene claras ventajas: a) En algunos pacientes puede obtenerse una clara mejoría que por el momento retrase la intervención quirúrgica o incluso la haga innecesaria. b) Acostumbrar al paciente a la nueva sensación que va a combatir su dolor, así como a manipular estos instrumentos, que para ciertas personas de bajo nivel cultural puede hacerse difícil entender. c) Por lo general, si se obtiene algún efecto beneficioso con la NET, hay un 80-90% de posibilidades de obtener efecto analgésico con la EMCA. d) Rara vez en un paciente que no pueda tolerar las parestesias de la NET o no le hacen efecto obtendremos una analgesia adecuada si se le aplica EMCA.
3.-Técnica quirúrgica. Primera fase de prueba.- La mayoría de los equipos neuroquirúrgicos o anaestésicos suelen realizar la implantación de los electrodos con técnicas percutáneas. Para esto, y dada nuestra preocupación de que a un paciente con dolor crónico no se le realicen actuaciones terapéuticas que le provoquen mas dolor, preferimos que el enfermo este ligeramente sedado, bajo la supervisión del anestesista.
La punción epidural se realiza bajo anestesia local y a nivel lumbar alto, introduciendo los electrodos con control radioscópico hasta región dorsal alta (Fig. 5). A continuación se realiza la estimulación y, según la respuesta obtenida, se movilizan los electrodos hasta lograr la aparición de parestesias en la zona dolorosa. Se fijan los electrodos al plano aponeurótico y conectamos sendos cables que tras un trayecto subcutáneo afloramos en el flanco derecho. Para más detalles técnicos ver los trabajos de Sedan y Lazorthes (1977) y Ray (1981).
A continuación se realiza, con el paciente ingresado, un periodo de estimulación de prueba. Si el enfermo no mejora, se le retiran los electrodos tras una pequeña intervención con anestesia local. En casos de excepcionales podemos permitir que el paciente vaya a su casa para que, en su entorno habitual, pruebe los efectos beneficiosos o no de la EMCA.
4.- Técnica quirúrgica. Segunda fase.- Si el resultado ha sido positivo, procedemos a internalizar el receptor y conectarlo a los electrodos. Por la misma razón expuesta anteriormente, preferimos realizar esta fase con anestesia general, evitando al paciente todo tipo de stress. El receptor queda alojado en una bolsa subcutánea, por lo general a nivel de hipocondrio derecho, quedando fuera el emisor y baterías; consiguiéndose la estimulación tras acercar la antena del emisor a la zona cutánea debajo de la cual se encuentra el receptor. Existen en el mercado otros tipos de sistemas, totalmente implantables (con baterías que pueden durar de dos a tres años, o recargables desde el exterior) y programables desde fuera; tienen un sistema de imán que al pasarlo sobre el estimulador realiza su puesta en marcha o parada. Estos sistemas, frente a las ventajas de aparente mayor sencillez, tienen varios inconvenientes:
- a) Es necesario una intervención quirúrgica para el recambio de batería, en caso de que no sea recargable.
b) El paciente ha de vivir relativamente cerca del hospital, dado que cualquier reajuste de los parámetros del estimulador ha de realizarse mediante un programador externo complejo, que sólo pueda ser manejado por personal adecuado de una unidad de dolor hospitalaria. c) Esto último supone disponer de mayor tiempo de dedicación a los pacientes en la policlínica del dolor.
En algunos centros se utilizan electrodos de 4 contactos implantables mediante laminectomía. Con respecto a la técnica percutánea (ya se disponen de electrodos percutáneos de 4 o más contactos) tiene la ventaja de que la técnica quirúrgica es más rápida, no hay exposición a los Rayos X y fácilmente se coloca bajo visión directa el electrodo en línea media posterior. Mas, como desventaja, hemos de exponer que al paciente se le realiza una laminectomía, aunque muy limitada; y si fracasa el periodo de estimulación de prueba, para retirar el electrodo es necesario una nueva intervención quirúrgica, quedándonos siempre la duda de si hubiéramos obtenido una respuesta más adecuada en otra localización. Por estas razones creemos que este tipo de intervención solo estaría justificada en aquellos pacientes en los que la estimulación es beneficiosa pero deja de serlo por movimientos de los electrodos percutáneos, impidiendo entonces implantar estos, que quedan más fijos, al nivel adecuado de los electrodos previos. O en casos en que precisemos obtener parestesias bilaterales.
B.- Parámetros de estimulación
Son similares a los descritos para la NET, aunque lógicamente con menor amplitud. Por lo general las diferentes casas comerciales van a ofrecer una presentación similar del estimulador de la NET y del EMCA por lo que al paciente no le va a ser difícil su manipulación. Aunque varía con cada paciente, por regla general aconsejamos una estimulación discontinua, en periodos de 20-30 min., varias veces al día (2 a 6 como máximo), aumentando la amplitud hasta que el paciente aprecie parestesias suaves.
C.- Mecanismos de acción de la EMCA
En resumen las bases fisiológicas de la EMCA que hoy día se admiten como más validas son las siguientes:
- 1.- Mediante un mecanismo de estimulación antidrómica de los cordones posteriores y basado en la teoría de Melzach y Wall 1965), directamente sobre las neuronas inhibidoras de la SGR o indirectamente inhibiendo las células T de la lamina V.
2.- Bloqueo de conducción de las vías espinotalámicas (Larson, 1974).
3.- Bombardeo ortodrómico del núcleo VPL talámico y posterior feed-back negativo sobre núcleos reticulares del tálamo (Bowsher, 1974).
4.- Elevación del nivel de endorfinas, por estimulación directa de las astas posteriores o por activación de centros superiores ricos en endorfinas. Estos centros, por ejemplo la SGPA, pueden utilizar una vía descendente inhibidora como la vía reticuloespinal (Basbaum, 1978) y otros sistemas serotoninérgicos (Mayer, et al., 1975).
En este sentido se ha observado que la administración de 5-L hidroxitriptófano o el mantenimiento de una dieta rica en triptófano favorece una mayor duración del efecto beneficioso y menor frecuencia de fenómenos de tolerancia en la EMCA, al igual que ocurre en la estimulación de la SGPA (Hosobuchi, 1980).
D.- Indicaciones y resultados
Es extremadamente difícil obtener una conclusión clara sobre las indicaciones y resultados de la EMCA a largo plazo. No obstante, basados en la revisión de algunos de las principales estadísticas en su primera fase de implantación (Sweeet, 1974; Sedan, 1977; Burton, 1977; Nielson, 1975), así como en experiencias más recientes referidas en la literatura (Barolat, et al., 2009; Prager, 2009), puede destacarse que es posible obtener un resultado positivo (tras una correcta selección de los pacientes) a largo plazo (más de dos años) al menos en un 40-50% de los pacientes afectados por:
- a) Dolor crónico lumbar postquirúrgico, debido a problemas complejos de aracnoepiduritis y que, por lo general, han sufrido varias intervenciones quirúrgicas sin resultado. Esta es la indicación más frecuente en la bibliografía americana (que lo denominan ¨failed back syndrome¨ o ¨low back pain syndrome¨) y supone una de las causas más frecuentes de invalidez en las personas de edad media.
b) Dolor postamputación y miembro fantasma doloroso, sobre todo en extremidades inferiores.
c) Otros dolores neuríticos (postraumáticos, diabetes…).
d) Dolor periférico por desaferentización (neuralgia postherpética, dolor postcordotomìa y avulsión del plexo braquial fundamentalmente). En estos casos las estadísticas son poco numerosas y contradictorias.
e) Dolor isquémico, aunque este problema merece mención aparte. La aplicación de EMCA en el dolor isquémico fue propuesta por primera vez por Dooley (1976) y posteriormente sistematizado y difundido por Meglio et al. (1981). Comprobándose que la EMCA no sólo produce una muy importante disminución del dolor, sino que se encontraron signos de aumento de flujo sanguíneo en las extremidades. La explicación de este aumento de flujo aún no esta clara, abogándose varios mecanismos (Broseta, et al., 1986; Linderot, et al., 2009):
- a) Activación antidrómica de las fibras C de las raíces posteriores. b) Activación de vías ascendentes hacia centros autonómicos superiores.
c) Inhibición segmentaría de las fibras vasoconstrictoras simpáticas.
Fueron los europeos los que han dado mayor impulso a esta nueva indicación (Broseta, et al., 1986; Linderot, et al., 2009). En nuestra propia experiencia el dolor isquémico es el que mejor responde a la EMCA de todos los tipos de dolor referido anteriormente. Pero dado que este dolor puede ser además un mecanismo de defensa de una extremidad con importante déficit de flujo, si tratamos una arteriopatía con gran componente obstructivo hemos de tener la precaución de que el paciente, libre del dolor con la EMCA, no incremente bruscamente su actividad física, por el riesgo a una mayor isquemia e incluso gangrena. A nuestros pacientes les hemos obligado a permanecer con la misma actividad previa durante un mes al menos y a continuación, de forma muy lenta y progresiva, han ido realizando una vida normal. Al igual que otros autores, hemos apreciado la curación de las ulceras tórpidas. Para obtener este efecto beneficioso no han precisado largos espacios de tiempo de estimulación, aconsejando el mínimo posible: de 2 a 3 sesiones diarias de 20-30 min.; de acuerdo con la capacidad analgésica obtenida.
También es nuestra impresión, al igual que refieren Cook et al. (1976) que los efectos de la EMCA son más duraderos y beneficiosos que la simpatectomia y tiene la ventaja de que no se ha realizado una lesión irreversible.
Parece que la mejor indicación de la EMCA en dolor isquémico por arteriopatia periférica es la enfermedad de Leo Burger y fenómeno de Raynaud, seguida de la arteriopatia –neuropatía diabética; y la de peor pronostico la arterioesclerosis. Una cooperación multidisciplinaría, centradas en las unidades de dolor, entre cirujanos vasculares, traumatólogos, diabetólogos y rehabilitadores, junto con el anestesista y neurocirujano, es posible que aportase un gran beneficio a este tipo de pacientes con enfermedades vasculares periféricas abocados en más o menos corto plazo a la amputación.
En otro proceso isquémico en el que hemos tenido experiencia ha sido en el angor pectoris, procediendo probablemente a las primeras implantaciones en España (Melero, Garcia de Sola, et al., 1989) (Fig. 21). Esta indicación fue propuesta por primera vez por Murphy y Giles en 1987. Está reservada a aquellos pacientes con angor inestable, que no responde a otras medidas terapéuticas. El tratamiento se ha de llevar bajo supervisión de un equipo multidisciplinario de cardiología, cardiovascular, anestesia y neurocirugía. DeJonste y Foreman (2009) exponen de manera exhaustiva las indicaciones y el manejo terapéutico.
f) Dolor maligno. El porcentaje de éxitos es muy reducido y los avances farmacológicos últimos hacen muy dudosa la indicación de la EMCA en estos casos.
Como ideas finales acerca de la EMCA, ante un paciente concreto en el que pensemos la posibilidad de aplicar esta modalidad terapéutica, nuestro consejo seria que fuera evaluado por el equipo de tratamiento del dolor, teniendo en cuenta que es una técnica prácticamente atraumática, aunque de alto coste económico y que ofrece la posibilidad de efectuar una prueba antes de internalizar todo el sistema. Si el tipo de dolor no esta incluido en los que hasta el momento ofrecen mayores garantías de éxito, con más razón aún ha de cumplir con las siguientes condiciones expuestas por Long, et al., 1981: a) Que el dolor tenga clara causa fisiológica. b) Que no existan alteraciones de la personalidad. c) Que se identifiquen, si existen, y se traten adecuadamente tanto la ansiedad como la depresión. d) Que el test previo de control del dolor mediante la aplicación de la NET sea positivo.
E.- Complicaciones
Tenemos que tener en cuenta las complicaciones, aunque es excepcional que sean graves: a) Parestesias inadecuadas en otras zonas no dolorosas, contracturas musculares, dolores radiculares, etc. Se debe a la mala colocación del electrodo o posterior emigración de este. b) Desplazamiento de electrodos e ineficacia de la estimulación, o deterioro de los elementos del sistema (la rotura del electrodo es la más frecuente). c) Infección, que obliga a retirar el sistema. d) Las propias de la laminectomia, si se realiza la implantación a cielo abierto. Es muy raro hoy en día la posibilidad de fístula de LCR o meningitis. En la actualidad, gracias al perfeccionamiento técnico y de los materiales implantables, así como a la realización de una técnica quirúrgica cuidadosa con los rigores clásicos de la asepsia y antisepsia, el riesgo global de complicaciones es inferior al 5%.
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACION MEDULAR CRONICA ANALGESICA (EMCA)
- Dolor crónico lumbar postquirúrgico
- Dolor postamputación y miembro fantasma doloroso
- Otros dolores neuríticos (postraumáticos, diabetes…)
- Dolor periférico por desaferentización
- Dolor isquémico
IV.- ESTIMULACION CEREBRAL PROFUNDA ANALGESICA (ECPA)
El efecto analgésico de la estimulación eléctrica de estructuras cerebrales subcorticales fue referido por primera vez por Heath en 1954 y por Pool en 1956. El lugar de aplicación de los electrodos fue el área septal, anterior y lateral a las columnas anteriores del fornix, apreciándose que el efecto analgésico persistía incluso varios días después de una sola sesión de estimulación. Otro punto elegido como idóneo para la estimulación analgésica fue el núcleo caudado (Ervin, et al.,1966). Estas estructuras fueron posteriormente relegadas al no obtenerse los mismos efectos beneficiosos y a largo plazo (Gol, 1967).
Sin embargo la idea de la ECPA persistió, aunque a nivel experimental, resurgiendo en los años 70. El interés de la ECPA se debió fundamentalmente a que abrió la posibilidad de tratar dolores que hasta entonces eran rebeldes a todo tipo de terapéuticas, a que se le fue encontrando un claro soporte fisiológico y, sobre todo, a que no es una técnica destructiva.
En este tiempo las localizaciones elegidas para realizar la ECPA fueron: 1) Áreas somatosensoriales subcorticales.- Lemnisco medial (Mudinger et al., 1980); núcleos sensitivos del tálamo (VPL y VPM) y el brazo posterior de la capsula interna (Adams, et al., 1974; Hosobuchi, etb al.,m 1973; Mazars, et al., 1973). Fundamentalmente indicada para el dolor por desaferentizaciòn. 2) Sustancia gris periacueductal y periventricular (SGPA y SGPV) (Richardson y Akil, 1977), indicado por lo general en el dolor por exceso de nocicepción.
1.- NUCLEOS TALAMICOS
La primera implantación de electrodos con la finalidad de realizar una ECPA fue efectuada por Mazars et al. en 1962, basándose en el hecho observado en intervenciones anteriores de que la estimulación de las fibras del lemnisco medio suprimía los dolores postherpéticos; que, por el contrario, se exacerbaban con la estimulación del fascículo espino-talámico. Este efecto analgésico se vio que era más eficaz con la estimulación del núcleo ventral posterolateral talámico (VPL).
Durante los diez primeros años Mazars (1976) dejaba electrodos en esta localización durante periodo de tiempo variables, de pocos días a dos meses como máximo, constatando que: a) La desaparición del dolor era completa y duraba varias horas e incluso días tras una sola sesión de estimulación; comenzaba a las 1-3 min. después de finalizar ésta y se prevenía la reaparición del dolor realizando dos o tres sesiones diarias de estimulación. b) La eficacia de la estimulación no se agotaba en el 20% de los casos c) El tipo de dolor que mejor respondía era el de desaferentizaciòn sin grandes zonas de afectación sensitiva.
En 1966 Adams et al., observan durante una estimulación localizadora del núcleo VPL, en el que iba a realizar una lesión, que el paciente no solo refirió las parestesias adecuadas sino también la supresión del dolor. Tras afianzar la técnica, comenzaron a realizar implantaciones de electrodos talámicos a partir de 1971. E igualmente Mazars continúa implantando electrodos de forma crónica junto con un generador de impulsos.
A.- Técnica de implantación
Hemos de tener en cuenta varios estadios en toda ECPA:
- 1.- Selección del paciente.- Lógicamente ha de tratarse de un dolor incoercible no controlable por la medicación, incluidos opiáceos a dosis altas. En el caso de estimulaciones talámicas se han de seleccionar preferentemente los pacientes con un síndrome doloroso por desaferentizaciòn aislado (por ejemplo, anestesia dolorosa) o asociado a dolor por exceso de nocicepción (por ejemplo, dolor lumbar postquirúrgico).
Para facilitar esto, Hosobuchi (1980) propuso la realización de un test de morfina, que además puede aclarar la existencia o no de tolerancia a los opiáceos. El dolor por desaferentización que no se reduce con la morfina responde mejor a la estimulación talàmica que a la estimulación de la SGPA. Y los pacientes que han desarrollado tolerancia a los opiáceos manifiestan tolerancia cruzada a los efectos analgésicos de la estimulación de la SGPA, debiendo revertir previamente la tolerancia si deseamos obtener buen resultado con la estimulación.
2.- Implantación de electrodos.- Se realiza con el enfermo despierto y con las técnicas estereotáxicas convencionales. El punto seleccionado para la estimulación del núcleo VPM (dolor facial) o el VPL (dolor en el resto del cuerpo) varía ligeramente con cada autor (Sedan y Lazorthes, 1977; Mazars, 1972; Adams, et al., 1977) y con la localización exacta de la zona dolorosa. De ahí que sea aconsejable introducir primero microelectrodos o un electrodo monopolar exploratorio que obtenga las parestesias adecuadas en la zona dolorosa; e implantar en la localización bien definida los electrodos definitivos de varios contactos de platino, efectuando una última estimulación de prueba antes de fijarlo definitivamente al orificio de trepano. A este electrodo multipolar se le conecta un cable que tras un trayecto subcutáneo aflora la piel.
Los parámetros de estimulación solían ser: Alrededor de 1-3 voltios, 50-100 Hz de frecuencia y 0,5 mseg. de amplitud de pulso. A las 24-48 h. de la intervención se procedía a realizar sesiones de estimulación bipolar en las 12 combinaciones posibles utilizando los 4 contactos, anotando los dos puntos y su polaridad en los que se obtenga el mejor efecto analgésico. De igual forma se anotaba si el paciente apreciaba mejor la analgesia con estimulación continua o en forma de rampa (la amplitud de la onda va aumentando de forma progresiva durante 20-30 seg. y cae a 0 durante 5 seg., para comenzar un nuevo ciclo a continuación). Esta forma de estimulación en rampa fue diseñada por Hosobuchi, et al (1973) y en numerosos pacientes resultó más efectiva y suponía menos energía transmitida, por lo que los fenómenos de tolerancia eran más tardíos.
Para esta fase suele ser suficiente una semana de estancia hospitalaria. Aunque en caso de duda puede permitirse el traslado del paciente a su domicilio y que realice la estimulación de prueba realizando su vida normal con las habituales medidas de higiene y asepsia.
3.- Internalización del sistema.- Si la estimulación de prueba ha sido eficaz, se anotaban los puntos de contacto y su polaridad, procediéndose bajo anestesia general a internalizar un receptor de radiofrecuencia que se conectaba a los electrodos (Sedan y Lazorthes, 1977; Hosobuchi, 1980) y que se colocaba en una bolsa subcutánea subclavicular. El paciente manipulaba el estimulador externo que, mediante una antena circular aplicada sobre la zona cutánea que cubría el receptor, transmitía la energía suficiente para generar los impulsos. Por lo general el paciente sólo tenía que manipular la amplitud aumentando hasta notar parestesias agradables en la zona dolorosa.
Los sistemas de estimulación más recientes llevan la fuente de energía incorporada, por lo que son implantables totalmente. Ultimamente con baterías recargables. Se puede poner en marcha o detener la estimulación mediante un mecanismo de on-off efectuado al pasar un imán por la zona cutánea que lo cubre. Desde fuera y mediante un dispositivo complejo es posible leer y cambiar los parámetros la estimulación (Mazars, 1960).
La estimulación se realiza habitualmente es sesiones de unos 30min. De duración varias veces al día. Para evitar fenómenos de tolerancia se recomendó (Hosobuchi, et al., 1980; Tsubokawa, et al., 1982) la administración de L-Dopa y Triptófano, precursores de la Dopamina y serotonina respectivamente, que actúan como mediadores del efecto analgésico de este tipo de estimulación.
B.- Indicaciones y resultados
La indicación principal es aquel tipo de dolor cuyo mecanismo fisiopatológico comporta un déficit sensitivo discriminativo en el que, por otra parte, están contraindicadas las intervenciones que interrumpen la vía nociceptiva, ya que aumentaríamos la desaferentización. Y otro punto importante a tener en cuenta es que, mientras mayor sea la zona con alteración de la sensibilidad, menores posibilidades de éxito tiene la estimulación talámica.
Después de una primera fase de buenos resultados obtenidos tanto por Mazars (1960, 1973, 1976) como por Adams (1977) y Hosobuchi (1980), que llegaban a referir hasta un 70-80% de éxitos (Sedan y Lazorthes, 1977), posteriormente, habiéndose valorado los pacientes más a largo plazo, se apreció que el efecto beneficioso disminuye con el tiempo.
Los mejores resultados y la serie europea más extensa de pacientes continuó siendo la de Mazars (1979). Excluyendo los dolores por exceso de nocicepción, en los que la estimulación de los núcleos VPL y VPM no obtiene resultados, y revisando sus más de un centenar de implantaciones en dolores por desaferentizaciòn, distinguía dos grupos de acuerdo con sus resultados:
- • Algias por desaferentizaciòn con extensa zona de anestesia cutánea. Se obtenían resultados positivos a largo plazo en un 50% de los casos. Se incluyen las lesiones de plexo braquial, neuralgias postherpética, dolores postrizotomia o postcordotomìa y síndrome talámico.
• Algias por desaferentizaciòn que son indicaciones de elección. Comprenden las lesiones de nervios periféricos (por heridas, aplastamiento, cirugía, radioterapia), lesiones medulares o mesencefálicas de causa vascular o por esclerosis múltiple, que produzcan un síndrome de hiperpatia-hiperestésica, y las paraplejías traumáticas.
Otros autores también han referido resultados optimistas, aunque no en tan alto porcentaje, en diferentes síndromes por desaferentizaciòn (Hosobuchi, et al., 1973; 1980; Siegfried, 1987; Dieckman, 1982). Pero es difícil, estudiando las diferentes series, obtener una conclusión acertada dado que hay numerosas variables: Localización del electrodo, tipo de dolor, tiempo de seguimiento, número escaso de pacientes, forma de valoración de los resultados, etc. La experiencia personal de Adams (Levy, et al., 1987), con un numero similar de pacientes, muestra sin embargo un resultado a largo plazo (media de 5 años de seguimiento) positivo en un 39% en los casos de síndrome talámico, disestesias postcordotomìa, anestesia dolorosa, dolor en paraplejías y dolor por neuropatía periférica. En este último tipo de dolor se incluyen los cuadros de aracnoiditis lumbar postquirúrgica (failed back síndrome), problema complejo y difícil de tratar, incapacitante y, por otro lado, de importancia creciente en nuestro tipo de sociedad. Y llama la atención que fueron los autores americanos prácticamente de forma exclusiva los que intentaron esta modalidad terapéutica con buenos resultados en general (más de la mitad de los casos, teniendo en cuenta que son pacientes seleccionados porque no se les podía plantear otra alternativa de tratamiento de su dolor). Realizando, bien la estimulación talámica sólo (Turnbull, et al., 1980) o combinada con la estimulación de la SGPA (Hosobuchi, 1986).
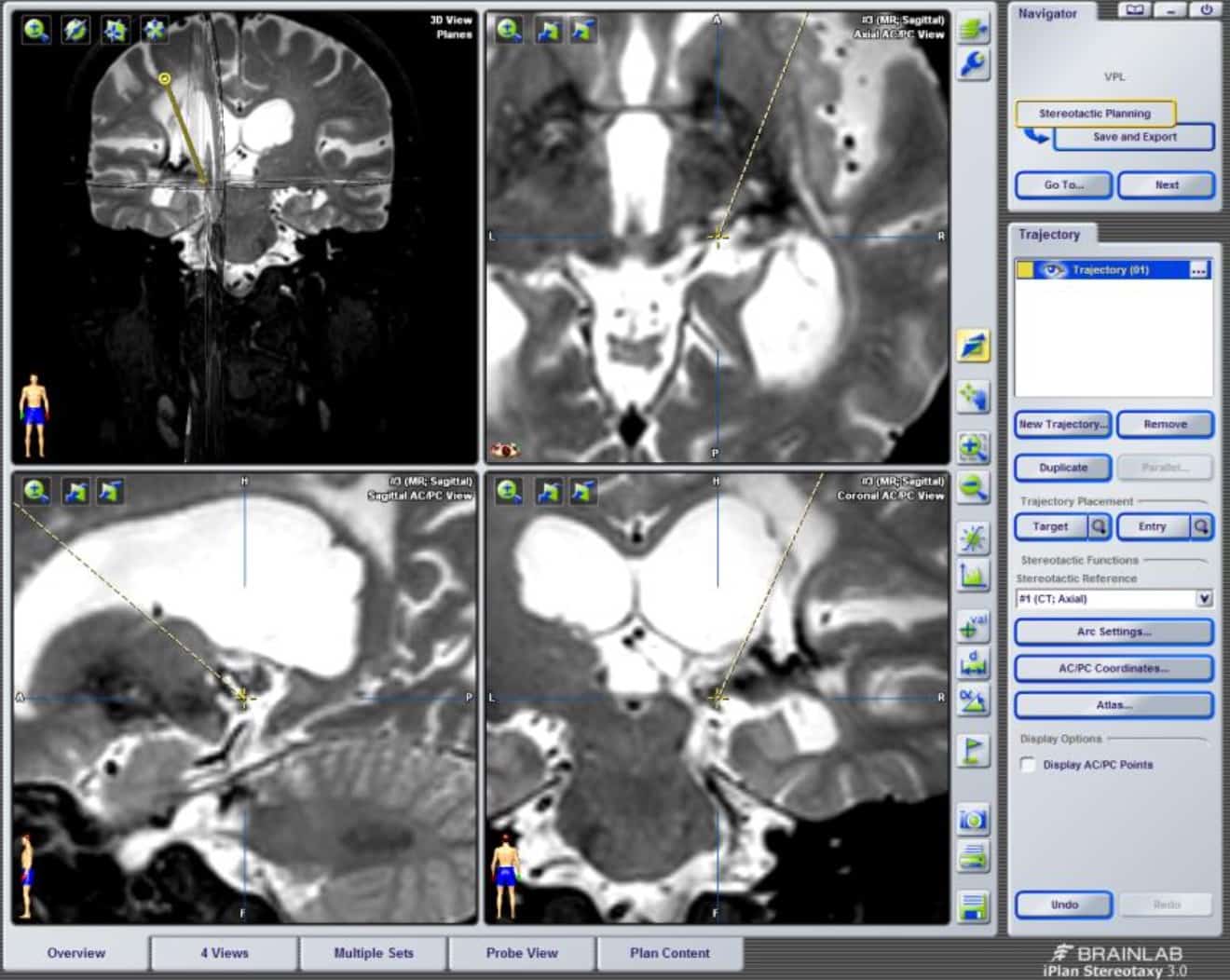
En resumen, la estimulación de los núcleos sensitivos talámicos mantiene su indicación en los casos de dolor neuropático, por desaferentizaciòn, con un resultado positivo a largo plazo que va a oscilar desde un 30 a un 50%. El dolor del síndrome talámico sólo tiene posibilidades de ser reducido si la lesión es pequeña. Y habrá que tener cada día más en cuenta la posibilidad que se abre de tratamiento del dolor incapacitante en los pacientes intervenidos a nivel de la columna lumbar, con estimulación talámica simple o combinada con la SGPA.
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACION TALAMICA (ECPA)
- Dolor crónico neuropático, por desaferentización
- Síndrome talámico
- Disestesias postcordotomìa
- Anestesia dolorosa
- Dolor en paraplejías
- Dolor por neuropatía periférica
- Failed back syndrome (¿)
2. BRAZO POSTERIOR DE LA CAPSULA INTERNA
Esta zona fue propuesta por Adams et al. (1974) tras una observación fortuita en quirófano y obtener un excelente resultado en su primer ocaso de dolor debido a lesión cortical. Su teoría fue que el refuerzo del mecanismo inhibidor cortical, que el paciente tenia afectado por su lesión a este nivel, podría ser obtenido mejor actuando a nivel de la capsula interna que supone un nivel más alto que los núcleos sensitivos talámicos.
Como en el resto de las localizaciones, al principio los resultados fueron extraordinarios, incluso el dolor talámico (Hosobuchi, 1978). Pero a largo plazo fue descendiendo su eficacia (Adams, et al.,1977; Hosobuchi, 1980).
Los resultados de Adams y Hosobuchi parecen coincidir en que la estimulación a este nivel podría ser una indicación en los siguientes casos de dolor por desaferentización: a) Disestesias postcordotomias (50% o más de resultados positivos); b) Dolor talámico (30% de éxitos); c) Lesiones de los hemisferios cerebrales que provoquen dolor, de resultados difíciles de valorar dada su rareza.
3. LEMNISCO MEDIAL
Fundamentalmente realizada por Mundinguer (1980) y Hosobuchi (1980). Su finalidad fue inducir el bloqueo tanto del sistema espinotalámico y lemniscal medial como de las vías espinoreticulares y sistema aferente que va hacia el núcleo pulvinar. Además parece que su acción esta mediada por la liberación de endorfinas.
Aunque es difícil de valorar los resultados por el escaso numero de pacientes y poco tiempo de seguimiento postquirúrgico, podría ser una indicación a tener en cuenta para la anestesia dolorosa.
4. SUBSTANCIA GRIS CENTRAL
Reynolds, en 1969, descubrió el fenómeno de analgesia producida por estimulación de la substancia gris periacueductal (SGPA) en la rata. A partir de aquí numerosas experiencias van descubriendo la existencia de una activación de un sistema descendente inhibitorio sobre las células del asta posterior medular (Mayer y Hayes, 1975), mediado por la liberación a este nivel de endorfinas (Hughes, et al., 1975).
Richardson y Akil (1977) fueron los primeros en ensayar y demostrar que la estimulación de esta zona en el hombre también produce analgesia; comprobando que, sin embargo, producía efectos colaterales no beneficiosos (alteraciones oculares fundamentalmente), por lo que cambiaron la localización del electrodo a la substancia gris periventricular (SGPA) en la parte posteromedial del tálamo, a nivel del núcleo parafascicular. La acción analgésica obtenida era bilateral, aunque con mayor efecto en el lado contralateral al electrodo. A diferencia de la estimulación talámica, no se producían parestesias con la estimulación. Mas, en ocasiones, sí se podía provocar sensación de calor o frío. Siendo los resultados a largo plazo (Richardson y Akil, 1988) muy buenos, en el sentido de disminución de mas del 50% del dolor en el 70% de los pacientes con dolor por exceso de nocicepción (fundamentalmente dolor maligno y dolor lumbar postquirúrgico) y en el 40% de los enfermos con dolores por desaferentización.
De forma casi simultánea Adams y Hosobuchi (1977) utilizan la SGPA y SGPV en un amplio número de pacientes. Pudiéndose obtener varias conclusiones analizando los resultados de ambos grupos: a) La analgesia producida recuerda la obtenida por opiáceos (Hosobuchi, 1980). b) La analgesia es revertida por la administración de naloxona (Adams, 1976; Akil, et al.,1976). c) La estimulación induce un aumento de endorfinas en LCR (Hosobuchi, 1980). d) Hay tolerancia cruzada con los opiáceos (Hosobuchi, et al., 1977). e) La analgesia está mediada por un sistema inhibidor descendente que se origina a nivel de los núcleos del rafe y que es serotoninergico (Basbaum y Fiuelds, 1978), por lo que la administración simultanea de triptófano (precursor de la serotonina) retrasa la posible aparición de fenómenos de tolerancia a la estimulación (Hosobuchi, et al., 1980).
- A. Técnica de implantación
Los estadios son similares a la estimulación talámica:
- 1. Selección del paciente.- Como en toda ECPA, hemos de tener en cuenta que es el último recurso a ofrecer a un paciente con dolor crónico. Y la selección cuidadosa ha de realizarse dentro de un equipo o unidad del dolor.
La mejor respuesta se obtiene en el dolor por exceso de nocicepción, siendo un excelente método de selección la realización de un test de morfina (Hosobuchi, 1986). Si el paciente ha desarrollado ya tolerancia a los opiáceos hay que revertir este fenómeno si deseamos que la estimulación de la SGPA obtenga buenos resultados. (Hosobuchi, 1980).
2. Implantación de electrodos. Igualmente se realiza con el paciente despierto. Para apreciar las coordinadas de los puntos seleccionados, así como la localización del electrodo aconsejamos la lectura de la bibliografía especializada (Richardson y Akil, 1977; Sedan y Lazorthes, 1977; Adams y Hosobuchi, 1977).
El electrodo puede colocarse uni o bilateralmente, aunque no necesariamente ha de ser contralateral al dolor. Hosobuchi (1986) refiere que en el lado izquierdo la analgesia es mejor. A diferencia de la estimulación talámica los parámetros son de menor amplitud de pulso (0,25 mseg.) y frecuencia (10-25 Hz.) La intensidad va aumentándose hasta que el paciente nota oscilopsia e incapacidad de iniciar movimientos oculares, reduciendo la intensidad a la mitad para la estimulación posterior.
El periodo de prueba postoperatorio así como la opción a utilizar una estimulación en forma de rampa o continua es similar a la expuesta por las otras localizaciones, al igual que la fase de internalización del sistema, si esta fase de prueba ha sido beneficiosa.
Las sesiones de estimulación han de variar de 10 a 20 min., unas tres veces al día. Hemos de tener en cuenta que a menor tiempo y menor energía transmitida mayor retraso en la aparición de fenómenos de tolerancia.
B.- Indicaciones y resultados
Aunque Richardson y Akil (1988) refirieron un 40% de buenos resultados de la estimulación de la SGPA y SGPV en el dolor por desaferentización, el número escaso de pacientes de su serie con este tipo de dolor, así como los resultados no tan favorables de otros autores (Hosobuchi, 1986) hizo que no se aconsejara la estimulación de la SGPA o SGPV en este tipo de dolor.
En relación al dolor de etiología maligna, aunque los resultados de las diferentes series no es malo (alrededor de un 50% de buenos resultados), se cuestionó su indicación, ya que los pacientes están menos motivados a proseguir la estimulación a medida que su estado general se deteriora (Meyerson, 1983) ; aparte de que los nuevos avances farmacológicos así como las técnicas anestésicas y neuroquirúrgicas alternativas están haciendo que el numero de pacientes con este tipo de dolor, que teóricamente se beneficiaria de una estimulación de la SGPA y SGPV, fuera progresivamente disminuyendo en las sucesivas estadísticas (Young y Rinaldi, 1997).
Por otro lado, en el dolor benigno por exceso de nocicepción, en el que ocupa un lugar destacado el dolor lumbar postquirúrgico (failed back syndrome), sí se obtuvieron resultados favorables con esta modalidad de ECPA. De forma que, tanto a nivel europeo (Meyerson, 1983) como en EEUU (Hosobuchi, 1980) se refieren hasta un 80% de éxitos. Aunque quizás sean más realistas los resultados de Adams (Levy, et al., 1987) de un 48% de casos favorables a largo plazo.
Se llegó a abordar este problema del dolor lumbar postquirúrgico incapacitante, en el que no aparecía ninguna alternativa de tratamiento valido, con una estimulación combinada de la SGPA/SGPV y núcleos sensitivos del tálamo, con excelentes resultados en más del 50% de los casos (Young y Rinaldi, 1997; Hosobuchi, 1983).
C.- Complicaciones
La metodología de la ECPA plantea la posibilidad de complicaciones inherentes al hecho quirúrgico de implantación de un material inerte a nivel cerebral, y que se puede resumir en (Mazards, 1976; Adams y Hosobuchi, 1977; Richardson y Akil, 1988): a) Infecciones y rechazo del material; b) neurológicas (por hemorragias o por trastornos oculares a nivel de la SGPA); c) modificación de la localización del electrodo; d) avería del sistema implantado, tanto a nivel de los electrodos como del receptor-estimulador. Siendo el porcentaje global próximo al 20% (Young y Rinaldi, 1997).
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACION SGPA-SGPV (ECPA)
- Dolor crónico maligno nociceptivo (¿)
- Failed back syndrome (¿)
5.- HIPOTALAMO
Las cefaleas en racimo (cluster headache) son cefaleas trigémino-vasculares, a nivel de 1ª rama, junto con signos vegetativos como enrojecimiento conjuntival, lagrimeo, edema parpebral, rinorrea). De varios minutos de duración. En ocasiones son muy intensas y no ceden a tratamiento médico. Plantean una situación clínica muy dramática. Una de las soluciones apuntadas, aparte de intentar tratamientos como radiofrecuencia en el ganglio de Gasser y el esfenopalatino es la estimulación hipotalámica (Molet, 2011).
Fue propuesta por Leone et al., en 2001. (2001, 2011). La localización estereotáctica se puede hacer siguiendo las indicaciones de estos autores (2010) o las de Seijo, et al., (2011).
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACION HIPOTALÁMICASGPA-SGPV (ECPA)
- Cefaleas en racimo
REFLEXIONES Y ESTADO ACTUAL DE LA ECPA
Como ha ocurrido en multitud de actitudes terapéuticas en Medicina, la neuroestimulación en sus diversas facetas nació tras la observación de un hecho fortuito beneficioso. A continuación, gracias a su aplicación más sistematizada, a la valoración de los efectos favorables y también de los errores, así como a la investigación de los fenómenos provocados, se han ido estructurando unas teorías fisiopatológicas, unas bases tecnológicas y unas indicaciones de aplicación que aun distan mucho de estar consolidadas.
Se ha expuesto el camino andado hasta finales de los años 80. Parecía igualmente un nuevo conocimiento terapéutico cargado de euforia y abocado al éxito a corto o largo plazo. Si se seguía una actitud critica y la cautela en las indicaciones y aplicaciones, se iría construyendo y ofreciendo una nueva modalidad de tratamiento muy útil para bastantes pacientes con dolor incoercible a los que, hasta ese momento, la Medicina no podía ofrecer nada excepto consuelo y recomendar paciencia.
Pero ocurrieron varios fenómenos que detuvo casi en seco la indicación y realización de este tipo de técnicas. Por un lado, el continuo avance en el tratamiento médico en las Unidades del Dolor, con técnicas menos agresivas y complejas. Por otro lado, el posible abuso en las indicaciones, junto con la aparición de múltiples series de pequeño número de pacientes, por grupos quirúrgicos llevados por la sana ambición de mejorar su capacidad terapéutica, por no pensar en otras fuerzas menos plausibles de competición profesional y duras reglas de subsistencia en el mercado económico.
De manera que los trabajos publicados mostraban tamaños muestrales insuficientes, empleo limitado y no consensuado de las escalas de seguimiento, incapacidad de localización de la lesión mediante técnicas de neuroimagen, dificultad para cegar los estudios y disponer de grupos control, seguimientos a un plazo excesivamente corto, caracterización incompleta de los pacientes incluidos en el estudio, así como de los efectos adversos que presentaban (Hernando-Requejo, García de Sola, et al, 2004).
De hecho, la ECPA no fue admitida por la FDA americana y solamente a raíz de la aceptación de ECP para el tratamiento de los movimientos anormales en 1997 se retomó esta posibilidad terapéutica (Levy, et al., 2010).
En esta segunda etapa, a partir de los años 90, habría que tener en cuenta varios hechos:
- 1.- Así como en la primera época hubo una rica aportación fisiopatológica básica simultánea a los resultados clínicos publicados, en esta segunda etapa no ha habido grandes avances en los estudios básicos fisiopatológicos que apoyen la ECPA, aunque sí en los avances clínicos, basados en la neuroimagen, que refrendan lo ya expuesto.
Así, se ha visto en estudios de PET y RM funcional que la estimulación de la SGPA-SGPV activa el tálamo medial y parte anterior del cíngulo y que la estimulación de los núcleos sensitivos del tálamo activa la amígdala, ínsula, parte anterior del cíngulo, así como la corteza sensitiva primaria y secundaria (Hamani, et al., 2009),
2.- En la implantación de electrodos intracraneales, dada la expansión producida por las indicaciones en los trastornos de movimiento, se han producido grandes avances que han modificado las técnicas quirúrgicas de colocación, así como de control intra y postoperatorio. Mejorándolo, aportando mucha más precisión y exactitud, así como disminuyendo de forma muy drástica las complicaciones quirúrgicas al hacer prescindible la ventriculografía.
Nos referimos a la utilización de programas de fusión de TAC y RM (Richardson, 2004) y de nuevos softwares en neuronavegación, que incluyen los diferentes atlas estereotáxicos (Hamani, et al., 2009). A lo que hay que sumar la mejora en la exploración neurofisiológica intraoperatoria, mediante registro previo con microelectrodos, frente a la estimulación clásica con el macroelectrodo implantable (Rezai y Lozano, 2002).
Las coordenadas de los diferentes targets se pueden consultar en los trabajos de Hamani, et al., 2009; Richardson, 2004; Rezai y Lozano, 2002; Pereira et al., 2009. El registro y estimulación con microelectrodos son muy útiles a nivel de los núcleos sensitivos del tálamo, en los que existe una distribución somatotópica, aunque no es tan útil a nivel de SGPA-SGPV (Hamani, et al., 2009).
3.- La ECPA quedó restringida durante estas dos décadas precedentes a pocos centros a nivel europeo y americano. A pesar de esto, en esta última década del pasado siglo se trataron más de 1.000 pacientes con este procedimiento (Pereira, et al., 2009).
Las indicaciones más claras, con mayor porcentaje de éxitos son: Lesión de plexo braquial y miembro fantasma, neuropatía periférica y failed back syndrome, (Hamani, et al.,m 2009; Owen, et al., 2006). El efecto positivo decae con el tiempo (Richardson, 2004).
No se obtienen resultados en las lesiones medulares (Hamani, et al., 2010), siendo mejor el tratamiento con EMCA (Pereira, et al., 2009); o en el dolor central talámico (Levy, et al., 2010), proponiendo Katayana et al. para este último la estimulación en el núcleo oval posterior (Katayama, et al., 2003).
En cuanto a la relación tipo de dolor/target a elegir, en general se acepta que el dolor nociceptivo responde mejor a la estimulación de SGPA-SGPV y el dolor neuropático a los núcleos sensitivos talámicos. Pero mientras en estos últimos hay respuesta positiva para el dolor neuropático (algo más del 50% de pacientes) y no responde el dolor nociceptivo, en la SGPA-SGPV se obtienen respuesta positiva en el dolor nociceptivo (>50% de los pacientes) y neuropático, aunque en este último el porcentaje es menor (>20% de pacientes) (Levy et al, 2010).
El dolor nociceptivo, por tanto, responde mejor que el neuropático, se consiguen mejores resultados con la estimulación en SGPA-SGPV que en los núcleos sensitivos talámicos y la asociación de estimulación en ambos targets aumenta la eficacia en dolores como el failed back syndrome (Bittar, et al., 2005). Los dolores faciales por desaferentización tienen resultados muy variables, dependiendo de los grupos quirúrgicos (Levy, et al., 2010).
V.- ESTIMULACION MOTORA CORTICAL ANALGESICA (EMCOR)
Acabamos de ver la dificultad de respuesta a la ECPA de varias entidades, todas dentro del dolor neuropático: dolor central talámico post-infarto, neuralgia facial con componente de desaferentización y lesiones medulares.
En el intento de mejorar estas opciones, Tsubokawa propone en 1991 la estimulación de la corteza motora como alternativa al tratamiento del dolor talámico, lo que es refrendado en una nueva publicación dos años más tarde. Esta respuesta positiva es confirmada por otros autores, que además amplían la indicación al dolor facial neuropático (Meyerson, et al., 1993: Nguyen et al, 1997) (Fig. 19).
Esta nueva posibilidad terapéutica estaba basada en el siguiente razonamiento (Tsubokawa, 2002): 1.- El dolor por desaferentización a nivel central es un tipo de dolor neuropático que supone una lesión completa o incompleta de la vía espino- talámica, sin lesión de la vía de los cordones posteriores-lemnisco medio. Aparece varios meses después de la lesión, se distribuye por la misma área de pérdida de sensibilidad, no responde a morfina y responde sólo en muy pocos casos a las terapias ya referidas. 2.- Se ha encontrado una hiperactividad en las neuronas de la vía sensitiva, por encima de la lesión, tanto a nivel animal (Kjerulf y Loser, 1973; Hirayama, et al., 1990) como en humanos (Lenz, et al., 1989). 3.- Esta hiperactividad puede ser reducida mediante estimulación del córtex motor (Hirayama, et al., 1990).
Su idea fue realizar esta posibilidad terapéutica mediante la colocación epidural de electrodos sobre la zona motora primaria (Area 4 de Brodman) y proceder a la estimulación crónica, similar a la EMCA o la ECPA.
1.- Técnica quirúrgica
Se recomiendan los siguientes pasos:
- A.- Selección del paciente.- Indicado en pacientes con dolor neuropático, preferiblemente talámico, en área trigeminal, periférico o tras lesión medular. Con los condicionamientos habituales de duración de la clínica dolorosa, no haber respondido a las terapias convencionales, normalidad psicológica, aceptación de la nueva terapia, sin generar falsas expectativas y, a ser posible, que respondan adecuadamente a los tests de morfina (no disminución del dolor) y barbitúricos (sí disminución del dolor) (Tsubokawa, 2002).
B.- Localización del córtex motor.- En la actualidad, gracias a los neuronavegadores, es muy fácil reconocer la circunvolución prerrolándica (Krombach et al., 1998; Brown, 2004). La zona de la cara se corresponde con el área por encima de la cisura de Sylvio y detrás de F3 (por debajo del surco frontal inferior). La zona de la extremidad superior se encuentra por encima de la cara, por detrás de F2 (entre surcos frontal superior e inferior) y la zona del tronco y extremidad inferior, inmediatamente por detrás de F1 (Nguyen et al., 2009).
Para la localización no es necesario hacer RM funcional o exploración con Magnetoencefalografía. Incluso podría llevar a error (Nuti et al., 2005; Velasco et al., 2002).
Se puede tener al paciente bajo anestesia general, sin relajantes musculares. Se localiza en el neuronavegador la zona cortical elegida y se procede a realizar una craneotomía de unos 5cms de diámetro alrededor de su punto central.
C.- Exploración neurofisiológica.- Sobre la duramadre expuesta, se coloca una manta de 16 o 20 electrodos (4×5) y se procede a realizar la localización neurofisiológica del área motora elegida mediante: 1.- Potenciales Evocados Somatosensoriales (PESS) y visualización de los electrodos donde se produce la inversión de fase de la onda N20 (Wood et al., 1998). 2.- Estimulación motora de la zona correspondiente a la onda positiva y comprobación de una buena respuesta con potenciales motores (PEMs) a bajo umbral de estimulación.
Suele haber una muy buena correlación entre la localización con el neuronavegador y los resultados de la exploración con PESS y PEMs (Nguyen et al., 2009).
D.- Colocación de electrodos.- Se colocan dos tiras de 4 electrodos, paralelas entre sí y perpendiculares a la cisura de Rolando, con 3 de sus electrodos por delante y el cuarto sobre o por detrás de dicha cisura. Sujeción de dichos electrodos a la duramadre. Se puede hacer una comprobación de su correcta localización mediante obtención de PEMs.
La duramadre debe colgarse con puntos periféricos, para evitar el hematoma epidural.
Colocación del hueso, mediante microplacas y cierre del colgajo cutáneo. Paso subcutáneo de los cables hacia el estimulador/batería, que se sitúa en una bolsa subclavicular.
E.- Estimulación.- La mayoría de los autores prefieren un período de prueba de 7-10 días, antes de implantar el estimulador (Levy, et al., 2010; Machado, et al., 2009; Rasche, 2006), dado que tiene un alto valor predictivo (Velasco et al., 2002). Habría argumentos en contra, como el hecho de que el efecto de la estimulación puede durar 24-48h., por lo que no es lógico probar diferentes posibilidades en un mismo día (Nguyen, et al., 2009), así como que la implantación definitiva en un solo acto quirúrgico reduce el riesgo de infección (Constantoyannis, 2005). La mayor experiencia y seguridad ha podido influir en que en ciertos centros (Fagundes-Pereira, et al.,m 2010; Lefaucheur, et al.,m 2009) estén prescindiendo de dicho periodo de prueba.
Inicio de la estimulación, en consulta, una vez recuperado el paciente y dado de alta hospitalaria. Se realizan los controles pertinentes, clínicos, de escalas de dolor, psicológicos, de calidad de vida, etc, de acuerdo con el protocolo de cada Unidad del Dolor. Los parámetros oscilan entre (Levy, et al., 2010): 0’5-10V, 5-130Hz y 60- 450seg de anchura de pulso. Se han descrito crisis epilépticas durante el periodo de prueba y no durante la estimulación crónica. De manera que hay autores que recomiendan tratamiento profiláctico (Tsusbokawa, 2002) y otros no.
2.- Indicaciones y resultados
De nuevo la experiencia expuesta en las diferentes series varía, aunque se encuentran datos en común.
1.- Desde el punto de vista de evidencia científica, las series tienen mejor calidad metodológica que las series de la ECPA (Hernando-Requejo, er al., 2004). Incluso en este procedimiento se puede llevar a cabo pruebas a doble ciego, ya que el paciente no nota nada durante la estimulación, pudiendo hacer on y off y registrar la respuesta clínica (Lefaucheur, et al., 2009; Velasco, 2008), encontrando un efecto placebo en el 35% de los pacientes (Rasche, 2006).
2.- Aunque es difícil compendiar todas las series, se puede decir que las mejores respuestas (hasta un 70% de pacientes con más del 50% de reducción del nivel del dolor) se dan, por este orden, en (Nguyen, et al.,m 2009; Lefaucheur, et al., 2009; Fontaine, et al., 2009): neuralgias faciales, avulsión de plexo braquial, neuropatías periféricas, lesiones medulares y dolor talámico y miembro fantasma. Hay que tener en cuenta que la eficacia va disminuyendo con el tiempo (Lima, et al., 2008; Henderson, 2004), precisando un buen conocimiento de las posibilidades de estimulación (Tanel, et al, 2011).
En el caso de lesiones talámicas, la respuesta es mejor si no hay una pérdida completa de fuerza en las extremidades contralaterales (Tsubokawa, 2002).
3.- Complicaciones
En cuanto a las complicaciones, sólo ha habido complicaciones graves en los intentos de hacer estimulación con electrodos subdurales, para abordar la zona motora de la extremidad inferior. Pero hay autores que no estiman su necesidad y abogan por la colocación epidural paramedial (Levy, et al., 2010). Ya hemos hablado de las crisis epilépticas. Las infecciones y problemas de hardware son similares a otras técnicas de neuroestimulación.
Con el fin de dar una visión general y objetiva acerca de la indicación y posibilidades de la EMCOR, hemos de tener en cuenta que los resultados están variando, entre otras razones, por la mejoría tecnológica que permite una correcta localización del área sobre la que implantar los electrodos. Pero sigue siendo una técnica que no permite reducir el dolor a cero ni a todos los pacientes. Ahora bien, al igual que la ECPA, presenta hoy día un índice muy bajo de complicaciones y un nivel superior al 60% de pacientes con excelentes o buenos resultados sobre su dolor (reducción superior al 50%, con mejora de la calidad de vida) (Lima, et al., 2008).
Ante esto, la cuestión importante sigue en pie. Dejamos sin alternativa a los pacientes con dolor incoercible, que no han tenido respuesta a todas las diferentes alternativas terapéuticas que hoy día ofrecen las modernas Unidades del Dolor?
Son pacientes con el tipo de dolor más difícil y frustrante de tratar. Nos vienen tras años de sufrir el dolor, que además está modificado por múltiples tratamientos. Incluso han sufrido complicaciones iatrogénicas que lo han empeorado. Arrastran complejos problemas de comportamiento. Pero la Neuroestimulación (ECPA o EMCOR) es su último recurso (Machado, et al., 2009).
O, mejor, nos planteamos los neurocirujanos ofrecer estas posibilidades de neuroestimulación, de muy bajo nivel de complicaciones graves y posibilidades reales de favorecer al menos al 50% de esta población de pacientes, bien seleccionados?
en resumen
PRINCIPALES INDICACIONES DE LA ESTIMULACION MOTORA CORTICAL ANALGESICA (EMCOR)
- Neuralgias faciales
- Avulsión de plexo braquial
- Neuropatías periféricas
- Lesiones medulares
- Dolor talámico
- Miembro fantasma doloroso
Abbe R. Intradural section of the spinal nerves for neuralgia. Boston Med Surg J. 1986; 135: 329-335
Abdelaiz OS y Cosgrove GR. Stereotactic Cingulotomy for the Treatment of Chronic Pain. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York.
2002812-820.:
Adams JE, Hosobuchi Y, Fields HL. Stimulation of internal capsule for relief of chronic pain. J Neurosurg. 1974, 41: 740-4.
Adams JE. Naloxone reversal of analgesia produced by stimulation in the human. Pain 1976, 2: 161-166.
Adams JE y Hosobuchi Y. Deep brain stimulation technique and technical problems. Neurosurgery 1977, 1: 196-199
Adams JE, Hosobuchi Y, Linchitz R. The present status of implantable intracranial stimulators for pain. Clinical Neurosurgery. 1977, 24: 347-361
Adams JE, Lippert R, Hosobuchi Y. Commissural Mielotomy. En: Schmidek, Sweet (Ed). Operative Neurosurgical Techniques: Indications, Methods an Results. New York: Grune & Stratton. 1982: 1155-1161.
Adrian ED. The messages in sensory nerve fibres and their interpretation. Proceedings of the Royal Society. 1931, Series B 109: 1-18
Akil H, Mayer DJ, Liebeskind JC. Antagonism of stimulation-produced analgesia by naloxone, a narcotic antagonist. Science. 1976,191: 961-962.
Akil H, Watson SJ, Barchas JD, Li CH. B-ETA-Endorphin immunoreactivity in rat and human blood: radioimmunoassay, comparative levels and physiological alterations. Life Sci. 1979, 24: 1659-65.
Albe-Fessard D. Electrophysiological methods for the identification of thalamic nuclei. Z Neurol. 1973, 205: 15-28.
Albe-Fessard D, Levante A, Lamour Y. Origin of spino-thalamic tract in monkeys. Brain Res. 1974, 65: 503-509.
Amano K. Destructive central lesions for persistent pain. En: Textbook of Stereotactic and Functional Neurosurgery. Gildenberg PL, Tasker RR (Eds).. McGraw-Hill. New York. 1998: 1425-1429.
Armour D. Surgery of the spinal cord and its membranes. Lancet 1927; 1: 691-697
Ballantine HT, Cosgrove GR, Giriunas IE. Surgical treatment of intractable psychiatric illness and chronic pain by stereotactic cingulotomy. En: Operative Neurosurgical Techniques: Indications, Methods and Results. Schmidek HH y Sweet WS (Ed).. Saunders. Philadelphia. 1995: 1423-1430.
Barolat G. Spinal cord stimulation for painful neuropathies. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 377-384
Basbaum AI, Fields HL. Endogenous pain control mechanisms: review and hypothesis. Ann Neurol. 1978, 4:451-62.
Baumann ThK. Physiologic Anatomy of Nociception. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002. Pp 2-24.
Behan RJ. Pain: Its Origin, Conduction, Perception and Diagnostic Significance. Bew York: V Appleton, 1914:198-203
Bentley JN, Viswanathan A, Rosenberg VS, Patil PG. Treatment of medically refractory cancer pain with a combination of intrathecal neuromodulation and neurosurgical ablation: case series and literature review. Pain Med. 2014;15(9):1488- 95.
Bernard J, Nashold BS, Caputi F, et al. Nucleus caudalis DREZ lesions for facial pain. Br J Neurosurg. 1987; 1: 81
Bittar RG, Kar-Purkayastha I, Owen SL, Bear R, Green A, Wang S, Aziz T. deep brain stimulation for pain relief: a meta-analysis. J Clin Neurosci 2005, 12: 515-519.
Bloom F, Segal D, Ling N, Guillemin R. Endorphins: profound behavioral effects in rats suggest new etiological factors in mental illness. Science. 1976, 194: 630-632
Bonica JJ. Management of intractable pain. En: Way EL (Ed). New Concepts in Pain and Its Clinical Management. Philadelphia, FA Davis; 1967: 155-167
Bonica JJ. Pain. Raven Press. New York.1980.
Bonica JJ. Causalgia and others reflex sympathetic dystrophies. En: Bonica JJ (Ed). The Management of Pain. Philadelphia: Lea &Febiger. 1990.
Bonica JJ. Semantic, epidemiology and educational issues of central pain. En: Casey K (Ed). Pain and Central Nervous System Disease: The Central Pain Syndromes. New York: Raven Press; 1991: 13-29.
Bowsher D. Thalamic convergence and divergence of information generated by noxious stimulation. Adv in Neurol 1974, 4. Bonica JJ (Ed). Raven Press NY. Pp 223- 232
Bowsher D. Role of the reticular formation in responses to noxious stimulation. Pain 1976, 2: 361-378
Broseta J, Barberá J, de Vera JA, Barcia-Salorio JL, Garcia-March G, González- Darder J, Rovaina F, Joanes V. Spinal cord stimulation in peripheral arterial disease. A cooperative study. J Neurosurg. 1986, 64: 71-80.
Burquiel KJ, Johans TJ, Ochoa J. The surgical treatment of painful tramatic neuromas. J Neurisurg 1993; 78: 714-718.
Burton C. Safety and clinical efficacy of spinal cord stimulation. Neurosurgery 1977, 1: 214-215
Campbell JM, Taub A. Local analgesia from percitaneous electrical stimulation. A peripheral mechanism. Arch Neurol 1973, 28: 347-350
Campbell JN, Long DM. Peripheral nerve stimulation in the treatment of intractable pain. J. Neurosurg 1976, 45: 692-699
Carroll D, Moore RA, MsQuay HJ, Fairman F, Tramer M, Leijon G. Transcutaneous electrical nerv stimulation (TENS) for chronic pain. The Cochrane Database of Systemic Reviews. 4
Cervero F, Molony V, Iggo A. Extracellular and intracellular recordings from neurones in the substantia gelatinosa Rolandi. Brain Res. 1977, 136 :565-9.
Constantoyannis C. Reducing hardware-related complications of deep stimulation. Can J Neurol Sci 2005, 32: 194-200
Cook AW, Weinstein SP. Chronic dorsal column stimulation in multiple sclerosis. NY State J Med. 1973, 73: 2868-2872.
Cook AW, Oygar A, Baggenstos P, Pacheco S, Kleriga E. Vascular disease of extremities. Electric stimulation of spinal cord and posterior roots. NY State J Med. 1976, 76: 366-368.
Cooper IS. Effect of chronic stimulation of anterior cerebellum on neurological disease. Lancet 1973, 1: 1321.
DeJonste MJL y Foreman RD. Spinal cord stimulation for refractory angina. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 831-843
Dieckmann G, Witzmann A. Initial and long-term results of deep brain stimulation for chronic intractable pain. Appl Neurophysiol. 1982, 45: 167-72.
Dooley DM. Spinal cord stimulation. AORN J 1976, 23: 1209-1212
Ebershold JC, Laws RE, Stonnington HH, Stillwell CK. Transcutaneous electrical stimulation for treatment of chronic pain. A preliminary report. Surg Neurol 1975, 4: 96-99.
El-Naggar AO y Nashold BS. Nucleus caudalis DREZ lesions for relief of intractable pain. En: Neurosurgery. Wilkins y Rengachary (Eds). 2nd ed. Mc Graw Hill Book Co. New York. 1995: 4047-4054.
Ervin FR, Brown CE, Mark VH. Striatal influence on facial pain. Confin Neurol. 1966, 27: 75-90.
Fagundes-Pereira WJ, Teixeira MJ, Reyns N, Touzet G, Dantas S, Laureau E, Blond
S. Motor cortex electric stimulation for the treatment of neuropathic pain. Arq Neuropsiquiatr 2010, 68: 923-929
Foltz EL, White LE. Pain relief by frontal cingulumootomy. J Neurosurg 1962; 19: 89- 100.
Fontaine D, Hamani C, Lozano A. Efficacy and safety of motor cortex stimulation for chronic neuropathic pain: critical review of the literature. J Neurosurg 2009, 110: 251- 256
Fox EJ, Melzack R. Transcutaneous electrical stimulation and acupuncture: comparison of treatment for low-back pain. Pain. 1976, 2: 141-148.
García de Sola, R. Neuromodulación del dolor mediante estimulación eléctrica. En: Neurocirugia Funcional y Estereotáctica. García de Sola R y García Navarrete, E (Eds.). Viguera Ed. Barcelona. 2011: 363-395.
Gildenberg PL. Management of chronic pain. Appl Neurophysiol. 1984, 47:157-70.
Gildenberg Ph L. Mesencephalotomy. En: Surgical Management of Pain. Burchiel KJ (Ed).. ThiemeNew York. 2002: 786-794.
Gol A.- Relief of pain by electrical stimulation of the septal area. J Neurol Sci 1967, 5: 115-120
Goldtein A. Opioid peptides (endorphins) in pituitary and brain. Science 1976, 193: 1081-1086
Gorecki JP y Rubin LL. Caudalis Dorsal Root Entry Zone, Nucleotomy and Tractotomy. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 763-785.
Guillemin R. The expanding significance of hypothalamic peptides, or, is endocrinology a branch of neuroendocrinology? Recent Prog Horm Res. 1976, 33: 1- 28.
Haines, D.E. Neuroanatom,y. An Atlas of Structures, Sections and Systems. 6ª Ed. Lippincott Williams & Wilkins. Philadelphia. 2004.
Hamani C, Fontaine D, Lozano A. BBS for persistent non-cancer pain. En: Textbook of Stereotactic and Functional Neurosurgery. Lozano A, Gildenberg PhL, Tasker RR. Springer. 2ªEd. 2009. pp. 2227-2238.
Hamani C, Schwalb JM, Rezai AR, Dostrovsky AR, Davis KD, Lozano AM. Deep brain stimulation fo chronic neuropathic pain: long-term outcome and the incidence of insertional effect. Pain 125, 1-2: 188-196.
Hammond DL. Do opioids relieve central pain?. En: Casey KL (Ed). Pain and the Central Nervous System Disease: the Central Pain Syndromes. New York: Raven; 1991: 233-241.
Hassenbuch SJ. Comentario al capítulo: Hypophysectomy for Intractable Pain from Metastatis Carcinoma: a Historical Perspective. Polin RS, Laws ER, Shaffrey ME. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 826-827.
Hassler R, Riechert T. [Clinical and anatomical findings in stereotactic pain operations on the thalamus]. Arch Psychiatr Nervenkr Z Gesamte Neurol Psychiatr. 1959, 200: 93-122.
Headache Classification Committee of the International Headache Society. The International Classification of Headache Disorders (2nd Ed). Cephalalgia 2004, 24, Suppl 1: 1-160
Heath R. Studies in Schizophrenia: A Multidisciplinary Approach to Mind-Brain Relationship. Cambridge, MA: Harvard University Press. 1954.
Henderson JM…..Recovery of pai control by intensive reprogramming after loss of benefit from motor cortex stimulation for neuropathic pain. Stereot Funct Neurosurg 2004, 82: 207-213
Hendler NH. The Four Stages of Pain. En: Diagnosis and Treatment of Chronic Pain Hendler NH, Long DL, Wise Th N (Eds). John Wright PSG Inc. Boston. 1982: 1-8
Hernando-Requejo V, Pastor J, García-Camba E, Sola RG. Psicocirugía y tratamiento neuroquirúrgico del dolor: revisión sistemática de la experiencia alcanzada en este tipo de tratamiento. Rev Neurol. 2004;16-31;38(10):949-56.
Hess WR. Beiträge zur Physiologie des Hirnstammes. Georg Thieme. Leipzig. 1932
Hillman P y Wall PD. Inhibitory and excitatory factors controlling lamina 5 cells. Experimental Brain Research 1969, 9: 284-206.
Hirayama T, Tsubokawa T, Katayama Y. Chronic change in activity of thalamic relay neurons following spinothalamic tractotomy in cat: effect of motor cortex stimulation. Pain 1990, 5 (Suppl): 273
Hitchcock ER. Stereotactic cervical myelotomy. J Neurol Neurosurg Psychiatrry. 1970; 33: 224-230.
Hitchcock ER. Stereotactic trigeminal tractotomy. Ann Clin Rers 1970; 2:131-135.
Hitchcock ER y Schvarcz JR. Stereotaxic trigeminal tractotomy for postherpetic facial pain. J Neurosurg 1972; 37: 412-417.
Hitchcock ER. Stereotactic spinal surgery. Neurol Surg. 1977; 433: 271-280.
Hökfelt T, Kellerth JO, Nilsson G, Pernow B. Substance p: localization in the central nervous system and in some primary sensory neurons. Science. 1975, 190: 889-90.
Holmes G. Pain of Central Origin. En: Osles W (Ed). Contributions to Medical and Biological Research. New TYork: Paul B Hoeber; 1919:235-246.
Hosobuchi Y, Adams JE, Weinstein PR. Preliminary percutaneous dorsal column stimulation prior to permanent implantation. Technical note. J Neurosurg 1972, 37: 242-245
Hosobuchi Y, Adams JE, Rutkin B. Chronic thalamic stimulation for the control of facial anesthesia dolorosa. Arch Neurol 1973, 29: 158-161
Hosobuchi Y, Adams JE, Linchitz R. Pain relief by electrical stimulation of the central grey matter in humans and its reversal by naloxone. Science 1977, 197: 183-186.
Hosobuchi Y. Chronic brain stimulation for the treatment of intractable pain. Res Clin Stud Headache. 1978, 5: 122-6.
Hosobuchi Y, Lamb S, Baskin D. Tryptophan loading may reverse tolerance to opiate analgesics in humans: a preliminary report. Pain. 1980, 9: 161-169.
Hosobuchi Y. The current status of analgesic brain stimulation. Acta Neurochir Suppl (Wien). 1980, 30: 219-27.
Hosobuchi Y. Combined electrical stimulation of the periaqueductal gray matter and sensory thalamus. Appl Neurophysiol. 1983, 46: 112-5.
Hosobuchi Y. Subcortical electrical stimulation for control of intractable pain in humans. Report of 122 cases (1970-1984). J Neurosurg. 1986, 64: 543-53.
Hughes J, Smith TW, Kosterlitz HW, Fothergill LA, Morgan BA, Morris HR. Identification of two related pentapeptides from the brain with potent opiate agonist activity. Nature. 1975, 258: 577-80.
Iggo A. Is the physiology of cutaneous receptors determined by morphology? Prog Brain Res. 1976,43 :15-31.
Javed S, Viswanathan , Abd S. Cordotomy for Intractable Cancer Pain: A Narrative Review. Pain Physician 2020; 23:283-292
Jeanmonod D, Maguin M, Morel. Comentarios al capítulo: Medial Thalamotomy. Dougherty, PM, Lee J, Dimitriou T, Lenz FA. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002:802-804.
Kanpolat Y. Percutaneous Stereotactic Pain Procedures. En: Surgical Management of Pain. Burquiel KJ (Ed). Thieme. New York. 2002: 745-762
Katayama Y, Yamamoto T, Kobayashi K, Oshima H, Fukaya C. Deep brain and motors cortex stimulation for poststroke movement disorders and poststroke pain. Acta Neurochir 2003, 87: 121-123.
Kellaway P. The part placed by electrical fish in the early history of bioelectricity and electrotherapy. Bull Hist Med 1946, 20: 112-137
Kerr FW. The ventral spinothalamic tract and other ascending systems of the ventral funiculus of the spinal cord. J Comp Neurol. 1975, 159: 335-56.
Kerr FW. Neuroanatomical substrates of nociception in th espinal cord. Pain 1975, 1: 325-356
Kerr FW, Wilson PR. Pain. Annu Rev Neurosci. 1978;1: 83-102.
Kevetter GA, Haber LH, Yezierski RP, Chung JM, Martin RF, Willis WD. Cells of origin of the spinoreticular tract in the monkey. J Comp Neurol. 1982, 207: 61-74.
Kim D, Lee S, Son B. Stereotactic Mesencephalotomy for Cancer – Related Facial Pain. J Korean Neurosurg Soc. 2014 Jul; 56(1): 71–74.
Kjerulf TD, Loser JD. Neuronal hyperactivity following deafferentation of the lateral cuneatus nucleus. Exp Neurol 1973, 39: 86-102
Kumazawa T, Perl ER. Excitation of marginal ans substantia gelatinosa neurones in the primate spinard cord. Indications of their place in dorsal horn functional organisation. Journal of Comparative Neurology 1978, 177: 417-434
Larson SJ, Sances A, Riegel D, Meyer GA, Dallman DE. Neurophysiological effects of dorsal column stimulation in man and monkey. J Neurosurg 1974, 41: 217-223
Le Beau J. Anterior cingulectomy in man. J Neurosurg 1954; 11: 268-276.
Lefaucheur JP, Drouot X, Cunin P, Brucket R, Lepetit H, Creange A, Wolkenstein P, Maison P, Keravel Y, Nguyen JP. Motor cortex stimulation for the treatment of refractory peripheral neuropathic pain. Brain 2009, 132: 1463-1471
Lenz FA, Kwan HC, Dostrovsky J. Characteristic of the bursting pattern of action potentials that occurs in the thalamus of patients with central pain. Brain res 1989, 496: 357-369
Leone M, Franzini A, Bussone G. Stereotactic stimulation of posterior hypothalamic gray matter in a patient with intractable cluster headache. N Engl J Med. 2001; 345(19):1428-9.
Leone M, Franzini A, Proietti A, Broggi G, Bussone G. Hypothalamic deep brain stimulation in the treatment of chronic cluster headache. Ther Adv Neurol Disord. 2010; 3(3):187-95.
Leone M, Franzini A, Cecchini AP, Bussone G.Efficacy of hypothalamic stimulation for chronic drug-resistant cluster headache. Cephalalgia. 2012; 32(4):267-8.
Leriche R. The Surgery of Pain. Baltimore: Williams & Wilkins. 1939.
Levy RM, Lamb S, Adams JE. Treatment of chronic pain by deep brain stimulation: long term follow-up and review of the literature. Neurosurgery. 1987, 21: 885-93.
Levy R, Deer TR, Henderson J. Intracranial neurostimulation for pain control. Pain Physician 2010, 13: 157-165.
Lima MC, Fregni F. Motor cortex stimulation for chronic pain: systematic review and meta-analysis of the literature. Neurology 2008, 70: 2329-2337
Linderoth B, Foreman RF, Meyerson BA. Mechanisms of spinal cord stimulation in neuropathic and ischemic pain syndromes. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 345- 354
Loeser JD. Intraduction: ablative neurosurgical operations. En: Bonica JJ (Ed) The Management of Pain. Philadelphia: Lea and Febiger. 1990: 2040-2043.
Long DM. Cutaneous afferent stimulation for relief of chronic pain. Clin Neurosurg 1974, 21: 257-268
Long DM, Erickson D, Campbell J, North R. Electrical stimulation of the spinal cord and peripheral nerves for pain control. A 10-year experience. Appl Neurophysiol. 1981, 44: 207-217
Luft R, Olivecrona H. Experiences with hypophysectomy in man. J Neurosurg 1953; 10: 301-316.
Machado AG, Mogilner AY, Rezai AR. Motor cortex stimlation for persistent nn- cancer pain. En: Textbook of Stereotactic and Functional Neurosurgery. Lozano A, Gildenberg PhL, Tasker RR. Springer. 2ªEd. 2009. pp.2239-2249
Mannheimer JS. Nonmedicinal and noninvasive pain control techniques in the management of rheumatic disease and related musculoskeletal disorders. J Rheumatol Suppl. 1987, 14 Suppl 15: 26-32.
Marchet A. History of a singular nervous or paralytic affection, attended with anomalous morbid sensations. Med Chir Tr 1811; 2: 15
Mayer DJ, Hayes RL. Stimulation-produced analgesia: development of tolerance and cross-tolerance to morphine. Science. 1975, 188: 941-94
Mayer DJ, Price DD, Becker DP. Neurophysiological characterization of the anterolateral spinal cord neurons contributing to pain perception in man. Pain. 1975, 1: 51-58.
Mayer DJ, Price DD. Central Nervous System mechanisms of analgesia. Pain 1976, 2: 379-404.
Mazars G, Roge R, Mazards Y. Rèsultats de la stimulation du faisceau spino-thalamic et leur incidence sur la physiopathologie de la douleur. Revue Neurol 1960, 103: 136- 138.
Mazars G, Merienne L, Cioloca C. Stimulations thalamiques intermittentes. Revue Neurol 1973, 128: 273-279
Mazars G. Etat actuel de la chirurgie de la douleur. Neurochirurgie 1976, 22. Suppl 1
Mazars G, Merienne L, Cioloca C. Comparative study of electrical stimulation of posterior thalamic nuclei, periaqueductal grey and other midline mesencephalic structures in man. Raven Press. NY. 1979
Mazars GJ. Intermittent stimulation of nucleus ventralis posterolateralis for intractable pain. Surg Neurol 1975, 4: 93-94
Meglio M, Cioni B, Dal Lago A, De Santis M, Pola P, Serricchio M. Pain control and improvement of peripheral blood flow following epidural spinal cord stimulation: case report. J Neurosurg. 1981, 54: 821-823
Mehler WR. The anatomy of the so-called “pain tract” en man: an analysis of the course and distribution of the ascending fibres of the fasciculus anterolateralis. En: Basic Research in Paraplegia. French JD, Porter RW (Eds.). Thomas. Springfield. 1962. pp 26-55
Melzack R y Casey KL. Sensory, motivational and central control determinants of pain. A new conceptual model. En: The Skin Senses. Kenshalo DR (Ed). Thomas. Springfield. 1968: 423-439.
Melzack R y Wall PD. Pain mechanisms: a new theory. Science 1965, 150: 971-979.
Melzack R. Prolonged relief of pain by brief, intense transcutaneous somatic stimulation. Pain. 1975, 1: 357-73.
Melzack R, Stillwell DM, Fox EJ. Trigger points and acupuncture points for pain: correlations and implications. Pain. 1977, 3: 3-23.
Melero A, Martinez R, de Teresa E, García de Sola R, Reig E. Estimulación medular epidural en la angina refractaria al tratamiento convencional. En: Estimulación Eléctrica biológica. Barbera J (Ed.). Servicio de Publicaciones. Universidad de Cadiz. 1989. pp. 159-169
Merskey H y Bogduk N. Classification of chronic pain. 2nd ed. Seatle; IASP Press, 1994.
Meyerson BA, Håkansson S. Alleviation of atypical trigeminal pain by stimulation of the Gasserian ganglion via an implanted electrode. Acta Neurochir Suppl (Wien). 1980;30:303-9.
Meyerson BA. Electrostimulation procedures: effects, presumed rationale, and possible mechanisms. Adv Pain Res Ther 1983, 5: 495-534
Meyerson BA, Linddblom U, Linderoth B, Lind G, Herregodts P. Motor cortex stimulation as treatment of trigeminal neuropathic pain. Acta neurochir Suppl 1993, 58: 150-153
Mundinger F, Salomão JF. Deep brain stimulation in mesencephalic lemniscus medialis for chronic pain. Acta Neurochir Suppl (Wien). 1980, 30: 245-58.
Murphy DF y Giles KE. Dorsal column stimulation for pain relief for intractable angina pectoris. Pain 1987, 28: 365-368
Nashold BS y Fiedman H. Dorsal column stimulation for control of pain. Preliminary report on 30 patients. J Neurosurg 1972, 36: 590-597
Nashold BS, Urban B, Zorub DS. Phantom pain relief by focal destruction of the substantia gelatinoisa of Rolando. Adv Pain Res Ther 1976; 1: 959-963.
Nashold BS, Ostdahl Ph. Dorsal root entry zone lesions. J Neurosurg 1979; 51: 59-69.
Nashold BS Jr, Mullen JB, Avery R. Peripheral nerve stimulation for pain relief using a multicontact electrode system. J Neurosurg 1979, 51: 872-873
Nashold BR. Brainstem stereotaxic procedures. En: Stereotaxy of the Human Brain. Schaltenbrand G, Walker AE (Ed). Georg Thieme Verlag. New York. 1982:475-483.
Nashold BS, El-Naggar A, Addulhak MM, Ovelman-Levitt J y Cosman E. Trigeminal nucleus caudalis dorsal root entry zone: a new surgical approach. Stereotac Funct Neurosurg 1992; 59:45-51.
Nauta HJW, Westlund KN, Willis WD. Midline Myelotomy. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 714-731.
Nguyen JP, Keravel Y, Feve A. Treatment of deafferentation pain by chronic stimulation of the motor cortex: report of a series of 20 cases. Acta Neurochir Suppl (Wien) 1997, 68: 54-60
Nguyen JP, Lefaucheur JP, Raoul S, Roualdes V, Péréon Y, Keravel Y. Motor cortex stimulation for the treatment of neuropathic pain. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Oxford. 2009. pp. 515-526
Nielson KD, Adams JE, Hosobuchi Y. Experience with DC stimulation for relief of chronic intractable pain: 1968-1973. Surg neurol 1975, 4: 148-152
Nielson KD, Watts C, Kempclark W. Peripheral nerve injury from implantation of chronic stimulating electrodes for pain control. Sueg Neurol 1976, 5: 51-53
Owens S, Atkinson ER, Lees DE. Thermographic evidence of reduced sympathetic tone with transcutaneous nerve stimulation. Anesthesiology. 1979, 50: 62-65.
Owen SLF, Green AL, Nandi D, Bottar RG, Wang S, Aziz TZ. Deep brai stimulation for neuropathic pain. Neuromodulation 2006, 9: 100-106
Patel N, Agarwal N, Mammis A, Danish SF. Frameless Stereotactic Magnetic Resonance Imaging-Guided Laser Interstitial Thermal Therapy to Perform Bilateral Anterior Cingulotomy for Intractable Pain: Feasibility, Technical Aspects, and Initial Experience in 3 Patients. Operative Neurosurgery, Vol 11, 1. 2015: 17–25,
Pedrosa-Sánchez M, Sola RG. La moderna psicocirugía: un nuevo enfoque de la neurocirugía en la enfermedad psiquiátrica. Rev Neurol. 2003; 1-15; 36(9):887-97
Penfield W y Jasper H. Epilepsy and Functional Anatomy of the Human Brain. Little Brown Co. Boston 1954
Pereira EAC, Moir L, Green L, Aziz TZ. Deep brain stimulation for pain. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Oxford. 2009. pp. 499-505
Pfeiffer EA. Electrical stimulation of sensory nerves with skin electrodes for research, diagnosis, communication and behavioral conditioning: a survey. Med Biol Eng. 1968 6: 637-51
Perrault M, Lebeau J, Klotz B, Sicard J, Clavel B. L’hypophysectomie totale dans le traitment du cancer du sein: premier cas francais: avenir de la method. Therapie 1952; 7: 290-300.
Polin RS, Laws ER, Shaffrey ME. Hypophysectomy for Intractable Pain from Metastatis Carcinoma: a Historical Perspective. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 821-827.
Pool JL, Clark W, Hudson P, Lombardo M. Hypothalamic-Hypophyseal Interrelationships.Springfield IL: Charles C Thomas. 1956
Popeney CA y Alo KM. C1-C2-C3 peropheral nerve stimulation (PNS) for the treatment of disability associate with transformed migraine. Headache 2003, 43: 369- 373
Prager JP. Neurostimulation in the treatment of complex regional pain syndrome. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 385-395
Ray CD. Spinal epidural electrical stimulation for pain control. Practical details and results. Appl Neurophysiol. 1981, 44: 194-206.
Randić M, Miletić V. Effect of substance P in cat dorsal horn neurones activated by noxious stimuli. Brain Res. 1977, 128: 164-169.
Rasche D. Motor cortex stimulation for long-term relief of chronic neuropathic pain: a 10 year experience. Pain 2006, 121: 43-52
Reynolds DV. Surgery in the rat during electrical analgesia induced by focal brain stimulation. Science 1969, 164: 444-445
Rexed B. The cytoarchitectonic organisation of the spinal cord in the cat. Journal of Comparative neurology 1952, 96: 415-495
Rezai AR y Lozano AM. Deep brain stimulation for chronic pain. En: Surgical Management of Pain. Burchiel KJ (Ed.). Thieme. New York. 2002. pp 565-576.
Richardson DE y Akil H. Pain reduction by electrical stimulation in man. J. Neurosurg 1977, 47: 178-194.
Richardson DE y Akil H. Long-term results of periventriclar gray self-stimulation. Neurosurgery 1988, 1: 199-202
Richardson DE. Intracranial stimulation therapies: Deep-Brain Stimulation. En: Neurosurgical Pain Management. Follet KA (Ed.). Elsevier Saunders. Philadelphia. 2004. pp. 156- 159.
Riddoch G. The clinical features of central paiun. Lancet 1938; 234:1093-1098.
Schvarcz JR. Postherpetic craniofacial dysesthesiae: their management by stereotactic trigeminal nucleotomy. Acta Neurochir (Wien) 1977; 38: 65-77
Schvarcz JR. Stereotactic high cervical extralemniscal myelotomy for pelvic cancer pain. Acta Neuroch Suppl. 1984; 33: 431-435.
Scoville WB. Extradural spinal sensory rhizotomy. J Neurosurg 1966; 25: 94-95.
Sedan R y Lazorthes Y. La Neurostimulation électrique thérapeutique. Masson. Paris. 1977.
F Seijo 1, A Saiz, B Lozano, E Santamarta, M Alvarez-Vega, E Seijo, R Fernández de León, F Fernández-González, J Pascual. Neuromodulation of the posterolateral hypothalamus for the treatment of chronic refractory cluster headache: Experience in five patients with a modified anatomical target. Cephalalgia 2011; 31(16):1634-41.
Shealey CN, Mortimer JT, Reswick J. Electrical inhibition of pain by stimulation of the dorsal column: preliminary clinical reports. Anesth Analg 1967, 46: 489-491
Shealey CN. Transcutaneous stimulation for control of pain. Clin Neurosurg 1974, 21: 269-277
Shigenaga Y, Inoki R. Effect of morphine on single unit responses in ventrobasal complex (VB) and posterior nuclear group (PO) following tooth pulp stimulation. Brain Res. 1976, 103: 152-6.
Siegfried J. Introduction Historique. En: La neurostimulation électrique thérapeutique. Sedan R y Lazorthes Y (Eds). Masson. Paris. 1977. pp 5-10
Siegfried J, Shulman J. Deep brain stimulation. Pacing Clin Electrophysiol. 1987 Jan;10(1 Pt 2):271-2.
Sindou M. Etude de la Jonction radiculo-médullaire postérieure: La radicellotomie postérieure sélective dans la Chirurgie de la Douleur (Thesis). Lyon, France.
University Claude-Bernard. 1972.
Sindou MP. Microsurgical DREZotomy. En: Smideck HH, Sweet Wh (Ed). Operative Neurosurgical Techniques. 3rd Ed Philadelphua: WP Saunders. 1995: 1613-1622
Sindou MP, Turano G, Pantieri R, et al. Intraoperative monitoriung of spinal cord SEPs, during microsurgical DREZotomy (MDT) for pain, spasticity and hyperactive bladder. Stereot Funct Neurosurg 1994; 62: 164-170.
Sindou MP. Dorsal root entry zone lesions. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 701-713.
Sjöqvist O. Studies on pain conduction in the trigeminal nerve: a contribution to the surgical treatment of facial pain. Acta Psychiatr Neurol Scan 1938; 1: 93-122.
Sloan PA. Radiosurgical pituitary ablation for cancer pain. J Palliat Care 1996; 12: 51- 53.
Sluka KA, Smith HS, Walsh DM. Transcutaneous Electric Nerve Stimulation (TENS): A Review. En: Neuromudulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 335-344
Sourek K. Commissural myelotomy. J. Neurosurgery 1969; 31: 524-527.
Spiegel EA, Wycis HT, Marks M y Lex AJ. Stereotaxic Apparatus for Operations on the Human Brain. Science, 1947; 106: 349.
Spiegel EA y Wycis HT. Mesencephalotomy in the treatment of “intractable” facial pain. Arch Neurol 1953; 69: 1-13.
Spiegel EA, Kletzkin M, Szekely EG. Pain reaction upon stimulation of the tectum mesencephalic. J Neuropathol Exp Neurol 1954; 13: 212-220
Spiegel EA, Wycis HT, Szekely EG, Gildenberg PL, Zanes C. Combined dorsomedial, intralaminar and basal thalamotomy for relief of so-called intractable pain. J Int Coll Surg 1964; 42: 160-168
Spiller WG y Martin E. The treatment of persistent pain of organic origin in the lower part of the body by division of the anterolateral column of the spinal cord. JAMA 1912; 58: 1489-1490
Stanton-Hicks M. Peripheral nerve stimulation for pain peripheral neuralgia and complex regional pain syndrome. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp.397-407
Steel TR y Burchiel KJ. Ablative Neurosurgical Techniques in the Treatment of Chronic Pain: Overview. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 633-646.
Stillings D. A survey of the history of electrical stimulation for pain to 1900. Med Instrum 1975, 9: 235-259
Sweet WH y Wepsic JG. Stimulation of the posterior columns of the spinal cord for pain control. Indications-Technics and results. Clin Neurosurg 1974, 21: 278-310
Sweet WH. Control of pain by direct electrical stimulation of peripheral nerves. Clin Neurosurg 1976, 23: 102-111
Sweet WH. Central mechanisms of chronic pain (neuralgias and other neurogenic pain). En: Pain..Bonica JJ (Ed). Raven Press. New York.1980: 287-303..
Taha JM. Dorsal root ganglionectomy and dorsal rhizotomy. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 677-687.
Talairach J, Tournoux P. Appareil de stéréotaxie hypophysaire pour voie d’abord nasale. Neurochirurgie 1955; 1: 127-131.
Tanel T, Kajita Y, Noda H, Takebayashi S, Nakatsubo D, Maesawa S, Wakabayashi
T. Efficacy of motor cortex stimulation for intractable central neuropathic pain: comparison of stimulation parameters between post-stroke pain and other central pain. Neurol Med Chir (Tokyo) 2011, 51: 8-14.
Tasker RR, Emmers R. The Human Somesthetic Thalamus. Raven Press. New York, 1975.
Tasker RR, Organ LW, Hawrylyshyn P. Deafferentation and causalgia. En: Bonica JJ (Ed). Pain. New York: Raven Press. 1980: 305-329.
Tasker RR y Dostrovsky JO. Deafferentation and central pain. En: Wall PD y Melzack R (Ed). Textbook of Pain. 2nd Ed. Edinburg: Churchill-Livingstone; 1989:154-180.
Tasker RR. Deafferentation pain syndromes. En: Nashold BS y Ovelmen-Levittt (Ed). Deafferentation Pain Syndromes: Pathophysiology and Treatment. New York: Raven Press; 1991: 241-258.
Tasker RR. Percutaneous cordotomy. En: Schmidek HH y Sweet WH (Ed) Operative Neurosurgical Techniques. 3rd Ed. Philadelphia: WB Saunders 1995:1595-1612.
Taub E, Munz M, Tasker RR. Chronic electrical stimulation of the gasserian ganglion for the relief of pain in a series of 34 patients. J Neurosurg. 1997, 86: 197-202.
Treede RD, Kenshalo DR, Gracely RH, Jones AK. The cortical representation of pain. Pain. 1999, 79: 105-11.
Trevino DL, Coulter JD, Willis WD. Location of celles of origin of spinothalamic tract in lumbar enlargement of the monkey. J Neurophysiol 1973, 36: 750-761
Tsubokawa T, Yamamoto T, Katayama Y, Moriyasu N. Clinical results and physiological basis of thalamic relay nucleus stimulation for relief of intractable pain with morphine tolerance. Appl Neurophysiol. 1982;45(1-2):143-55.
Tsubokawa T, Katayama Y, Yamamoto Y, Hirayama T, Koyama S. Chronic motor cortex stimulation for the treatment of central pain. Acta Neurochir Suppl. 1991, 52: 137-139.
Tsubokawa T, Katayama Y, Yamamoto T, Hirayama T, Koyama S. Chronic motor cortex stimulation in patients with thalamic pain,. J Neurosurg 1993; 78: 393-401.
Tsubokawa T. Motor cortex stimulation for relief of central deafferentation pain. En: Surgical Management of Pain. Burchiel KJ. Thieme. Ney York. 2002. pp. 555-574
Turnbull IM, Shulman R, Woodhurst WB. Thalamic stimulation for neuropathic pain. J Neurosurg 1980, 52: 486-493
Uematsu S. Percutaneous electrothermocoagulation of spinal nerve trunk, ganglion and rootlets. En: Smidek HH y Sweet WS (Ed). Operative Neurosurgical Techniques: Indications, Methods and Resuls. 2nd Ed. New York: Grune & Stratton. 1988: 1207- 1221.
Velasco M, Velasco F, Brito F. Motor cortex stimulation in the treatment of deafferentation pain: localization of the motor cortex. Stereotact Funct Neurosurg 2002, 79: 146-167
Velasco F. Efficacy of motor cortex stimulation in the treatment of neuropathic pain: a randomized double-blind trial. J Neurosurg 2008, 108: 698-706
Viswanathan A, Harsh V, Erlick A, Pereira C, Aziz TZ.Cingulotomy for medically refractory cancer pain Neurosurg Focus 2013 Sep;35(3)
Walker AE. Relief of pain by mesencephalic tractotomy. Arch Neurol 1942; 48: 865- 883.
Wall PD y Sweet WH. Temporary abolition of pain in man. Science 1967, 155: 108- 109
Weiner RL. Occipital neuroostimulation (ONS) for treatment of intractable headache disorders. Pain Med 2006, 7: S137-S139
Weiner RL y Alo’ KM. Occipital neurostimulation for treatment of intractable headache síndromes. En: Neuromodulation. Krames ES, Peckham PH, Rezai AR (Eds). Elsevier. Amsterdam. 2009. pp. 409-416
West CR, Avellanosa AM, Brtemer AM, Yamada K, Hypophysectomy for relief of pain of disseminated carcinoma of the prostate. En: Advances in Pain Research and Therapy. Bonica JJ, Ventafrida V (Eds). Raven Press. New Yoek. 1979: 393-400.
White JC y Sweet WH. Pain and the Neurosurgeon. A Forty-Year Experience. Charles C Thomas Publ. Springfield. 1969.
Whitsel BL, Petrucelli LM, Werner G. Symmetry and connectivity in the map of the body surface in somatosensory area II of primates. J Neurophysiol. 1969, 32: 170-83.
Willis WD. The Pain System. The Neural Basis of Nociceptive Transmission in the Mammalian Nervous System. Karger. . Basilea. 1985
Yezierski RP. Central Pain. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002. Pp 42-64.
Young JN y Wilkins RH. Partial sensory trigeminal rhizotomy at the pons for trigeminal neuralgia. J Neurosurg 1993; 79(5):680-687.
Young RF, Jacques DS, Rand RW. Technique of stereotactic medial thalamotomy with Leksell gamma knife for treatment of chronic pain. Neurol Res 1995; 17: 59-65
Young RF y Rinaldi PC. Brain Stimulation. Springer Verlag. New York. 1997
Young RF. Comentario al capítulo de Gorecki JP y Rubin LL. Caudalis Dorsal Root Entry Zone, Nucleotomy and Tractotomy. En: Surgical Management of Pain. Burchiel KJ (Ed). ThiemeNew York. 2002: 785..
Zotterman Y. Touch, pain and tickling: an electrophysiological investigation o cutaneous sensory nerves. Journal of Physiology 1939, 95: 1-28
Bonica JJ. Pain. Raven Press. New York.1980.
Burchiel KJ (Ed). Surgical Management of Pain. ThiemeNew York. 2002
Follet KA (Ed). Neurosurgical Pain Management. Elsevier Saunders. Philadelphia. 2004.
Gildenberg PL, Tasker RR (Eds). Textbook of Stereotactic and Functional Neurosurgery. McGraw-Hill. New York. 1998
Schaltenbrand G, Walker AE (Ed). Stereotaxy of the Human Brain. Georg Thieme Verlag. New York. 1982:475-483.
Schmidek HH y Sweet WS (Ed). Operative Neurosurgical Techniques: Indications, Methods and Results. 2nd Ed. New York: Grune & Stratton. 1988
Wall PD y Melzack R (Ed). Textbook of Pain. 2nd Ed. Edinburg: Churchill- Livingstone. 1989.
Wilkins y Rengachary (Eds). Neurosurgery. 2nd ed. Mc Graw Hill Book Co. New York. 1995
White JC y Sweet WH. Pain and the Neurosurgeon: A Forty-Year Experience. Charles C Thomass. Springfield. 1969.