Simulación con Neuronavegación 3D para aprender la colocación de tornillos de trayectoria del hueso cortical
Nota técnica recibido: 22 de noviembre de 2019 aceptada después de la revisión 23 de marzo de 2020
(c) Georg Thieme Verlag KG Stuttgart – Nueva York
DOI https://doi.org/10.1055/s-0040-1715485. ISSN 2193-6315.
Publicación del equipo del Dr. R. García de Sola. Se trata de un estudio de investigación-innovación en el campo de la cirugía de columna y Neuronavegación en 3D.
Ver artículo publicado por Thieme en el Jornal of Neurological Surgery.
Juan Delgado-Fernández 1 Division of Neurosurgery University Hospital 12 de Octubre, Madrid, Spain.
Natalia Frade-Porto 2 Division of Neurosurgery, University Hospital La Princesa, Madrid, Spain.
Guillermo Blasco 2 Division of Neurosurgery, University Hospital La Princesa, Madrid, Spain.
Patricia Gonzalez-Tarno 2 Division of Neurosurgery, University Hospital La Princesa, Madrid, Spain
Ricardo Gil-Simoes 2 Division of Neurosurgery, University Hospital La Princesa, Madrid, Spain.
Paloma Pulido 2 Division of Neurosurgery, University Hospital La Princesa, Madrid, Spain.
R. García Sola 3 Department of Innovation in Neurosurgery, Universidad Autónoma de Madrid, Madrid, Spain4 Neurosurgical Department Hospital Nuestra Señora del Rosario, Madrid, Spain.
Dirección para correspondencia Juan Delgado Fernández, MD, División de Neurocirugía, Hospital Universitario 12 de Octubre, Avda de Córdoba S/N, 28041, Madrid, España (e-mail: juan.delgado.fdez@gmail.com).
Abstract
Antecedentes y objetivo.-
Aprender una nueva técnica en Neurocirugía es un gran desafío especialmente para los principiantes. En los últimos años, las simulaciones y los simuladores se han convertido en una herramienta de enseñanza. Nuestro objetivo es proponer un simulador para la colocación de tornillos de trayectoria ósea cortical (CBT) para mejorar los resultados y reducir las complicaciones.
Métodos.-
Hemos creado una plataforma que consiste en un hueso de sierra que se navega con un fluoroscopio 3D para familiarizar a nuestros aprendices y especialistas con la técnica de CBT y posteriormente implementarla en nuestro departamento. La evaluación objetiva estructurada de las aptitudes técnicas (OSATS) y la escala de inventario de diagnóstico del desempeño de los médicos (PPDI) se obtuvieron antes y después del uso del simulador por los cinco participantes en el estudio. Los pacientes que fueron operados después de la aplicación de la técnica fueron revisados retrospectivamente.
Resultados.-
Durante la simulación, hubo 4 casos de rotura de pedículo de los 24 tornillos insertados (16,6%). Después de completar la simulación, los participantes demostraron una mejora en el OSATS y el PPDI (p 1⁄4 0.039 y 0.042, respectivamente). Analizando las respuestas a los diferentes ítems de las pruebas, los participantes mejoraron principalmente en el conocimiento (p1⁄40.038), el rendimiento (p1⁄40.041), y la comprensión del procedimiento (p 1⁄4 0.034). En nuestra serie retrospectiva, ocho pacientes con inestabilidad L4-L5 fueron operados usando CBT, mejorando su puntuación en el Índice de Discapacidad de Oswestry (ODI) (ODI preoperatorio 58.5 [SD 16.7] vs. ODI postoperatorio 31 [SD 13.4]; p 1⁄4 0.028). Se observó una complicación intraoperatoria debido a un desgarro de la duramadre. En el seguimiento, encontramos un caso de pseudoartrosis y una violación de la articulación facetaria, pero ninguna otra complicación relacionada con la mala colocación, fractura del pedículo o fallo de hardware.
Conclusión.-
La simulación que hemos creado es útil para la aplicación de la CBT. En nuestro estudio, los especialistas y los alumnos han valorado muy positivamente el aprendizaje obtenido con el sistema. Además, la simulación facilitó el aprendizaje de la técnica y la comprensión de la anatomía quirúrgica. Esperamos que la simulación ayude a reducir las complicaciones en el futuro.
Palabras clave:
► trayectoria del hueso cortical
► simulación
► neuroquirúrgico formación
► complicaciones.
Introducción
En los últimos años, se han presentado desafíos y oportunidades en la formación de jóvenes neurocirujanos. Uno de los problemas más importantes es la restricción de horas de trabajo para los residentes, reduciendo la exposición a los casos quirúrgicos. Además, la neurocirugía es una especialidad de alta precisión que implica procedimientos complejos, junto con herramientas y software de alta complejidad. Así pues, dominar una nueva técnica con una pequeña cantidad de casos y una práctica real limitada es difícil (1,3).
La creciente atención a la seguridad y los resultados del paciente hace que la práctica tradicional de «ver a uno, hacer uno, enseñar a uno» ya no sea aceptable. Por lo tanto, hay que implementar nuevos métodos para enseñar a los jóvenes neurocirujanos. Algunos autores han propuesto que la formación en neurocirugía esté determinada por algunos hitos y competencias logrados durante la residencia que deben ser documentados objetivamente (4-6).
Los simuladores han sido desarrollados como una de las soluciones a este desafío en la educación neuroquirúrgica. Los simuladores se viene utilizando en la educación desde hace ya 20 años, principalmente como modelos sintéticos, como las sierras o los maniquíes, y como plataformas de realidad virtual (7,8) . Incluso antes se utilizaban cadáveres para el entrenamiento (2,4).
No obstante, en los últimos años ha aumentado el interés por desarrollar nuevos simuladores, porque la tecnología avanzada permite crear modelos con intercaras de tejido fiables que representan adecuadamente los hitos quirúrgicos (3,9). Este hecho ha sido reconocido por entidades como el Comité Conjunto de Capacitación Quirúrgica (2,10,11).
Sólo hay unos pocos simuladores, aparte de los modelos de huesos de sierra y cadáveres, para realizar la inserción de tornillos para la fijación de la columna vertebral (12-14). Como señalaron Boody y otros, el desarrollo de las aptitudes quirúrgicas necesita una «curva de aprendizaje» que requiere una repetición frecuente para garantizar la precisión y la coherencia (15).
En los últimos años, se han hecho nuevas propuestas de diferentes trayectorias para los tornillos pediculares en diferentes patologías de la columna vertebral (17).
Los tornillos de trayectoria ósea cortical (CBT), que han sido propuestos por Santoni y otros (18) , obtienen una mejor resistencia a la extracción en pacientes osteoporóticos, tienen buenas propiedades biomecánicas y también permiten una técnica mínimamente invasiva debido a una menor exposición. Aunque, como explicaron Dabbous y otros (19) , esta técnica es bastante sencilla debido a la similitud con el procedimiento tradicional, creemos que existe una curva de aprendizaje importante y que la técnica tiene que ser entrenada antes de utilizarla como procedimiento estándar en un departamento (20). Por lo tanto, el objetivo de este artículo es presentar un nuevo simulador de colocación de tornillos de trayectoria ósea cortical (CBT), y los resultados preliminares después de este entrenamiento.
Métodos
Desarrollo del simulador
El simulador consiste en huesos («sawbones») de la columna lumbar de anatomía normal, desde la L1 hasta el sacro, en un soporte de columna prefabricado. Los «sawbones» se colocan en una mesa quirúrgica radiotransparente Jackson y se fijan con cintas adhesivas.
Entonces, la matriz de referencia para la neuronavegación se une a la protuberancia sacra. A continuación, se obtuvieron imágenes con el sistema de fluoroscopia 3D intraoperatorio (Siemens Medical Solutions, Erlangen, Alemania) y se realizó una reconstrucción 3D con el sistema Brainlab (Munich, Alemania) para la navegación de la columna vertebral.
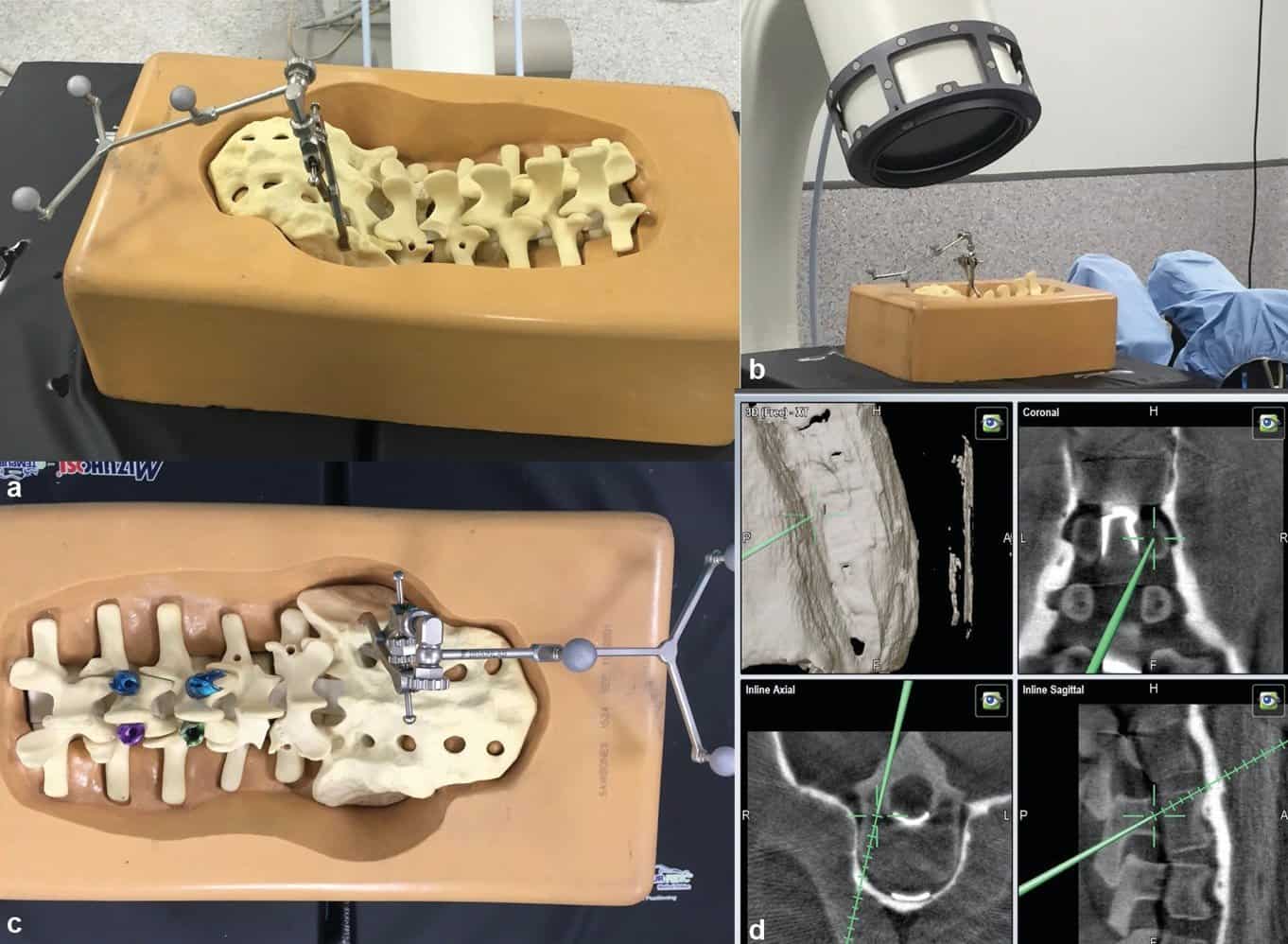
Las herramientas de neuronavegación fueron calibradas para su uso posterior. Utilizamos tornillos pediculares de doble rosca, ya que parecen más adecuado para los tornillos corticales21 y debido a su mejor características biomecánicas (22) con un diámetro de 5,5 mm y una longitud de 35 a 45 mm. Bajo la guía de la imagen, se insertaron tornillos corticales a ambos lados de la L1 a S1. Se utilizaron puntos de referencia anatómicos según la técnica descrita previamente (18,22,24,25), localizando el punto de entrada 1 mm inferior al borde inferior de la apófisis transversal y 3 mm medial al margen lateral del istmo y se proyecta en la posición de las 5 en el pedículo izquierdo y en la posición de las 7 en el pedículo derecho. Se utilizó una angulación craneocaudal de 25 a 30 grados en la dirección de la placa final superior. Después de planear la trayectoria correcta, y estimar el tornillo más adecuado, se usó un punzón guiado por imagen para crear la trayectoria del tornillo, y con una sonda de punta de bola el cirujano comprobó que era correcta. Después de la inserción del tornillo guiada por imagen, se realizó una nueva exploración 3D fluoroscopia para asegurar la posición correcta de los tornillos y, finalmente, se realizó una inspección visual de los huesos de la sierra para asegurarse de que no había complicaciones relacionadas con la inserción de tornillos ( ►Fig. 1).
Evaluación del simulador
Cinco personas del equipo de neurocirugía participaron en el estudio, dos residentes junior, un residente senior y dos especialistas. Todos llevaron a cabo la inserción de tornillos CBT. Para validar la utilidad del modelo, se evaluó a la persona en formación utilizando el método de Evaluación Estructurada Objetiva de Habilidades Técnicas (OSATS) y la Escala de Inventario de Diagnóstico del Desempeño del Médico (PPDI) antes y después del uso del simulador. La escala OSATS es una puntuación que se utiliza para evaluar el rendimiento de los aprendices en diversas tareas de procedimiento y se basa en los siguientes parámetros: respeto de los tejidos, tiempo y movimiento, manejo de los instrumentos, conocimiento de los instrumentos, flujo de operación, uso de asistentes y conocimiento del procedimiento específico (3,26).
Estas habilidades fueron evaluadas por un especialista senior. El PPDI se realizó antes y después de la simulación, y los elementos fueron evaluados como «insatisfactorio», «principiante», «competente», » eficiente» o «experto» (puntuaciones de 1 a 5). Los elementos evaluados en el PPDI fueron los siguientes: uso del punzón, uso de la sonda de punta de bola, rendimiento del procedimiento, conocimiento de la anatomía y economía de los movimientos/eficiencia del procedimiento (9,15).
Implementación de la técnica
Los pacientes con estenosis espinal en el nivel L4-L5 y sin o con mínima listesis (grado 1 de Meyerding) fueron incluidos como candidatos para este estudio, que se llevó a cabo entre diciembre de 2017 y mayo de 2018 en nuestro centro. En esos casos, la cirugía se realizó en una mesa quirúrgica radiotransparente Jackson con guía por imagen, de manera similar a la del simulador.
La matriz de referencia estaba unida a un fijador de dos pines colocado en la cresta ilíaca del paciente. Más tarde, se obtuvieron imágenes con fluoroscopia 3D intraoperatoria y se realizó una reconstrucción 3D. La cirugía comenzó con una incisión en la línea media sobre el nivel patológico y una disección subperióstica de los músculos hasta que el proceso articular quedó expuesto.A continuación se colocaron tornillos corticales (5,5 mm de diámetro y 40 a 45 mm de longitud; Janus, Orthofix Lewisville, Texas) utilizando los puntos de referencia descritos anteriormente y utilizando la guía de imágenes. La descompresión se realizó después de que se confirmara la posición correcta de los tornillos mediante un escáner fluoroscópico en 3D.
Las medidas de resultado se obtuvieron con la puntuación del Índice de Discapacidad de Oswestry (ODI), y las puntuaciones más bajas indican síntomas menos graves (27). Se obtuvo antes de la cirugía y en el seguimiento postoperatorio en el primer y sexto mes.
Los estudios radiológicos preoperatorios incluyeron tomografías y resonancias magnéticas en todos los casos. En el seguimiento postoperatorio del sexto mes, se realizó una TC para descartar complicaciones como la colocación incorrecta de tornillos, la pseudoartrosis y otras.
Además, se obtuvieron radiografías lumbares anteroposteriores y laterales en flexión-extensión para determinar la inestabilidad del segmento. Las tomografías computarizadas postoperatorias fueron evaluadas por los miembros del Departamento de Radiología, que estaban cegados al procedimiento quirúrgico.
Análisis estadístico
Los resultados de las pruebas OSATS y PPDI de los participantes que usaron el simulador se compararon con la prueba de rango firmada por Wilcoxon para muestras emparejadas no paramétricas con SPSS 21.0.
Resultados
Experiencia en el simulador
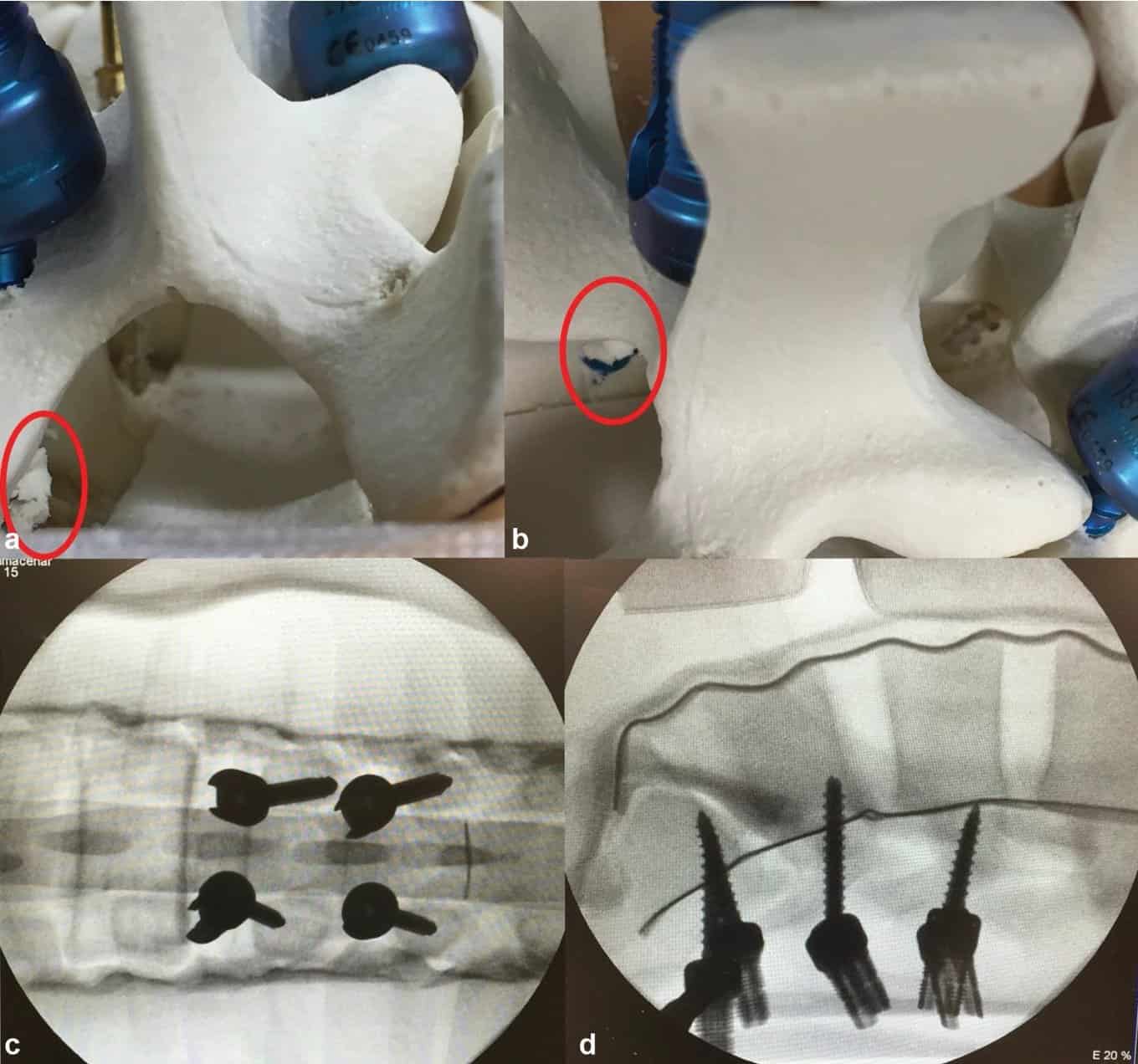
Cada participante pudo realizar al menos cuatro tornillos de hueso cortical con el simulador. En total, se colocaron 24 tornillos en dos «sawbones» diferentes, de la L1 a S1. Durante la inserción del tornillo, la parte medial del pedículo fue violada en cuatro ocasiones. Dos de ellas ocurrieron en la L2, mientras que el resto ocurrieron en la L1 y L4. Las violaciones ocurrieron al insertar el primer tornillo en un caso; en dos casos, fue el segundo tornillo; y en un caso, fue el tercer tornillo (►Fig. 2). No hubo ninguna rotura en la inserción del cuarto al sexto tornillo.
Se encontró una mejora estadísticamente significativa para el OSATS y el PPDI después del uso del simulador (p ¼ 0,039 y 0,042, respectivamente). Cuando analizamos las diferentes preguntas de cada una de las pruebas, en el caso del OSATS, hubo diferencias entre las relacionadas con el conocimiento del procedimiento (p ¼ 0.038) y las del tiempo y el movimiento, y la planificación anticipada que se acercaban a la significancia (p ¼ 0.059). De acuerdo con el PPDI, hubo una mejora en el rendimiento y la comprensión del procedimiento (p ¼ 0.041 y 0.034, respectivamente), y hubo una importante mejora en la economía de los movimientos y la eficiencia del procedimiento (p ¼ 0.059).
Experiencia clínica
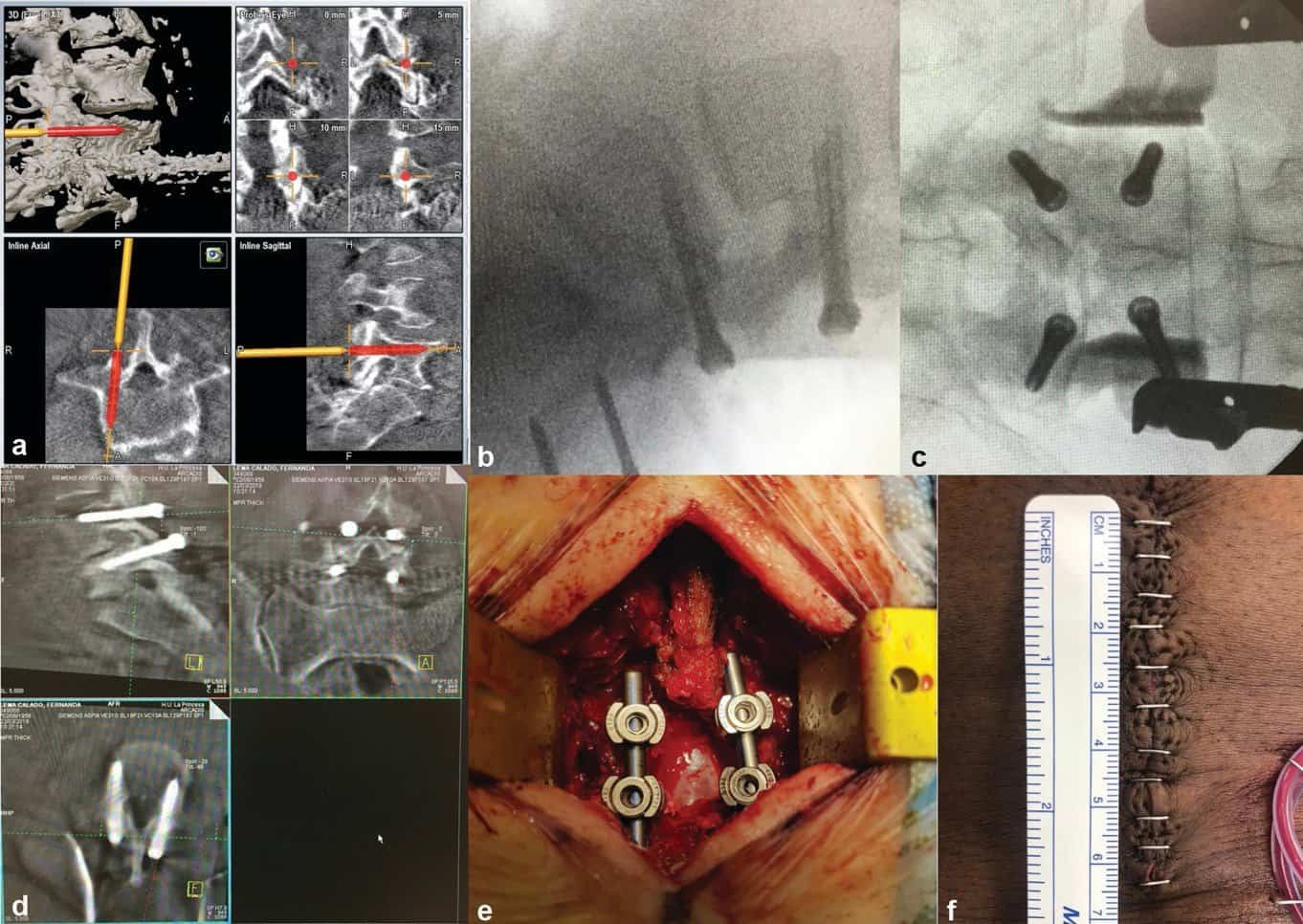
Ocho pacientes (cuatro hombres y cuatro mujeres) han sido operados en nuestro centro desde diciembre de 2017. La edad media de los pacientes fue de 72,25 años (SD: 9,5). Todos los pacientes fueron operados en el segmento L4-L5, y dos pacientes tenían una espondilolistesis de grado I de Meyerding. Todos los pacientes tenían signos de inestabilidad en las radiografías de flexion-extensión. La cirugía fue realizada por uno de los consultores y el residente principal en cada caso. La media de ODI preoperatorio fue de 58,5 (SD: 16,7). El tiempo medio de la operación fue de 138,75 minutos (rango 115-170 minutos) y sólo hubo una complicación intraoperatoria con un desgarro de la duramadre. La longitud media de la incisión fue de 7 cm (rango 6-8 cm). En ninguno de los casos se requirió una transfusión de sangre y la pérdida media de sangre durante la operación fue de 212,5 mL (rango de 100 a 300 mL; ►Fig. 3).
Se realizó una tomografía intraoperatoria en todos los casos. En un caso se observó la pérdida de dos tornillos, que fueron revisados posteriormente. El tiempo total medio de fluoroscopia fue de 2,55 minutos (SD: 0,55) y la exposición media a la radiación fue de 571,35 cGy/ cm2 (SD: 121,7).
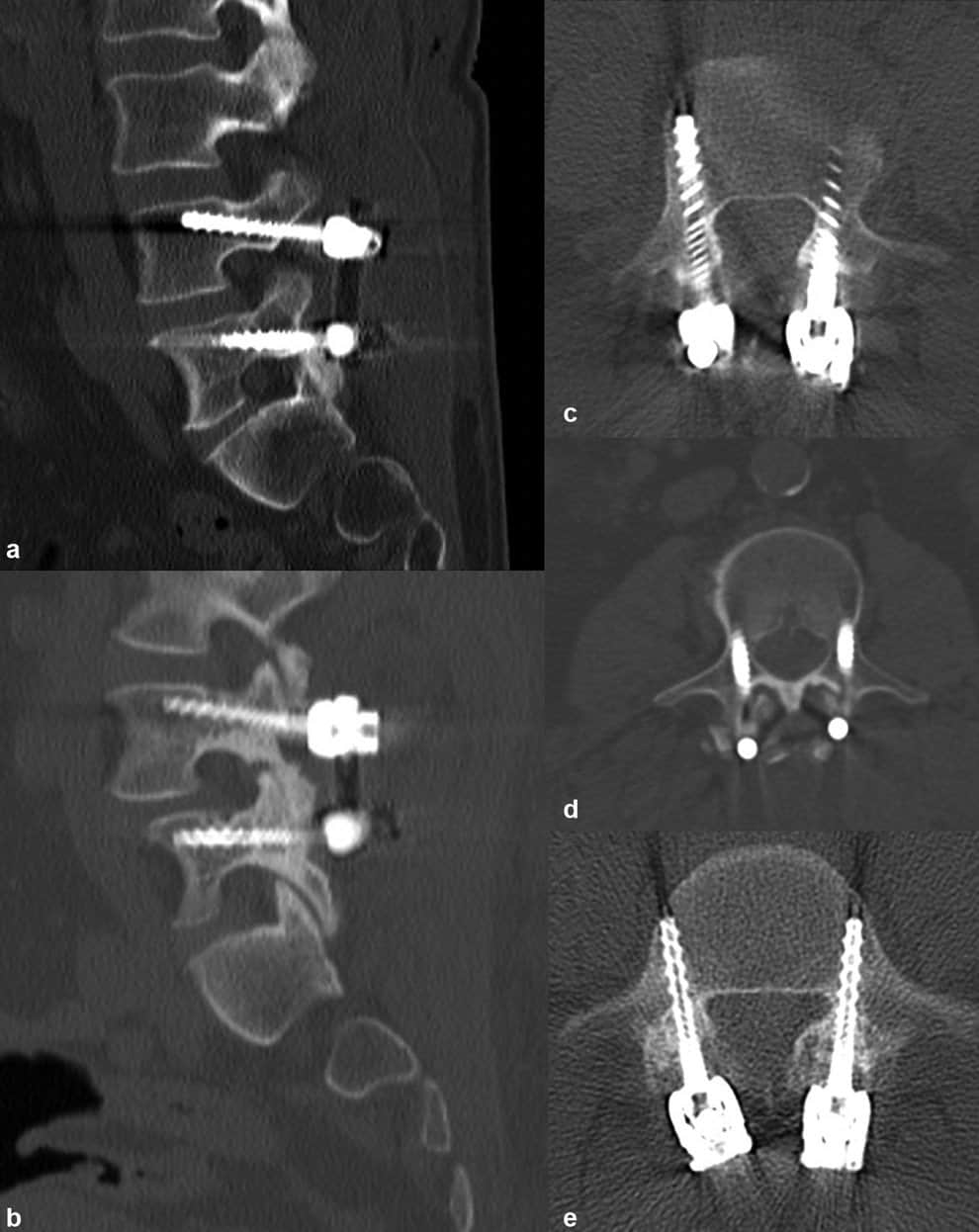
La media de seguimiento fue de 22,14 meses (rango 13,7-26,8 meses), mostrando una mejora en comparación con la puntuación de 31 en el postoperatorio inmediato del ODI (SD: 13,4, p 1/4 0,028). La duración media de la estancia fue de 4,5 días (SD: 1,7). En la tomografía postoperatoria durante el seguimiento, encontramos un caso de pseudorosis y una violación de la articulación de la cara superior. No hubo otras complicaciones relacionadas con el mala colocación, la rotura o la falla del «hardware» (►Fig. 4).
Discusión
El aprendizaje de nuevas técnicas en cirugía es un proceso complejo que requiere una gran cantidad de tiempo y disciplina. Según Krishnaney6 , las teorías más recientes sobre cómo se aprende una técnica son las de Fitts, Posner y Keebone.
Estos autores afirman que el proceso de aprendizaje incluye tres etapas: cognitiva, asociativa y autónoma. En la primera etapa los alumnos comprenden la técnica estudiando y observando, para conceptualizar el proceso. Luego, en la etapa asociativa, los alumnos comienzan a aplicar la técnica y a asociar las ideas previas con el proceso psicomotor. Finalmente, en la etapa autónoma, la repetición del procedimiento ayuda a realizar la operación de manera autónoma sin necesidad de «pensar» en el movimiento específico.
Según esta teoría, como hemos visto en los resultados de las pruebas del OSATS y el PPDI, nuestros alumnos han demostrado una mejora en la técnica CBT, principalmente en términos de conocimiento y comprensión del procedimiento; también se puede observar una mejora en el rendimiento. Este resultado está más relacionado con la fase asociativa del aprendizaje que con la economía de los movimientos o el tiempo y el movimiento, que podría estar más relacionado con la fase autónoma del aprendizaje. A pesar de estar en partes comparables a la colocación de tornillos pediculares estándar, una mejor comprensión de la técnica conducirá, en nuestra opinión, a obtener mejores resultados en el futuro (19).
Las curvas de aprendizaje de las nuevas técnicas han sido ampliamente estudiadas, y no sólo se necesitan las diferentes fases reconocidas en la teoría del ensayo mental para obtener experiencia en un procedimiento.
Algunos estudios han demostrado que los alumnos mejoran inicialmente su rendimiento antes de llegar a una meseta o fase plana, lo cual está determinado por sus capacidades innatas (28).
Ericsson et al (28) propusieron un esquema de «práctica deliberada» de tres pasos para mejorar el aprendizaje y el rendimiento: motivación del individuo, retroalimentación inmediata después de la actuación, y la oportunidad de repetir el procedimiento.
Sin embargo, en el aprendizaje neuroquirúrgico hay algunas limitaciones, como las descritas por Marcus et al11: la morbilidad asociada a los errores en los procedimientos, la ausencia de supervisión después de obtener un nivel de rendimiento aceptable y las oportunidades de llevar a cabo un procedimiento.
Dos estudios han discutido estos aspectos de la curva de aprendizaje de la técnica CBT. En primer lugar, Silva y otros (29) describieron su experiencia inicial con la técnica de fusión de la línea media intervertebral lumbar (MIDLIF); en sus primeros 30 pacientes, tuvieron
mejora de la duración del procedimiento a medida que aumentan los casos. Dayani y otros (30) compararon la tasa de complicaciones en el grupo inicial de 52 pacientes con el grupo posterior de 48 pacientes que operaron, mostrando una menor incidencia de ruptura del pedículo medial en este último grupo.
No obstante, creemos que el simulador es útil para comprender el procedimiento, la anatomía, incluido el punto de entrada, y que eventualmente ayudará a evitar complicaciones en el futuro.
Hasta donde sabemos, esta es la primera propuesta de un simulador con la técnica CBT desde su introducción por Santoni y otros (18). En nuestra serie, la tasa de complicaciones relacionadas con la fractura del pedículo fue del 16,6% (4 casos en 24 tornillos insertados).
Nosotros creemos que esto podría estar relacionado con el material del hueso del «sawbone», que es más débil y frágil, especialmente en la parte cortical del pedículo, en comparación con los huesos reales. Además, la fractura o la mala colocación se produjo en los primeros o segundos tornillos, cuando el equipo no estaba familiarizado con la técnica. Con la práctica, estas complicaciones disminuyeron. Sin embargo, en nuestra serie clínica, en el último seguimiento, no detectamos ninguna fractura de pedículo o fallo de hardware en los pacientes.
Al comparar nuestros resultados clínicos con los publicados anteriormente, tenemos una mayor tasa de complicaciones (12,5%, desgarro de la duramdre). En otras series cortas, la tasa de complicaciones clínicas fue ligeramente inferior y varió de 0 a 8,1%. (20). En las series de casos mayores, la tasa de complicaciones varió entre el 5,9% y el 10,1% (30-32).
Durante el período de seguimiento se detectaron dos complicaciones, una pseudoartrosis y una violación de la articulación de la cara superior (►Fig. 4, 3d); sin embargo, hay pruebas de que la TCC es por lo menos igual en la fusión en comparación con los tornillos pediculares y aún mejor en la prevención de la violación de la articulación de la cara (34) Snyder y otros (21) publicaron dos casos de pseudoartrosis y dos fallos de hardware en cuatro pacientes (5%), mientras que Sakaura y otros (35) describieron dos casos de desplazamiento de tornillos (2,1%). En las series de Marengo y otros (33) y Khanna y otros (31) la tasa de complicaciones relacionadas con el fallo del equipo oscilaba entre el 0,7 y el 0,95%. La incisión de nuestra serie es más larga que la de otras series publicadas anteriormente, en las que la longitud media era de unos 5 cm.35,36 En la serie de Lee y otros37 , la longitud media de la incisión de los tornillos pediculares.
Hay algunas limitaciones de nuestro estudio. Aunque nuestra experiencia con el simulador es positiva, sólo hemos tenido un número limitado de oportunidades para realizar tornillos CBT antes de comenzar con la técnica. Sin embargo, hemos visto en el resultado de la prueba PPDI, que los participantes creían que tenían un mejor conocimiento del procedimiento y que había una mejora en el rendimiento. Como se ha descrito anteriormente por Penner y otros (38) , el punto de inserción para la CBT y la anatomía podría ser difícil de identificar, y la simulación, en la que se combinan el modelo anatómico y la neuronavegación, podría facilitar la comprensión y la asimilación de la futura situación intraoperatoria. Además, el diseño retrospectivo del estudio y el número de procedimientos y participantes en el estudio son limitados; sin embargo, consideramos que esta experiencia inicial con la simulación es útil para ayudar a empezar a aplicar la técnica en nuestro departamento.
La simulación ha demostrado su utilidad en el aprendizaje del alumno, (11,39) y pensamos que el simulador que propusimos puede ser útil para mejorar la curva de aprendizaje de la CBT, y obtener resultados satisfactorios durante su implementación en el Departamento de Neurocirugía. Sin embargo, también se han descrito otros sistemas que facilitan la aplicación de la CBT, como la planificación de la CT preoperatoria en 3D (38) y las guías impresas adaptadas al paciente, (40,41) que facilitan la introducción de tornillos y reducen al mínimo las complicaciones.
Referencias
1 Volbers B, Wagner I, Willfarth W, Doerfler A, Schwab S, Staykov D. Intraventricular fibrinolysis does not increase perihemorrhagic edema after intracerebral hemorrhage. Stroke 2013;44(02): 362–366
2 Macdonald RL. Editorial: see one, simulate fifty, then do one? J Neurosurg 2014;121(02):225–227, discussion 226–227
3 Weinstock P, Rehder R, Prabhu SP, Forbes PW, Roussin CJ, Cohen AR. Creation of a novel simulator for minimally invasive neuro- surgery: fusion of 3D printing and special effects. J Neurosurg Pediatr 2017;20(01):1–9
4 Bergeson RK, Schwend RM, DeLucia T, Silva SR, Smith JE, Avilucea FR. How accurately do novice surgeons place thoracic pedicle screws with the free hand technique? Spine 2008;33 (15):E501–E507
5 Ray WZ, Ganju A, Harrop JS, Hoh DJ. Developing an anterior cervical diskectomy and fusion simulator for neurosurgical resi- dent training. Neurosurgery 2013;73(Suppl 1):100–106
6 Krishnaney AA. Incorporating simulators into neurosurgical edu- cation. World Neurosurg 2015;84(06):1527–1529
7 Spicer MA, Apuzzo MLJ. Virtual reality surgery: neurosurgery and the contemporary landscape. Neurosurgery 2003;52(03):489-–497, discussion 496–497
8 Chan S, Conti F, Salisbury K, Blevins NH. Virtual reality simulation in neurosurgery: technologies and evolution. Neurosurgery 2013; 72(Suppl 1):154–164
9 Craven CL, Cooke M, Rangeley C, Alberti SJMM, Murphy M. Developing a pediatric neurosurgical training model. J Neurosurg Pediatr 2018;21(03):329–335
10 Milburn JA, Khera G, Hornby ST, Malone PSC, Fitzgerald JEF. Introduction, availability and role of simulation in surgical edu- cation and training: review of current evidence and recommen- dations from the Association of Surgeons in Training. Int J Surg 2012;10(08):393–398
11 Marcus H, Vakharia V, Kirkman MA, Murphy M, Nandi D. Practice makes perfect? The role of simulation-based deliberate practice and script-based mental rehearsal in the acquisition and mainte- nance of operative neurosurgical skills. Neurosurgery 2013;72 (Suppl 1):124–130
12 Luciano CJ, Banerjee PP, Bellotte B, et al. Learning retention of thoracic pedicle screw placement using a high-resolution aug- mented reality simulator with haptic feedback. Neurosurgery 2011;69(1, Suppl Operative):ons14–ons19, discussion ons19
13 Gragnaniello C, Abou-Hamden A, Mortini P, et al. Complex spine pathology simulator: an innovative tool for advanced spine surgery training. J Neurol Surg A Cent Eur Neurosurg 2016;77 (06):515–522
14 Gasco J, Patel A, Ortega-Barnett J, et al. Virtual reality spine surgery simulation: an empirical study of its usefulness. Neurol Res 2014;36(11):968–973
15 Boody BS, Rosenthal BD, Jenkins TJ, Patel AA, Savage JW, Hsu WK. The effectiveness of bioskills training for simulated open lumbar laminectomy. Global Spine J 2017;7(08):794–800
16 Gonzalvo A, Fitt G, Liew S, et al. The learning curve of pedicle screw placement: how many screws are enough? Spine 2009;34 (21):E761–E765
17 Delgado-Fernández J, Pulido P, García-Pallero MÁ, Blasco G, Frade- Porto N, Sola RG. Image guidance in transdiscal fixation for high- grade spondylolisthesis in adults with correct spinal balance. Neurosurg Focus 2018;44(01):E9
18 Santoni BG, Hynes RA, McGilvray KC, et al. Cortical bone trajectory for lumbar pedicle screws. Spine J 2009;9(05):366–373
19 Dabbous B, Brown D, Tsitlakidis A, Arzoglou V. Clinical outcomes during the learning curve of MIDline Lumbar Fusion (MIDLF®) using the cortical bone trajectory. Acta Neurochir (Wien) 2016; 158(07):1413–1420
20 Delgado-Fernandez J, García-Pallero MÁ, Blasco G, Pulido-Rivas P, Sola RG. Review of cortical bone trajectory: evidence of a new technique. Asian Spine J 2017;11(05):817–831
21 Asamoto S, Kojima K, Winking M, Jödicke A, Ishikawa M, Ishihara S, Deinsberger W, Muto J, Nishiyama M, Asamoto S, et al. Opti- mized Screw Trajectory for Lumbar Cortical Bone Trajectory Pedicle Screws Based on Clinical Outcome: Evidence Favoring the Buttress Effect Theory. J Neurol Surg A Cent Eur Neurosurg 2018 Nov;79(06):464–470
22 Snyder LA, Martinez-Del-Campo E, Neal MT, et al. Lumbar spinal fixation with cortical bone trajectory pedicle screws in 79 patients with degenerative disease: perioperative outcomes and complications. World Neurosurg 2016;88:205–213
23 Brasiliense LBC, Lazaro BCR, Reyes PM, et al. Characteristics of immediate and fatigue strength of a dual-threaded pedicle screw in cadaveric spines. Spine J 2013;13(08):947–956
24 Iwatsuki K, Yoshimine T, Ohnishi Y, Ninomiya K, Ohkawa T. Isthmus-guided cortical bone trajectory for pedicle screw inser- tion. Orthop Surg 2014;6(03):244–248
25 Delgado-Fernández J, Pulido Rivas P, Gil-Simoes R, de Sola RG. How I do it? Lumbar cortical bone trajectory fixation with image- guided neuronavigation. Acta Neurochir (Wien) 2019;161(12): 2423–2428
26 Martin JA, Regehr G, Reznick R, et al. Objective structured assessment of technical skill (OSATS) for surgical residents. Br J Surg 1997;84(02):273–278
27 Fairbank JC, Pynsent PB. The Oswestry Disability Index. Spine 2000;25(22):2940–2952, discussion 2952
28 Ericsson A, Krampe R, Tesch-Romer C. The role of deliberate practice in the aquisition of expert performance. Psychol Rev 1993;100(03):363–406
29 Silva F, Silva PS, Vaz R, Pereira P. Midline lumbar interbody fusion (MIDLIF) with cortical screws: initial experience and learning curve. Acta Neurochir (Wien) 2019;161(12):2415–2420
30 Dayani F, Chen YR, Johnson E, et al. Minimally invasive lumbar pedicle screw fixation using cortical bone trajectory: screw accuracy, complications, and learning curve in 100 screw place- ments. J Clin Neurosci 2019;61:106–111
31 Khanna N, Deol G, Poulter G, Ahuja A. Medialized, muscle- splitting approach for posterior lumbar interbody fusion: tech- nique and multicenter perioperative results. Spine 2016;41(08, Suppl 8):S90–S96
32 Khanna N, Deol G, Poulter G, Ahuja A. Medialized, muscle- splitting approach for posterior lumbar interbody fusion: tech- nique and multicenter perioperative results. Spine (Phila Pa 1976) 2016;41(Suppl 8):S90–S96
33 Marengo N, Berjano P, Cofano F, et al. Cortical bone trajectory screws for circumferential arthrodesis in lumbar degenerative spine: clinical and radiological outcomes of 101 cases. Eur Spine J 2018;27(0123456789, Suppl 2):213–221
34 Lee GW, Son JH, Ahn MW, Kim HJ, Yeom JS. The comparison of pedicle screw and cortical screw in posterior lumbar interbody fusion: a prospective randomized noninferiority trial. Spine J 2015;15(07):1519–1526
35 Sakaura H, Miwa T, Yamashita T, Kuroda Y, Ohwada T. Posterior lumbar interbody fusion with cortical bone trajectory screw fixa- tion versus posterior lumbar interbody fusion using traditional
pedicle screw fixation for degenerative lumbar spondylolisthesis: a comparative study. J Neurosurg Spine 2016;25(05):591–595
36 Hussain I, Virk MS, Link TW, Tsiouris AJ, Elowitz E. Posterior lumbar interbody fusion with 3D-navigation guided cortical bone trajectory screws for L4/5 degenerative spondylolisthesis: 1-year clinical and radiographic outcomes. World Neurosurg 2018;110: e504–e513
37 Lee GW, Shin JH. Comparative study of two surgical techniques for proximal adjacent segment pathology after posterior lumbar interbody fusion with pedicle screws: fusion extension using conventional pedicle screw vs cortical bone trajectory-pedicle screw (cortical screw). World Neurosurg 2018;117:e154–e161
38 Penner F, Marengo N, Ajello M, et al. Preoperative 3D CT planning for cortical bone trajectory screws: a retrospective radiological cohort study. World Neurosurg 2019;126:e1468–e1474
39 Kirkman MA, Ahmed M, Albert AF, Wilson MH, Nandi D, Sevdalis
N. The use of simulation in neurosurgical education and training. A systematic review. J Neurosurg 2014;121(02):228–246
40 Marengo N, Matsukawa K, Monticelli M, et al. Cortical bone trajectory screw placement accuracy with a patient-matched 3- dimensional printed guide in lumbar spinal surgery: a clinical study. World Neurosurg 2019;130:e98–e104
41 Matsukawa K, Kaito T, Abe Y. Accuracy of cortical bone trajectory screw placement using patient-specific template guide system. Neurosurg Rev 2019 (e-pub ahead of print) . Doi: 10.1007/ s10143-019-01140-1


Me han operado de las tres vértebras cervicales hace 6 días me duele en la parte baja un poco más abajo de las cervicales, que puede ser?