Video-charla del Dr. García de Sola sobre el Síndrome de sección medular

Síndrome de sección medular
El Síndrome de sección medular es una de las situaciones más graves de la patología neuroquirúrgica, aunque afortunadamente su frecuencia ha disminuido gracias a las medidas preventivas en el ámbito laboral y del tráfico. Consiste en una lesión a nivel de la médula espinal que interrumpe, total o parcialmente, la transmisión de información entre el cerebro y el resto del cuerpo. Sus consecuencias pueden ser devastadoras: pérdida de fuerza, pérdida de sensibilidad, alteraciones de los esfínteres y de la función sexual, así como un complejo síndrome vegetativo que puede comprometer la vida del paciente.
Para comprender este síndrome es necesario conocer la anatomía y la función de la médula espinal, que se aloja dentro de la columna vertebral y de la que parten las raíces nerviosas que controlan todo el cuerpo. La clínica evoluciona habitualmente en tres fases: una primera de shock medular, otra de recuperación o readaptación, y una última de lesión establecida, completa o incompleta. La causa más frecuente son los traumatismos raquimedulares, principalmente accidentes de tráfico, laborales o deportivos, que afectan sobre todo a varones jóvenes.
El diagnóstico se apoya hoy en medios sofisticados (TAC, resonancia magnética, neurofisiología) y el tratamiento quirúrgico, cuando está indicado, busca descomprimir la médula, estabilizar la columna y corregir la deformidad. Gracias al desarrollo tecnológico —neuronavegador, microscopio, tornillos pediculares, cilindros expandibles y monitorización neurofisiológica intraoperatoria— la columna se aborda hoy con la misma delicadeza y precisión que el cerebro.
Rafael García de Sola
Director de la Cátedra UAM «Innovación en Neurocirugía»
Jefe del Servicio de Neurocirugía
Hospital Ntra. Sra. del Rosario
Madrid
Ver presentación síndrome de sección medular
Introducción al síndrome de sección medular
El Síndrome de sección medular es una situación clínica muy grave que implica una lesión a nivel de la médula espinal. Aunque afortunadamente su frecuencia está disminuyendo —gracias al desarrollo de medidas preventivas en el tráfico, en el ámbito laboral y en el deporte—, sus consecuencias siguen siendo devastadoras y conviene conocerlo bien para comprender su alcance.
Para entender este Síndrome es necesario analizar primero algunos aspectos básicos del funcionamiento de la médula espinal: cómo se organiza, qué estructuras la componen y qué papel desempeña en la transmisión de información entre el cerebro y el resto del cuerpo.
Recuerdo anatomo-funcional de la médula
La columna vertebral y las raíces medulares
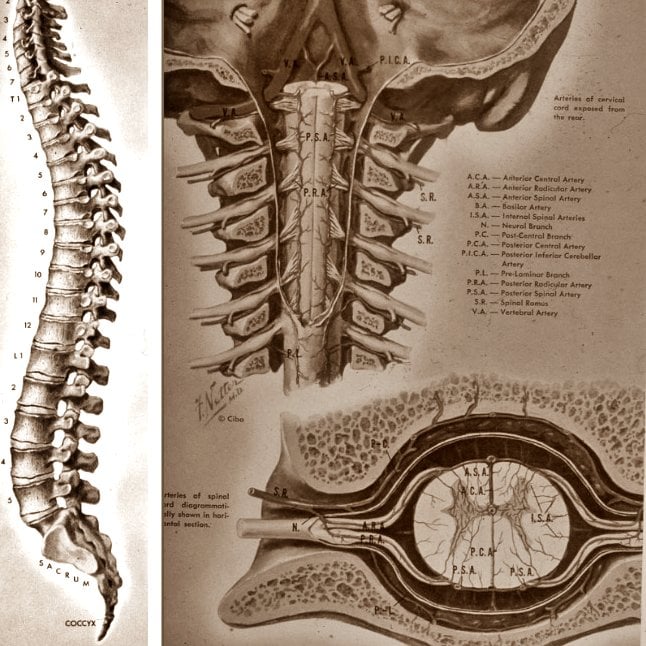
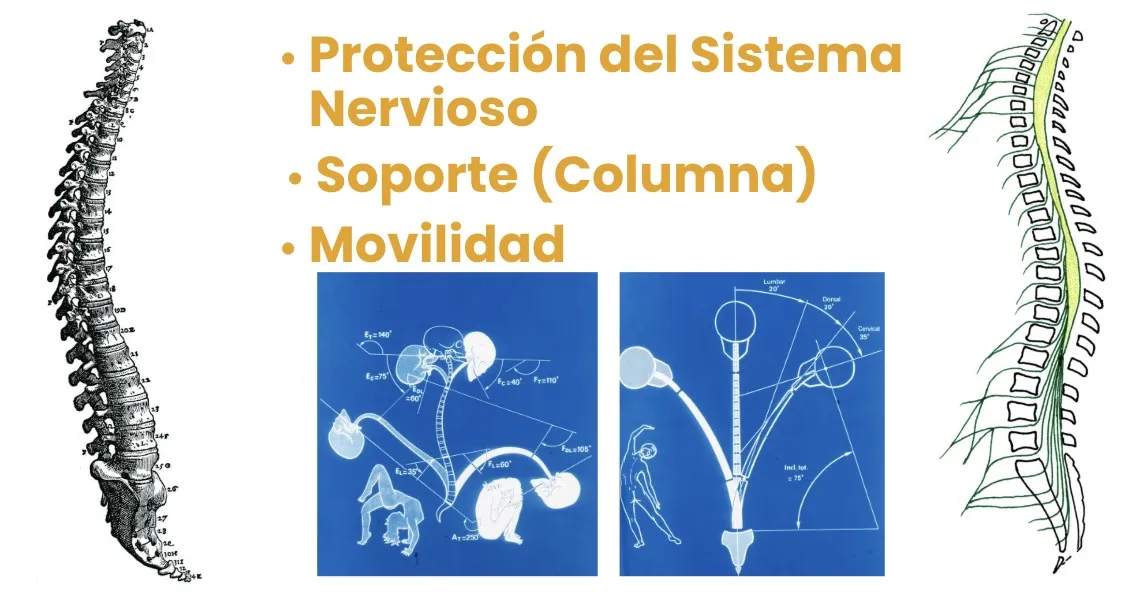
La columna vertebral no solamente sustenta el cuerpo, sino que protege la médula espinal y sus raíces mediante una compleja estructura anatómica. Las raíces medulares, o nervios que salen directamente de la médula, pasan entre dos vértebras por un canal óseo denominado agujero de conjunción. Una vez fuera de la columna, se unen para formar los plexos nerviosos, de los que salen finalmente los nervios periféricos que controlan todo el cuerpo.
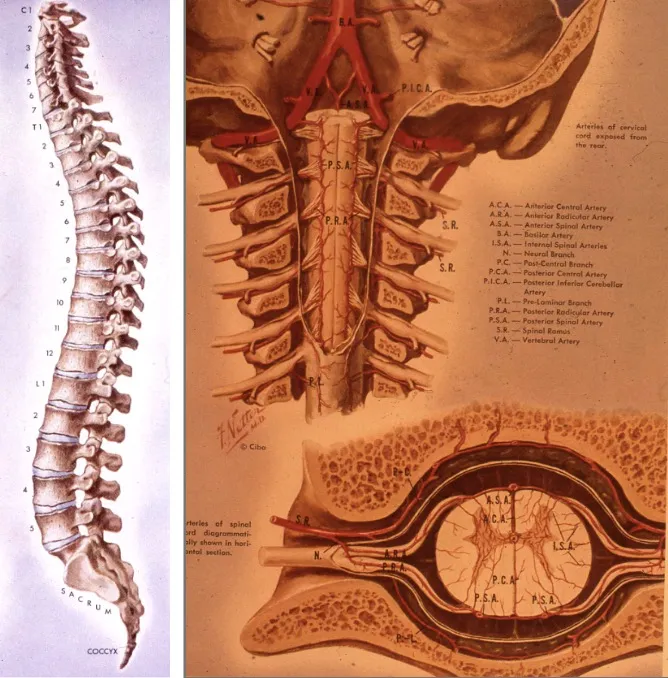
La columna es, por tanto, una estructura muy compleja, con tres funciones principales: aparte del soporte del cuerpo y de la protección del sistema nervioso, tiene que permitir la movilidad de todo el organismo. Esta movilidad exige una arquitectura articulada de múltiples vértebras que se mueven entre sí.
Estructura interna de la médula
Conviene distinguir, muy sucintamente, varias estructuras anatómicas dentro de la médula:
Astas medulares
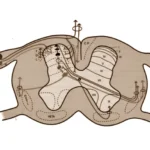
Las neuronas ocupan la zona central medular y se agrupan en formas de astas, visibles en un corte axial:
- Las astas anteriores, más gruesas, contienen las neuronas motoras, que reciben las órdenes procedentes de las neuronas motoras cerebrales.
- Las astas posteriores, más delgadas, son sede de las neuronas sensitivas, que reciben la información del cuerpo a través de los nervios y las raíces y la envían al cerebro.
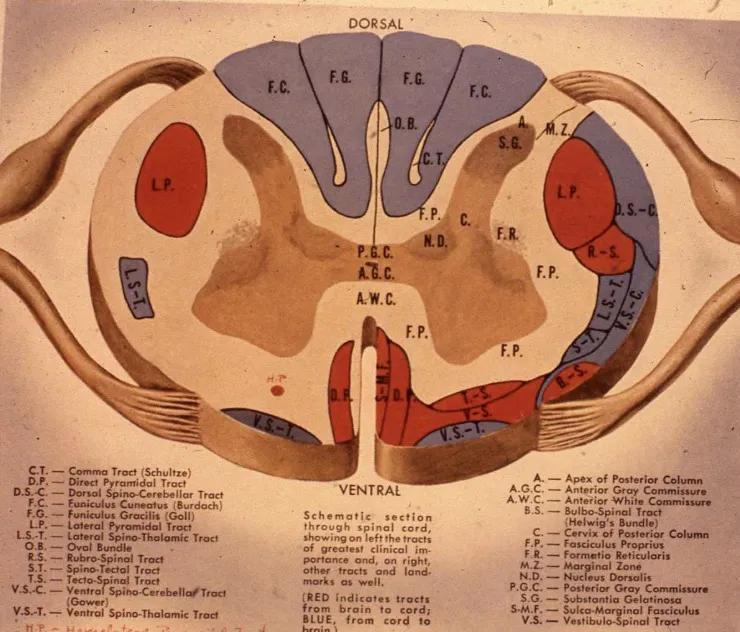
Sustancia blanca
La sustancia blanca se coloca alrededor de las astas. Está formada por las prolongaciones nerviosas (axones), que se agrupan en haces o cordones. Entre ellos destacan tres por su relevancia clínica:
- Cordones posteriores: situados por detrás de las astas, están formados por las prolongaciones axonales de las neuronas sensitivas de las astas posteriores. Llevan la sensibilidad profunda —que nos informa de la posición de las diferentes partes del cuerpo— así como la sensibilidad cutánea menos específica.
- Haz espino-talámico lateral: se sitúa en el cordón antero-lateral medular, por fuera de las astas anteriores. Está formado por prolongaciones de las neuronas sensitivas de las astas posteriores que cruzan por el centro de la médula hacia el lado contrario.
- Haz piramidal (o vía cortico-espinal): se localiza en la parte posterior y lateral. Es el conjunto de prolongaciones axonales de las neuronas motoras corticales cerebrales, que conectan con las neuronas motoras de las astas anteriores del mismo lado en que se encuentra el haz. Su nombre viene de la forma de pirámide de las neuronas corticales cerebrales que lo originan.
Las raíces medulares en detalle
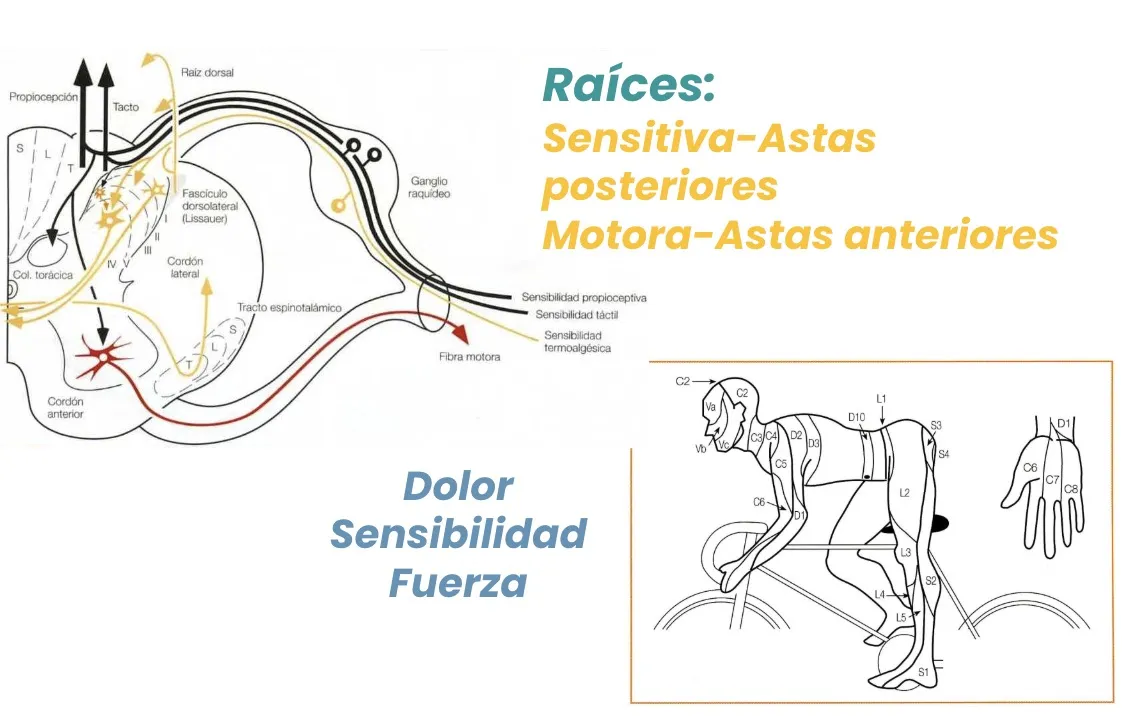
Las raíces salen de la médula por su parte lateral: una raíz anterior y otra posterior, que se unen antes de salir del agujero de conjunción.
- Las raíces posteriores traen información sensitiva procedente de los nervios. Disponen de una estación intermedia, el ganglio raquídeo, donde se localizan neuronas que emiten una prolongación para conectar con las neuronas sensitivas de las astas posteriores medulares. La zona del cuerpo de la que reciben información se denomina dermatoma.
- Las raíces anteriores están formadas por las prolongaciones de las neuronas motoras de las astas anteriores.
La unión de ambas raíces forma el nervio raquídeo, que sale del agujero de conjunción. Existe cierta confusión terminológica, ya que también se le denomina «raíz». Este nervio raquídeo lleva tres tipos de fibras: del dolor (sin protección mielínica), sensitivas (con baja protección mielínica) y motoras (con alta protección mielínica).
Vías sensitivas ascendentes
La información sensitiva que llega al cerebro, concretamente al lóbulo parietal, viaja por dos sistemas principales.
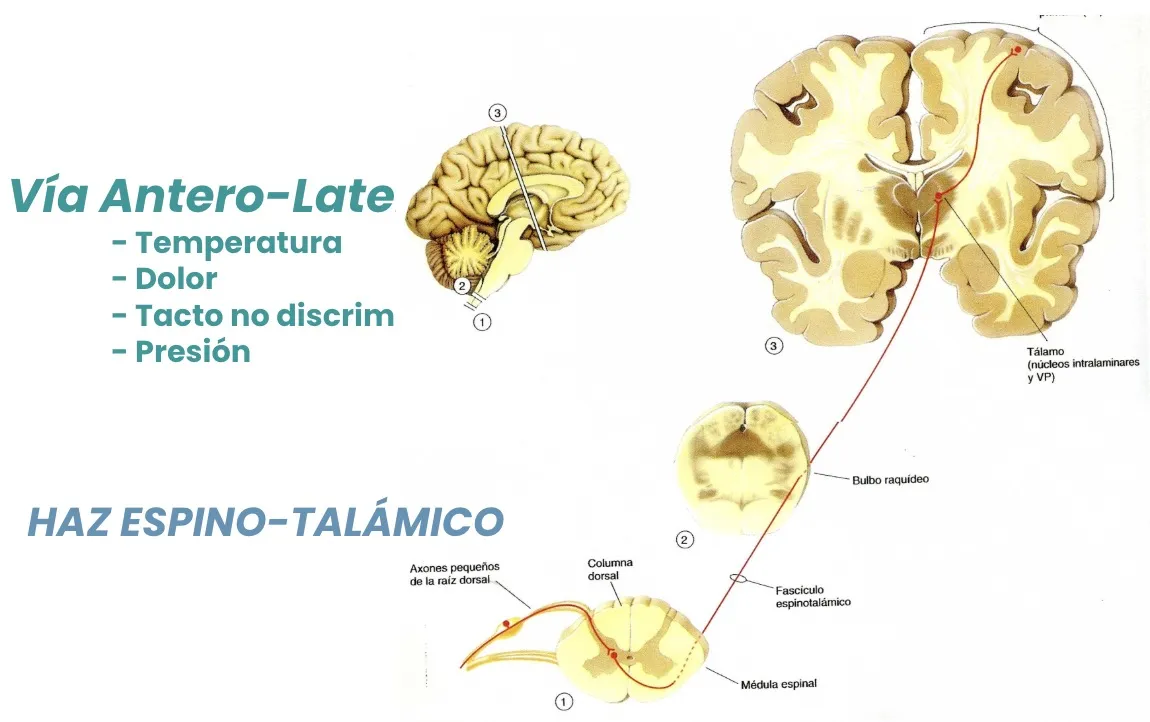
Vía antero-lateral: el haz espino-talámico
La primera vía es la que discurre por el cordón antero-lateral: el haz espino-talámico. Se forma con las prolongaciones de las neuronas situadas en las astas posteriores, que emiten sus axones cruzándolos casi al mismo nivel hacia el lado contrario de la médula.
Una sección a nivel medular de este haz impide que llegue al cerebro la información sensitiva relativa al dolor y la temperatura por debajo de la lesión y en el lado contralateral. Esta vía transporta también el tacto no discriminativo y la presión.
Cordones posteriores
El segundo gran sistema de información sensitiva se estructura en los cordones posteriores medulares. Está formado por las prolongaciones de las neuronas sensitivas de las astas posteriores del mismo lado. Estos haces se dirigen hacia la misma región cerebral parietal, pero a nivel del tronco cerebral es donde se produce su cruce.
Una sección de estos cordones a nivel medular provocará pérdida de la sensibilidad profunda (posición) y del tacto discriminativo fino en el mismo lado de la sección medular. En cambio, una lesión a nivel talámico o parietal condicionará una pérdida de este tipo de sensibilidad en el lado contrario del cuerpo.
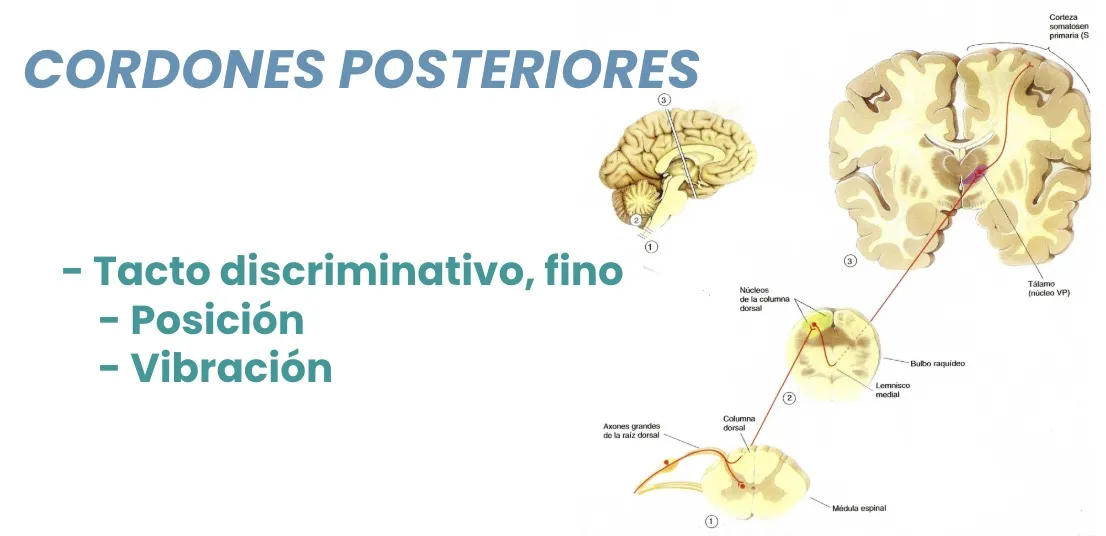
Vía motora: el haz piramidal
En el cordón póstero-lateral medular se encuentra el haz piramidal o vía cortico-espinal. Lleva las prolongaciones de las neuronas motoras —denominadas piramidales por su forma— que se localizan en la parte más posterior del lóbulo frontal cerebral.
Estos haces de fibras motoras descienden y se cruzan a nivel del tronco cerebral, hasta conectar con las neuronas motoras de las astas anteriores medulares. Una sección de este haz, a nivel medular, provocará la pérdida de fuerza por debajo y en el mismo lado de la sección. Sin embargo, una lesión a nivel del tronco cerebral, tálamo o corteza cerebral generará una pérdida de fuerza en el lado contralateral.
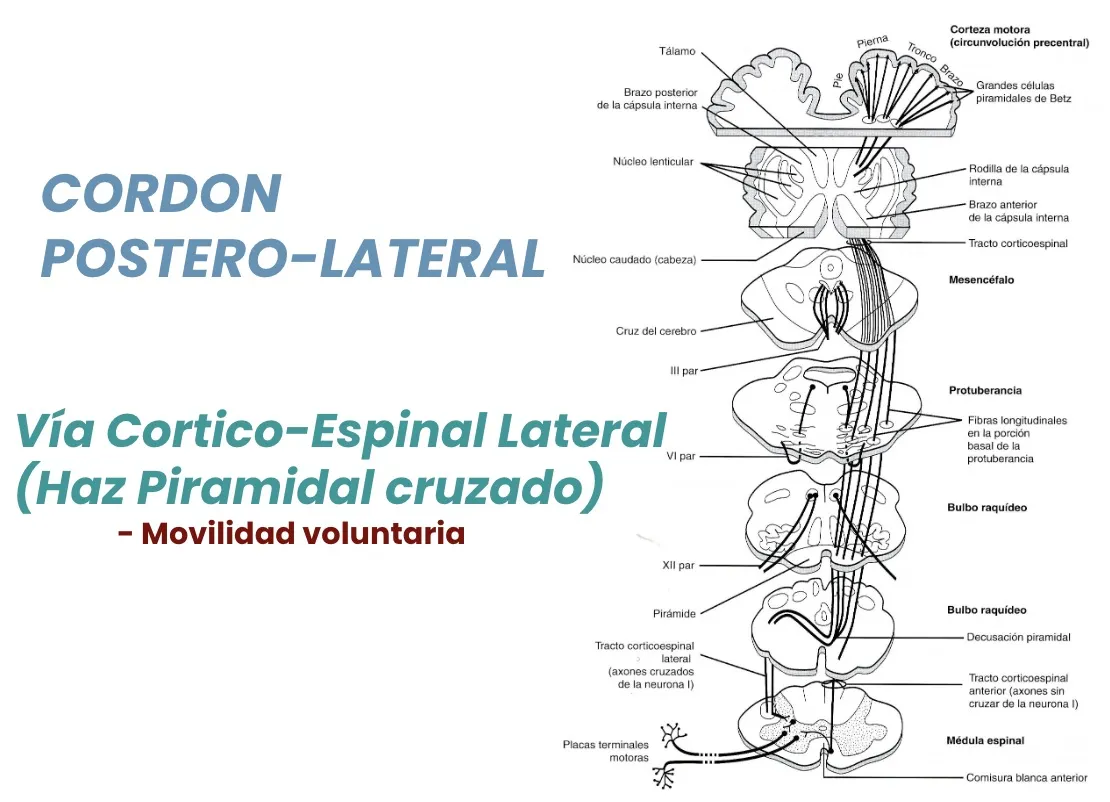
Control de esfínteres
A nivel medular bajo se encuentran los circuitos que controlan los esfínteres. Su lesión provoca un mal control esfinteriano, con urgencia urinaria, retención progresiva hasta que la vejiga se llena y se orina por rebosamiento, así como una importante tendencia al estreñimiento.
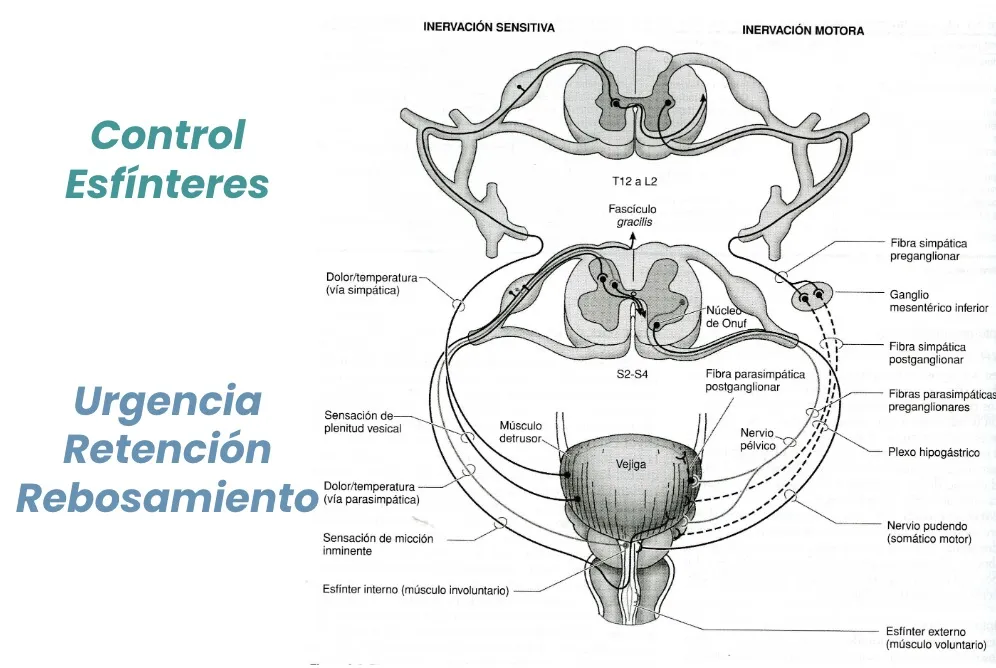
Función sexual y sistema nervioso autónomo
Hay que tener en cuenta también que, a nivel del cono medular, se sitúan neuronas que forman parte de los circuitos que controlan la función sexual. En esa misma región se encuentra asimismo el sistema nervioso autónomo parasimpático.
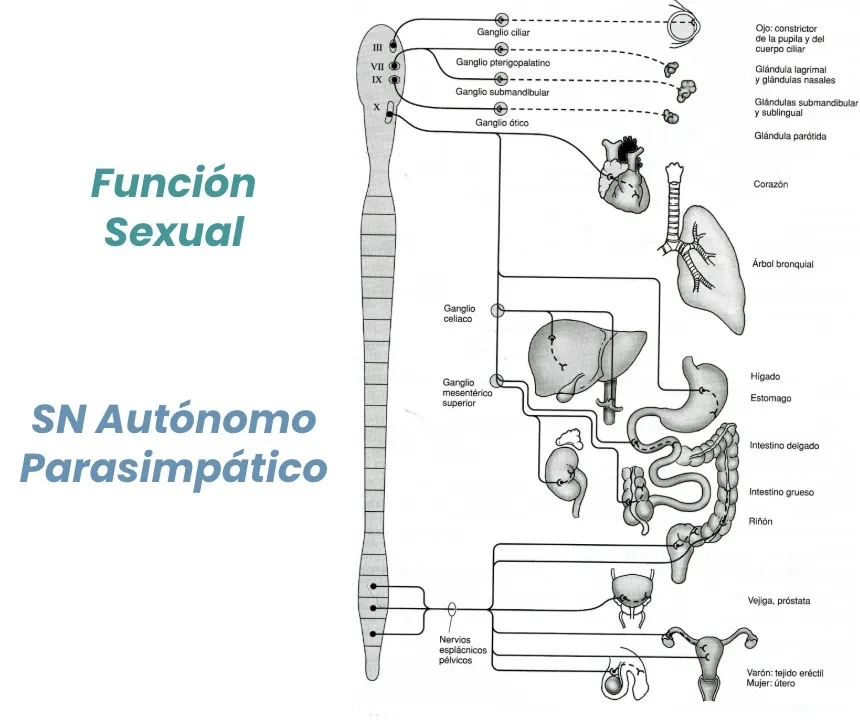
Fisiopatología de la sección medular
Tras esta visión del funcionamiento normal de la médula, conviene analizar la situación que se produce si una noxa o accidente provoca su sección en un punto determinado.
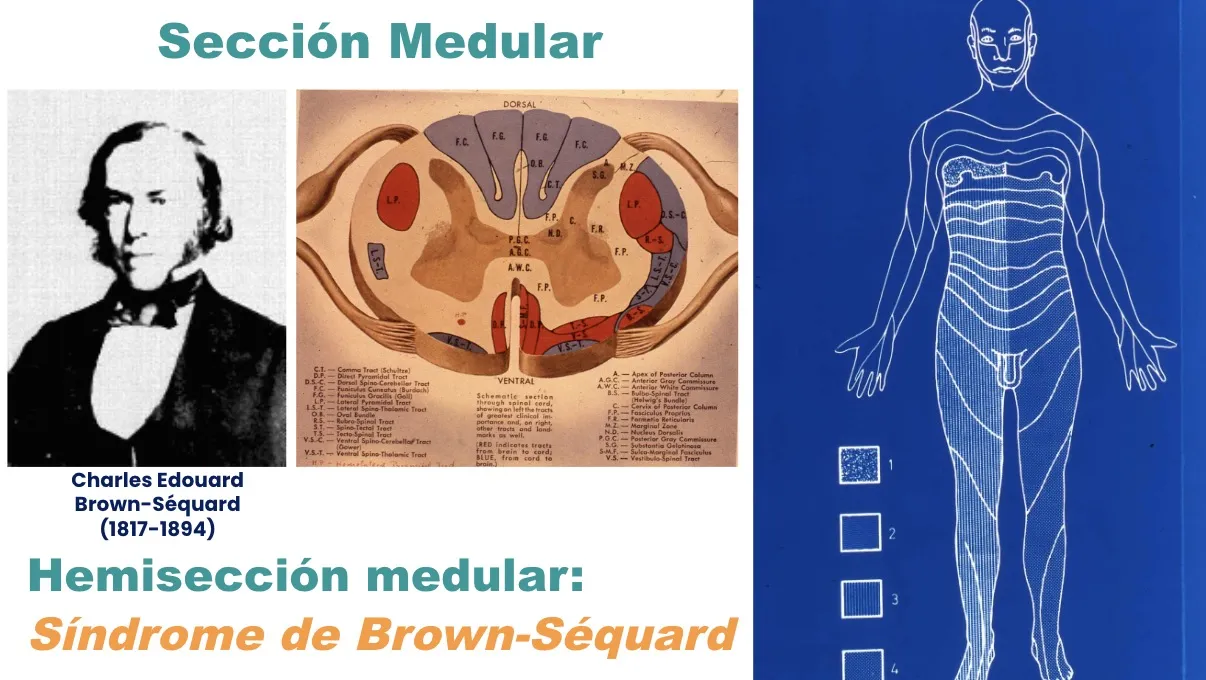
El síndrome de Brown-Séquard
Fue Charles Edouard Brown-Séquard (1817-1894) quien describió el síndrome que lleva su nombre, la hemisección medular, observado al realizar este tipo de lesión en el laboratorio.
En este síndrome se produce:
- Una parálisis ipsilateral, en el mismo lado de la lesión.
- Pérdida del tacto discriminativo y de la sensibilidad posicional también en el mismo lado.
- En el lado contrario, una falta de sensación dolorosa, térmica y táctil.
Clínica de la sección medular
Dependiendo del tipo de sección medular pueden aparecer varias situaciones clínicas. A continuación se analizan las más frecuentes.
Las tres fases evolutivas
Ante una agresión aguda medular, la clínica suele cursar en varias fases:
- I. Shock medular: lo primero que ocurre es una clínica de shock medular. La médula deja de responder, como le ocurre al cerebro cuando sufre un traumatismo craneal. Esta situación dura entre 3 días y 3 semanas.
- II. Recuperación: a continuación se va recuperando la función medular, de forma completa o parcial.
- III. Lesión establecida: en algunos casos queda una situación estable de lesión medular, también completa o incompleta. Por ejemplo, el síndrome de hemisección medular o de Brown-Séquard es una lesión establecida incompleta.
I. Shock medular
La fase de shock medular es similar a la fase del impacto en el caso de los traumatismos craneoencefálicos. Se produce un cese de función medular que posteriormente se va recuperando, consiguiendo la médula autonomía respecto al encéfalo o reiniciándose de nuevo la conexión. Es importante destacar que nada en el estadio de shock permite asegurar que no se va a recuperar la función medular.
Desde el lugar del impacto hacia abajo se manifiesta:
- Pérdida de fuerza: plejía flácida con reflejos abolidos.
- Pérdida de sensibilidad: anestesia y analgesia.
- Pérdida de los reflejos cutáneos.
- Un complejo síndrome vegetativo, cuya gravedad puede condicionar la evolución.
El síndrome vegetativo
Este síndrome vegetativo es una situación grave que puede hacer perder la vida al paciente. Presenta manifestaciones pulmonares, cardiocirculatorias, abdominales y de esfínteres:
- Alteraciones pulmonares, que pueden llegar a edema agudo de pulmón.
- Trastornos vasomotores: hipotensión arterial, inestabilidad térmica y úlceras cutáneas.
- Alteraciones abdominales: íleo paralítico, con detención del tránsito intestinal.
- Alteraciones de esfínteres: retención vesical con distensión y globo vesical, y estreñimiento.
Las dos primeras —pulmonares y cardiocirculatorias— deben atenderse de forma prioritaria, sin descuidar la prevención y manejo de las dos siguientes.
II. Fase de recuperación y readaptación
Pasada la fase de shock medular, la médula tiende a estabilizarse y a recuperarse. Pueden darse dos escenarios:
IIA. Evolución favorable
El resultado puede ser favorable, recuperándose la función más o menos íntegramente: el paciente va recuperando de forma progresiva la sensibilidad, los reflejos, la fuerza y la movilidad.
IIB. Evolución no favorable
En otras ocasiones, con traumatismos más graves, quedan lesiones permanentes, completas o incompletas. Esto supone pérdida de fuerza, anestesia, alteraciones tróficas y dolor grave.
Es interesante destacar que la médula, al dejar de estar conectada con el encéfalo, funciona de forma autónoma con circuitos entre sus propias neuronas motoras y sensitivas. La consecuencia es que la 2ª neurona medular recupera su función y se hace independiente de la 1ª neurona, pero el movimiento no es controlable ni consciente. Queda entonces una plejía espástica (mono, para, tri o tetraplejía, según el nivel y extensión), por afectación de la vía piramidal o de la 1ª neurona, con aumento de los reflejos, además de anestesia, alteraciones tróficas y de esfínteres, y dolor por desaferentización.
III. Fase de lesión establecida
IIIA. Sección medular completa
Si la médula ha sido seccionada completamente, la clínica es de pérdida completa de la movilidad, con:
- Para o tetraplejía espástica, en función del nivel de la lesión.
- Hiperreflexia por debajo del nivel lesional.
- Anestesia por debajo del nivel de sección.
- Alteraciones vesicales: retención.
- Alteraciones intestinales: estreñimiento.
- Alteraciones tróficas: úlceras de decúbito.
- Dolor neuropático o por desaferentización, de tratamiento muy difícil.
IIIB. Sección medular incompleta
Si la sección es incompleta, pueden darse varios cuadros, entre los que destaca el síndrome de hemisección medular. Las principales presentaciones son:
- Hemisección medular o síndrome de Brown-Séquard.
- Síndrome centromedular de Schneider.
- Síndrome medular anterior.
- Síndrome medular posterior (de Dejerine y Roussy).
El síndrome de Brown-Séquard
En este síndrome —relacionado con frecuencia con traumatismos penetrantes— se presentan tres signos cardinales:
- A.- Una parálisis ipsilateral.
- B.- Una pérdida de la sensibilidad al dolor y la temperatura contralateral.
- C.- Una pérdida de la sensibilidad profunda ipsilateral (cómo está colocado el miembro, los dedos, etc., en el mismo lado de la lesión).
Escalas clínicas de diagnóstico
Desde el punto de vista clínico existen numerosas escalas para valorar la situación del paciente en cada momento. Sirven para evaluar la evolución espontánea o la respuesta al tratamiento quirúrgico. Las dos más utilizadas son la escala de Frankel y la escala de ASIA, que clasifican las lesiones desde la afectación más grave (grado A) hasta la función conservada (grado E).
| Grado | Escala de Frankel | Escala de ASIA |
|---|---|---|
| A | Afectación completa sensitivo-motora | Afectación completa sensitivo-motora |
| B | Afectación motora completa. Sensibilidad conservada por debajo de la lesión | Afectación motora completa. Afectación sensitiva incompleta con preservación de zona sacra |
| C | Afectación motora incompleta pero no funcionante | Lesión medular incompleta sensitivo-motora con menos del 50% de los músculos claves por debajo del nivel lesional. Balance muscular < 3/5 |
| D | Afectación motora incompleta con funcionalidad | Afectación motora incompleta con más del 50% de los músculos claves por debajo del nivel lesional. Balance muscular > 3/5 |
| E | Recuperación total de la función motora y sensitiva | Función motora y sensitiva normal |
Traumatismos raquimedulares
La causa más frecuente del síndrome de sección medular son los traumatismos vertebro-medulares o raquimedulares.
Etiología
Las causas de estas lesiones son muy variadas, desde los accidentes de tráfico hasta complicaciones quirúrgicas de otros procesos:
- Accidentes de tráfico.
- Accidentes laborales.
- Accidentes deportivos.
- Agresiones.
- Caídas.
- Esfuerzos.
- Complicaciones quirúrgicas.
Incidencia
Como ya se ha referido, los traumatismos raquimedulares han disminuido en frecuencia. La principal razón es el progreso en las medidas de precaución en los vehículos, que reducen la gravedad de los accidentes de tráfico, así como las medidas tomadas en el lugar de trabajo. Su incidencia es, por tanto, proporcional al grado de desarrollo industrial de una sociedad.
Las vértebras con mayor riesgo de fracturarse o luxarse son:
- Cervicales (en primer lugar): 1ª y 2ª vértebras (atlas y axis) y 4ª a 6ª vértebras cervicales.
- Transición tóraco-lumbar (D11 a L2).
El perfil epidemiológico característico corresponde a varones jóvenes, especialmente entre los 20 y 30 años.
Mortalidad y morbilidad
Los traumatismos raquimedulares conllevan un alto porcentaje de morbimortalidad, situado entre el 5 y el 20%, siendo significativamente peor en las vértebras cervicales superiores. Aparte de la incidencia directa sobre la columna vertebral, el accidente puede provocar otras lesiones múltiples que agravan la situación clínica del paciente.
Fisiopatología de la fractura vertebral
La causa más frecuente de lesión medular es la rotura de la columna provocada por una fractura vertebral. Estas fracturas pueden producirse por varios mecanismos.
Mecanismos de fractura
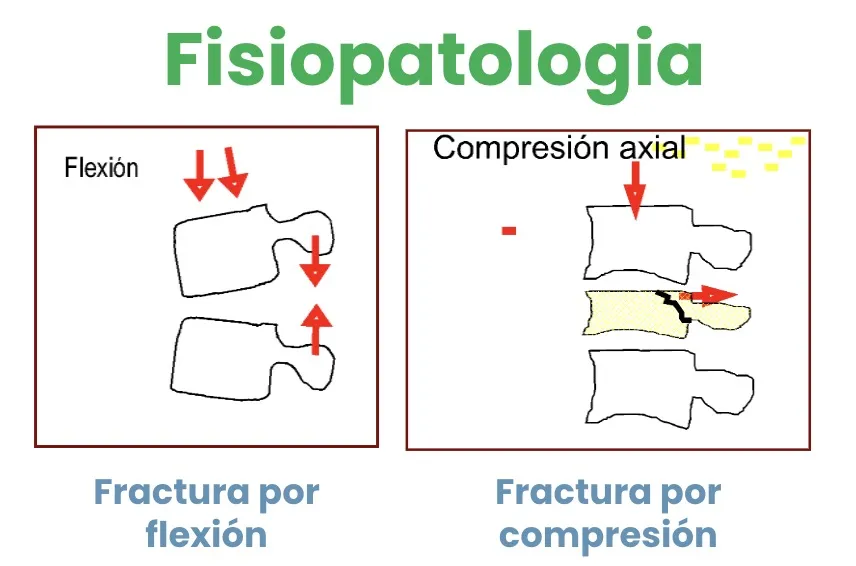
Los mecanismos básicos son dos:
- 1. Fractura por flexión: es la más frecuente.
- 2. Fractura por compresión: típica, por ejemplo, de las caídas sobre el fondo de una piscina.
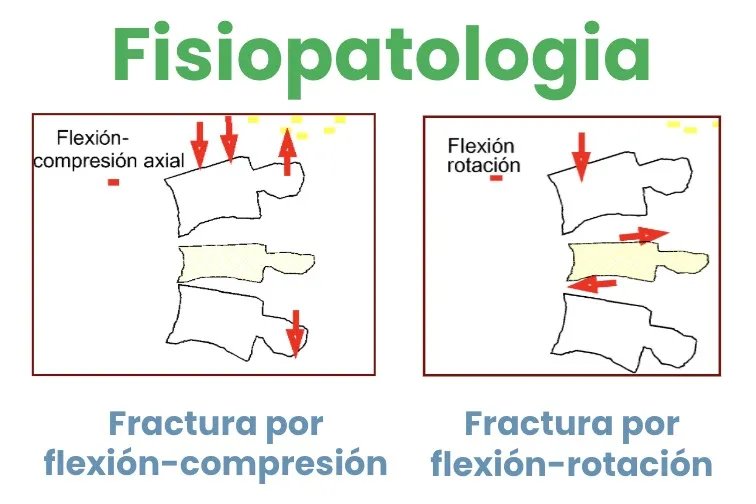
Existen mecanismos aún más graves, en los que se combinan varios movimientos:
- 3. Fractura por flexión-compresión.
- 4. Fractura por flexión-rotación.
En estos casos no solo se fractura la vértebra en alguno de sus componentes, sino que también se produce rotura o dislaceración del sistema ligamentoso. Esto aumenta la inestabilidad del segmento afectado y el riesgo de compresión-sección medular.
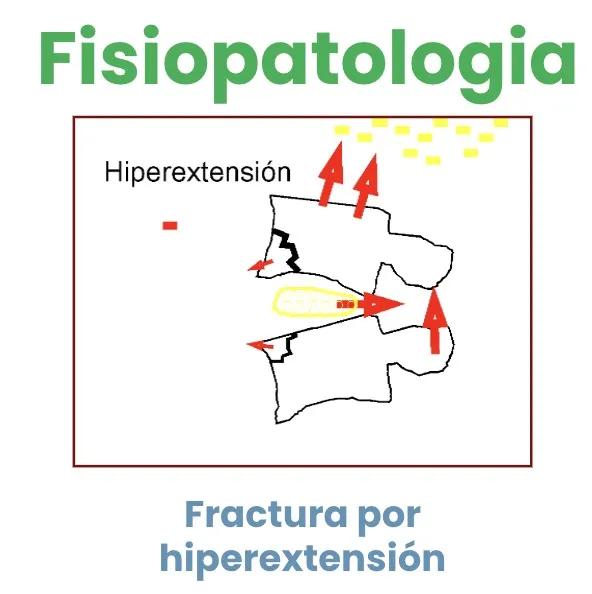
Existe un cuarto mecanismo, mucho más infrecuente:
- 5. Fractura por hiperextensión: posible, aunque rara.
Fenómenos derivados del traumatismo
De acuerdo con todo lo anterior, tras el accidente se producen varios fenómenos.
1. Inestabilidad
En primer lugar, se produce una pérdida de la estabilidad, que se manifiesta como:
- Pérdida de alineación vertebral, que puede llegar a cifosis traumática.
- Dolor.
- Lesión neurológica por compresión-sección medular aguda.
2. Lesión medular
El tipo de lesión medular se asemeja a la clasificación de las lesiones traumáticas cerebrales:
- 2A. Conmoción: sin lesión anatomopatológica; recuperable, cede en 24 horas.
- 2B. Contusión: nivel más grave; existe lesión anatomopatológica, aunque se mantiene la continuidad anatómica.
- 2C. Transección medular: pérdida clara de continuidad anatómica, completa o incompleta.
3. Lesión extramedular
Además, la afectación de los cuerpos vertebrales y estructuras anexas puede provocar otros tipos de lesiones, fundamentalmente hemorrágicas, o incidir sobre el recorrido de las raíces medulares:
- Hemorragias: subaracnoidea, subdural y extradural.
- Lesiones radiculares, frecuentemente por fragmentos óseos desplazados.
4. Lesiones secundarias
Dependiendo de la lesión medular y de su proceso de reparación espontánea, pueden quedar como secuelas varias situaciones clínicas, destacando:
- Siringomielia postraumática: aparición de un quiste dentro de la médula con tendencia a crecer con el tiempo.
- Mielopatía por aracnoiditis.
- Mielopatía por estenosis.
Estas secuelas pueden entorpecer la evolución clínica o incluso empeorarla con el paso del tiempo.
Clínica y diagnóstico de los traumatismos raquimedulares
Manifestaciones clínicas
En relación con la clínica, los síntomas y signos dependen de varios factores:
- Intensidad del traumatismo.
- Topografía: lugar de incidencia en la columna-médula.
- Extensión de las lesiones.
Los principales síntomas de la sección completa o incompleta medular ya se han descrito en los apartados anteriores sobre las distintas fases clínicas.
Diagnóstico
Para realizar un correcto diagnóstico de la situación post-traumática se dispone hoy de muchas facilidades:
- Rx (radiografía simple): a pesar de ser básica, conserva un alto valor por la facilidad de realizarla en la propia cama del paciente, en urgencia y sin moverlo.
- TAC (Tomografía Axial Computarizada): es la prueba fundamental y prioritaria, ya que permite ver el hueso y deducir la posible afectación del canal vertebral.
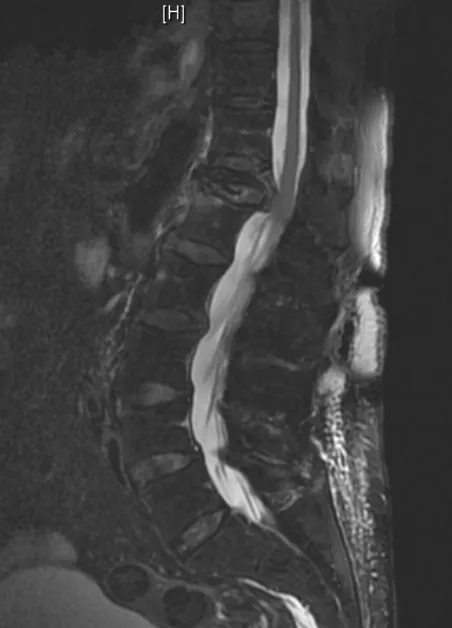
- RM (Resonancia Magnética): más compleja y no siempre indicada de forma urgente, aporta información detallada del tejido medular.
- NFL (Neurofisiología): los estudios funcionales determinan con gran seguridad el resultado de la lesión y orientan sobre su evolución.
Lesiones cervicales
Las vértebras cervicales son las más expuestas, debido a la gran movilidad de la zona y a que la cabeza pesa considerablemente sobre una columna que no está defendida por una caja como ocurre en el tórax.
Luxación atlo-axoidea
A nivel de las primeras vértebras cervicales —atlas y axis— pueden producirse luxaciones o fracturas que comprometen la estabilidad y, eventualmente, la médula.
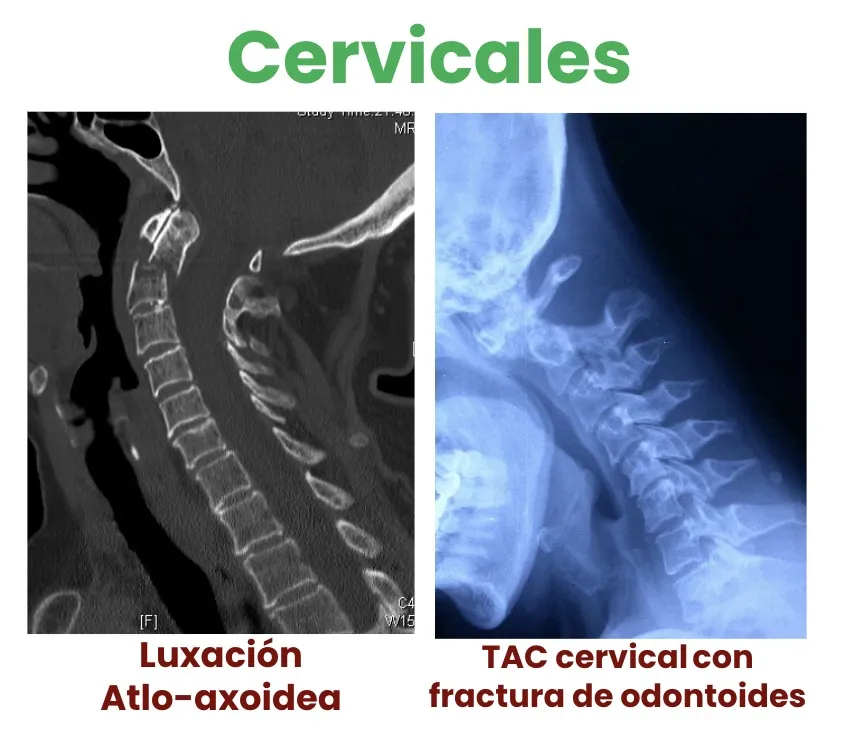
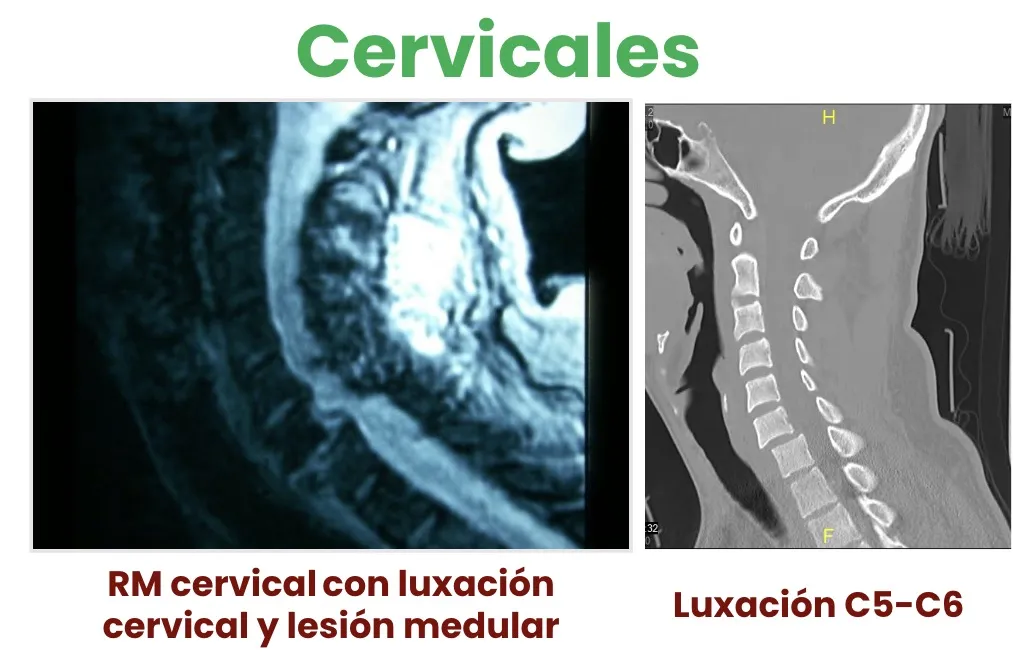
Luxación C5-C6
A nivel de las vértebras C3 a C7, los desplazamientos pueden incidir directamente sobre la médula, produciendo lesión medular asociada.
Esguince cervical o latigazo
Merece mención específica el síndrome de esguince cervical, también conocido como latigazo cervical. Es una patología que genera dolor, bajas laborales y litigios con gran frecuencia. Se produce por un mecanismo de flexión-extensión, aceleración y desaceleración, muy típico en accidentes de tráfico con golpe trasero.
- Se presenta con dolor cervical que puede prolongarse varias semanas.
- En la Rx y RM no se perciben lesiones estructurales.
- El tratamiento aconsejado es reposo cervical con collarín durante 1-2 semanas.
Lesiones torácicas
A nivel torácico es necesaria una mayor intensidad del agente traumático, ya que las vértebras están protegidas por la caja torácica, que limita los movimientos del segmento. Las lesiones torácicas son por ello más raras pero, cuando se producen, suelen suponer un trauma de mayor energía.
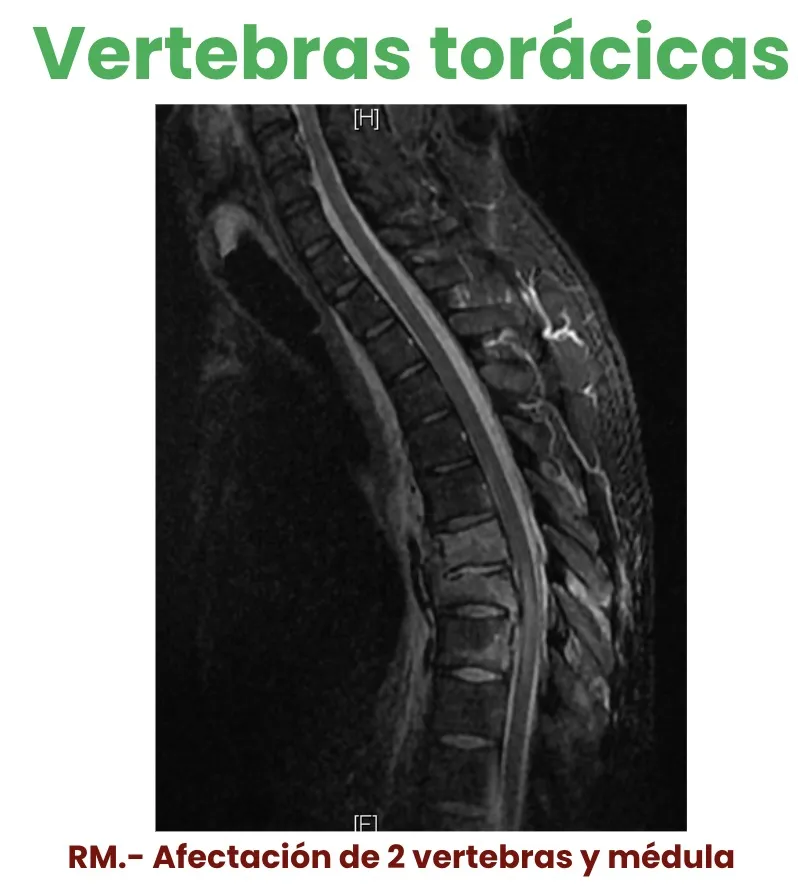
Lesiones lumbares
A nivel lumbar, debido a la mayor movilidad de la zona, es más frecuente la aparición de fracturas, sobre todo en la transición tóraco-abdominal. Toda la caja torácica puede «cimbrear» sobre la columna lumbar, lo que provoca fracturas a veces realmente violentas, con fragmentos óseos que pueden introducirse en el canal vertebral.
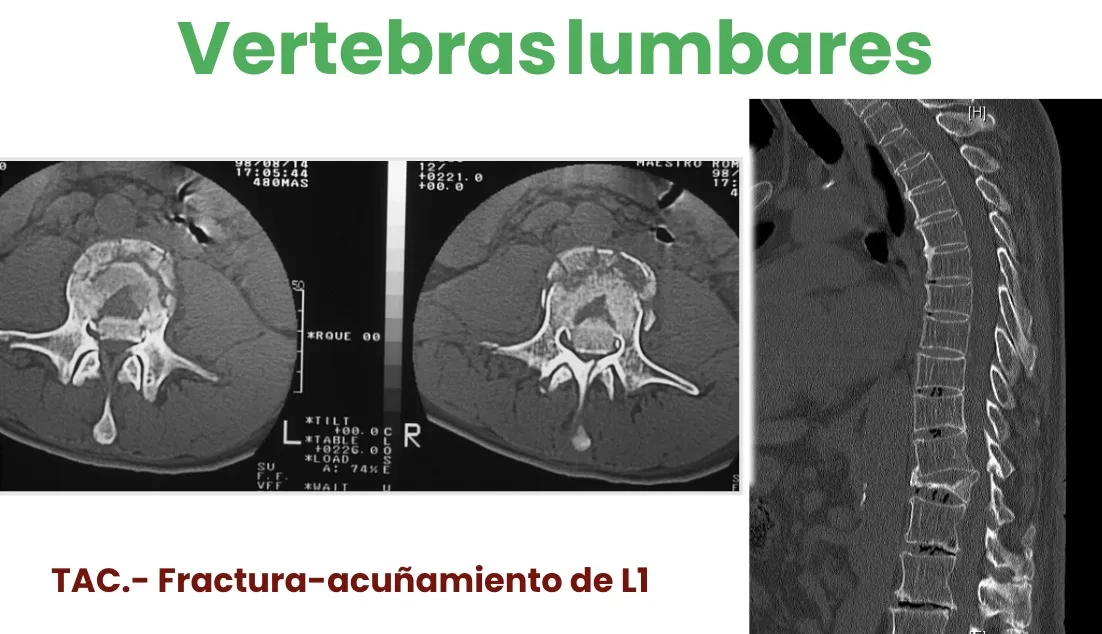
Fracturas de vértebras osteoporóticas
Otro aspecto importante son las fracturas de vértebras osteoporóticas, sobre las que existe una charla específica en esta misma web. En este tipo de fracturas:
- La energía del agente traumático suele ser mucho menor. A veces basta un pequeño esfuerzo o incluso una tos.
- Suelen producirse por mecanismo de compresión.
- Afortunadamente, no es frecuente que afecten al canal medular y, por tanto, raramente generan lesión neurológica, aunque sí dolor.

Tratamiento de la fractura vertebral y de la lesión medular
Tratamiento de la fractura vertebral
El tratamiento de una fractura vertebral sigue las reglas generales del tratamiento de cualquier fractura ósea:
- 1. Inmovilización.
- 2. Reducción y mejora del alineamiento de la columna.
- 3. Fijación-fusión, ya sea espontánea (si la postura permite que la fractura consolide) o quirúrgica.
Tratamiento de la lesión medular
Conjuntamente con el tratamiento de la fractura, hay que poner en marcha las medidas para el tratamiento adecuado de la lesión medular. Desde el primer momento, en urgencias, es necesario actuar sobre varios frentes:
- 1. Edema medular.
- 2. Alteraciones respiratorias: estabilizar al paciente, evitando las complicaciones respiratorias.
- 3. Alteraciones cardíacas-circulatorias: prevenir las complicaciones cardiovasculares antes comentadas.
- 4. Alteraciones esfinterianas: prevenir los problemas derivados de la malfunción de los esfínteres.
- 5. Úlceras de decúbito: prevenir las alteraciones tróficas.
Una vez superada la situación de urgencia, el paciente debe continuar la rehabilitación en centros especializados, para conseguir la mayor calidad de vida posible.
Tratamiento quirúrgico
Para el tratamiento quirúrgico de las lesiones raquimedulares se dispone hoy día de medios muy sofisticados, fruto de un desarrollo tecnológico extraordinario.
Objetivos del tratamiento quirúrgico
El objetivo de la cirugía es múltiple:
- Descomprimir la médula, retirando los fragmentos óseos que contacten con ella.
- Mantener o conseguir la estabilidad de la columna.
- Corregir la deformidad, si la hay.
- Tratar de alcanzar el mayor grado posible de recuperación funcional.
Funciones comprometidas
En el diseño de la intervención hay que tener en cuenta tres factores que alteran las funciones esenciales de la columna vertebral:
- Inestabilidad y deformidad.
- Compresión del sistema nervioso.
- Movilidad y rigidez.
Medios técnicos para la cirugía de columna
A continuación se realiza un breve recorrido por los medios disponibles hoy día para la cirugía de columna.
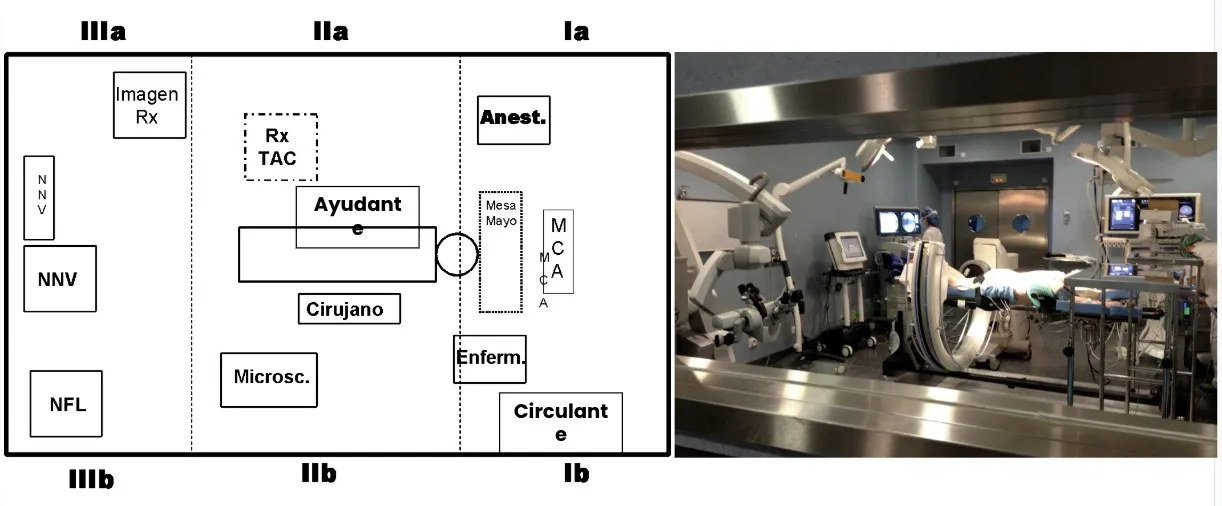
El quirófano
En relación con el quirófano, se ha conseguido un alto nivel de complejidad tecnológica, junto con una gran armonización entre un equipamiento muy sofisticado y el personal entrenado (ayudante, instrumentista, circulante, anestesia, neurofisiólogo), que trabajan de forma coordinada y eficiente.
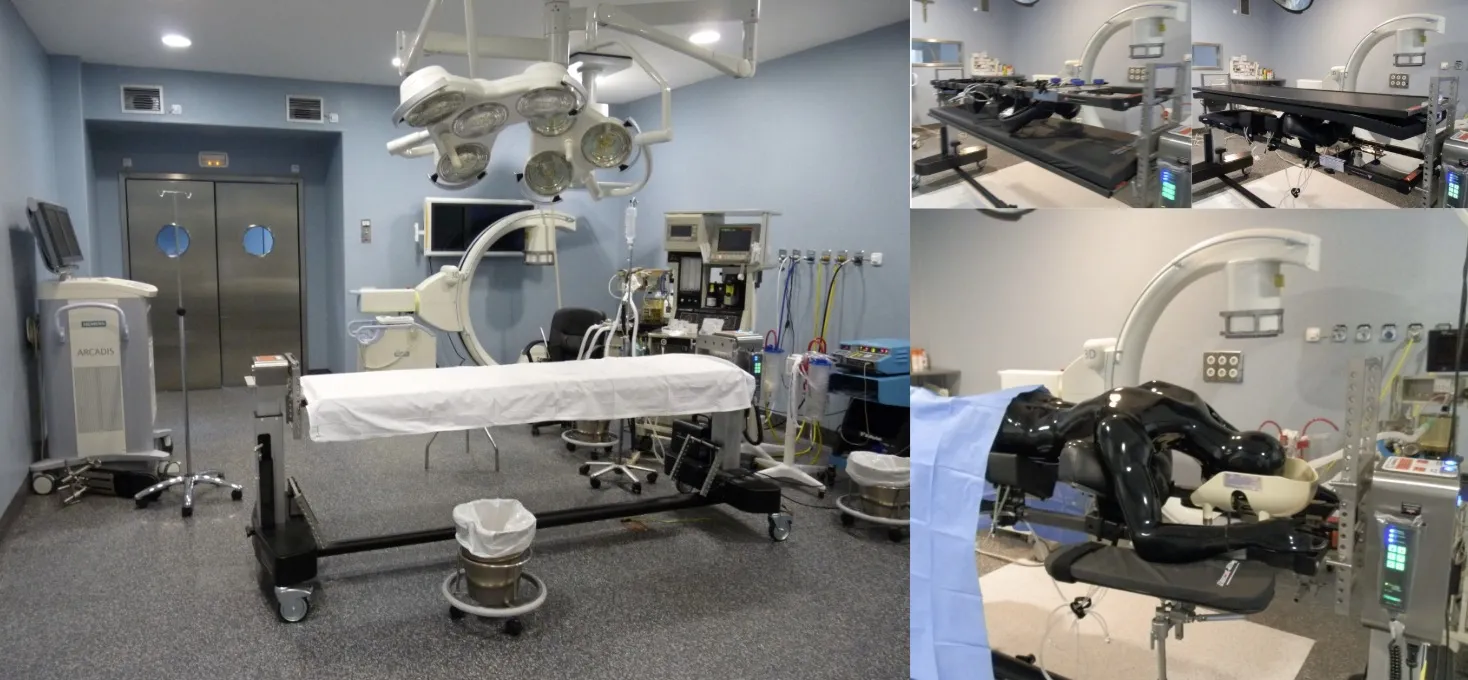
Mesa quirúrgica: la mesa de Jackson
La mesa de quirófano empleada en cirugía de columna es muy especial. Se trata de una mesa específica diseñada para esta cirugía, contemplando entre otros aspectos la situación grave de inestabilidad de las fracturas vertebrales. Se denomina mesa de Jackson y está fabricada en fibra de carbono, para no interferir con la exploración radiológica (Rx, TAC, etc.).
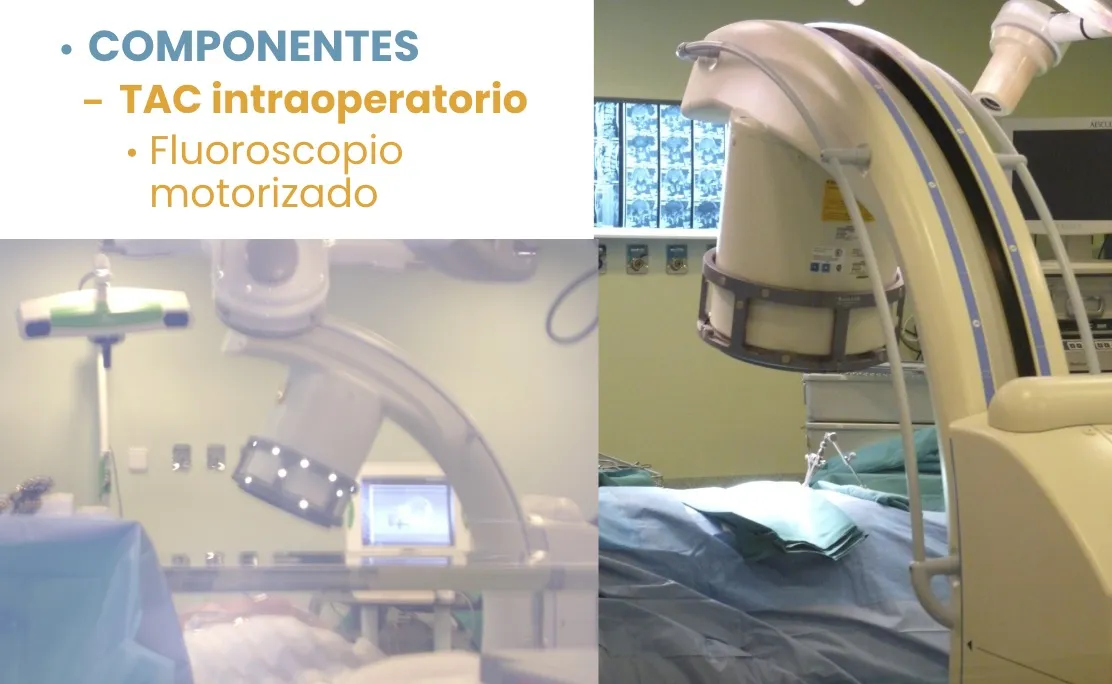
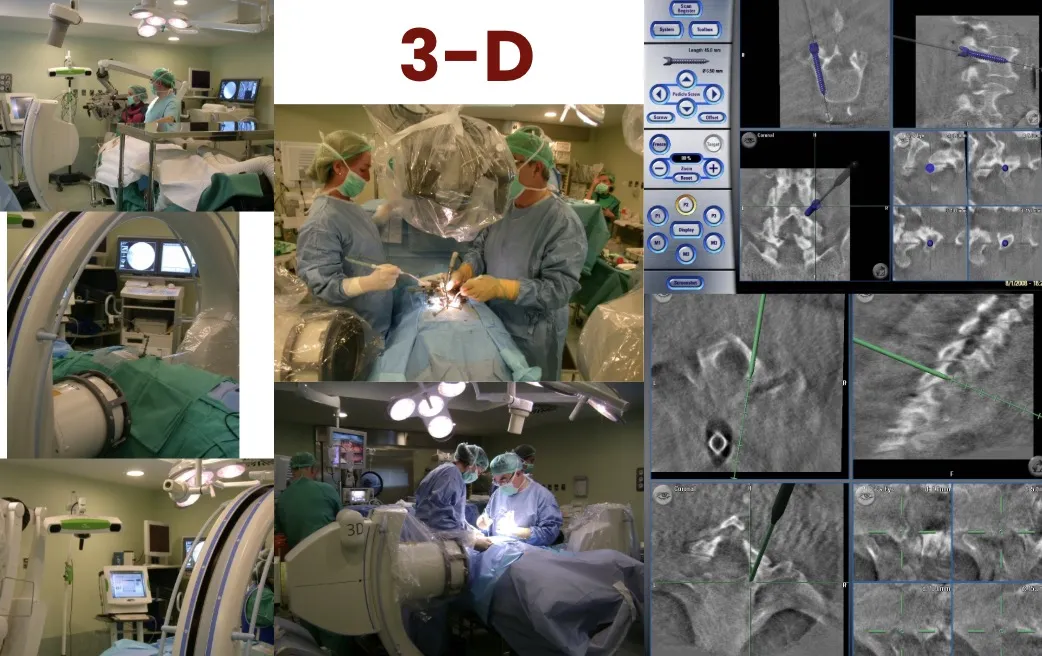
Neuronavegador 3D
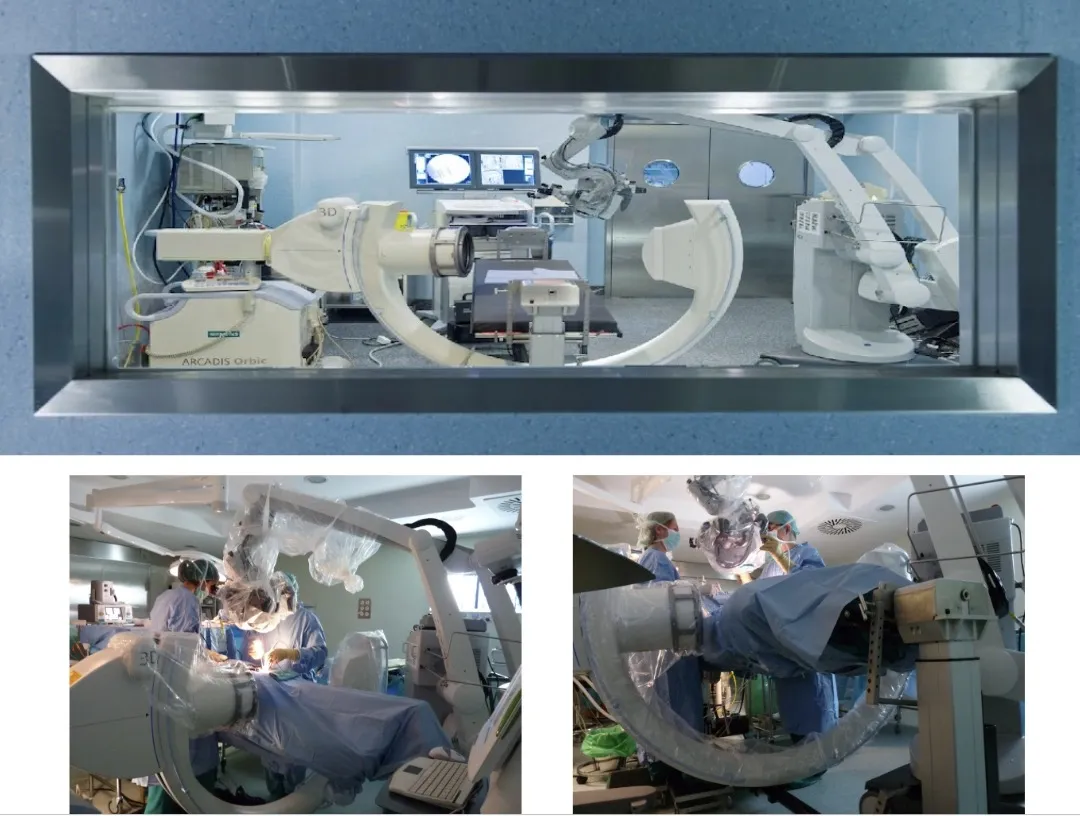
Los sistemas de neuronavegación, en conjunción con el TAC intraoperatorio, permiten obtener en tiempo real imágenes antes y de control durante el acto quirúrgico.
Sus componentes principales son:
- TAC intraoperatorio.
- Fluoroscopio motorizado.
El neuronavegador permite además guiar con gran precisión los instrumentos diseñados para fijar y fusionar las vértebras (como los tornillos pediculares).
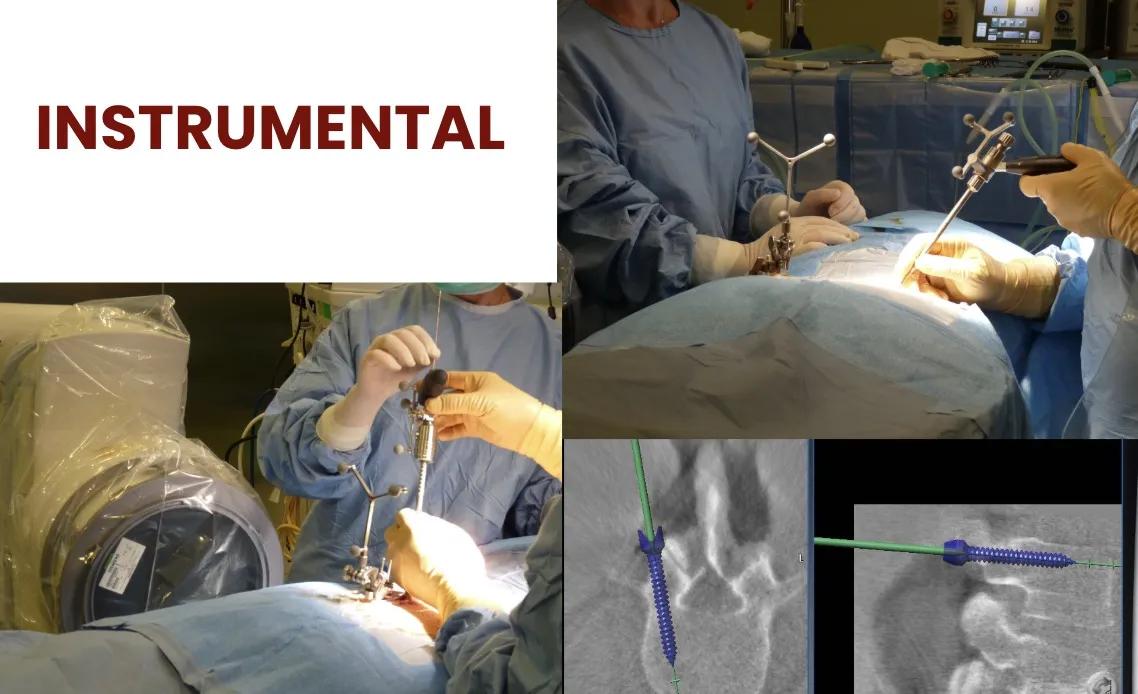
De este modo, el cirujano tiene en todo momento una gran seguridad y conocimiento de dónde se encuentra, con un error menor de 1 mm. Esto facilita además la realización de cualquier actuación microquirúrgica guiada.
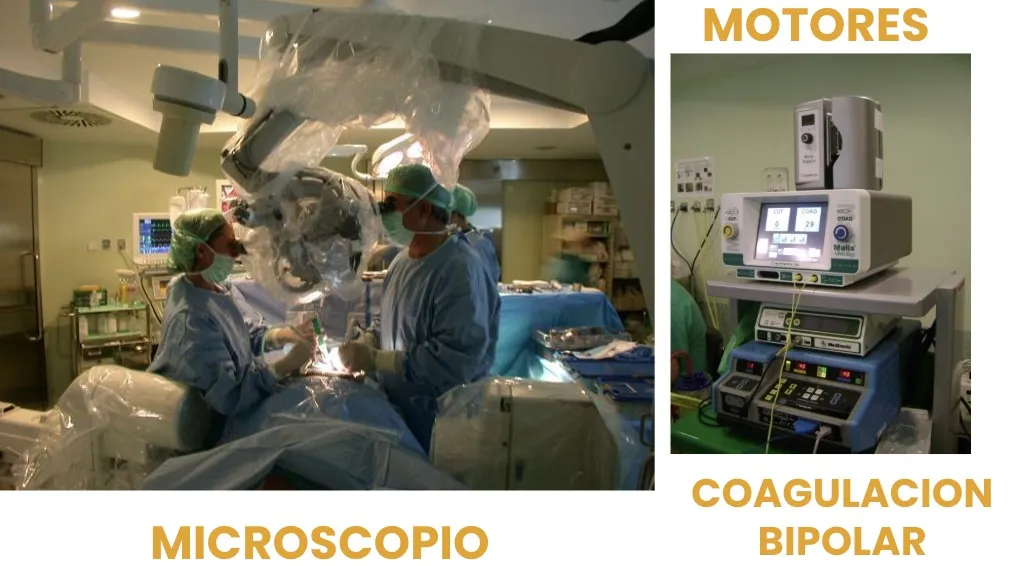
Microscopio quirúrgico
Los microscopios actuales son altamente eficaces, tanto en cuanto a la movilidad como a la visión del campo quirúrgico. La buena conjunción y armonización entre mesa de Jackson, TAC, neuronavegador y microscopio ha cambiado de forma sustancial el resultado quirúrgico.
Otros elementos: motores y coagulación bipolar
Hay otros elementos esenciales que merece la pena mencionar. Destaca el motor quirúrgico de altas revoluciones, con fresas de muy alta precisión y eficacia, que permite trabajar el hueso sin lesionar los tejidos blandos circundantes. Junto a él, la coagulación bipolar resulta fundamental para el control de la hemostasia con mínima agresión a los tejidos.
El resultado es que, alrededor del paciente, se conjugan perfectamente niveles de muy alta tecnología.
Instrumentación vertebral
En el capítulo de los implantes también se ha producido una notable sofisticación.
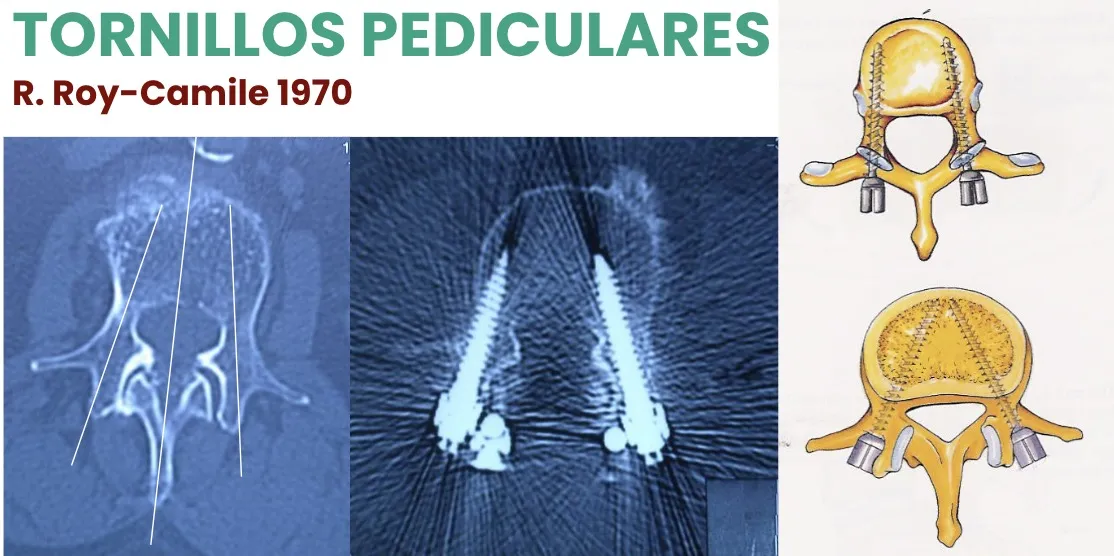
Tornillos pediculares
Se ha desarrollado mucho la posibilidad de fijar las vértebras con tornillos a través de sus pedículos. Los tornillos pediculares, introducidos por R. Roy-Camille en 1970, constituyen hoy un pilar fundamental de la instrumentación raquídea.
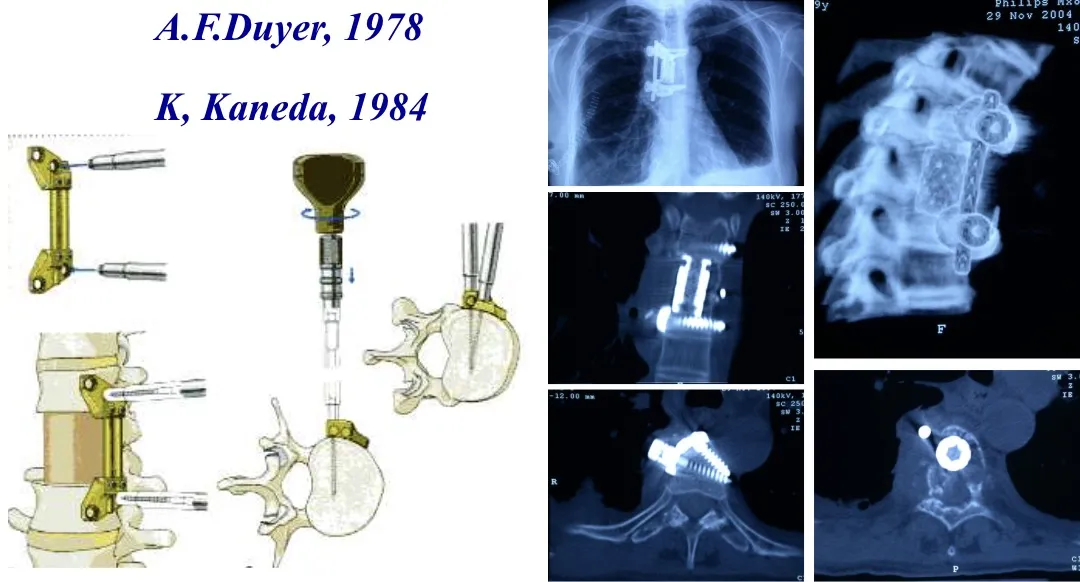
Instrumentación anterolateral
Otra opción es la instrumentación anterolateral, desarrollada por A. F. Dwyer (1978) y K. Kaneda (1984), que aborda la columna por vía anterior y resulta especialmente útil en determinadas patologías.
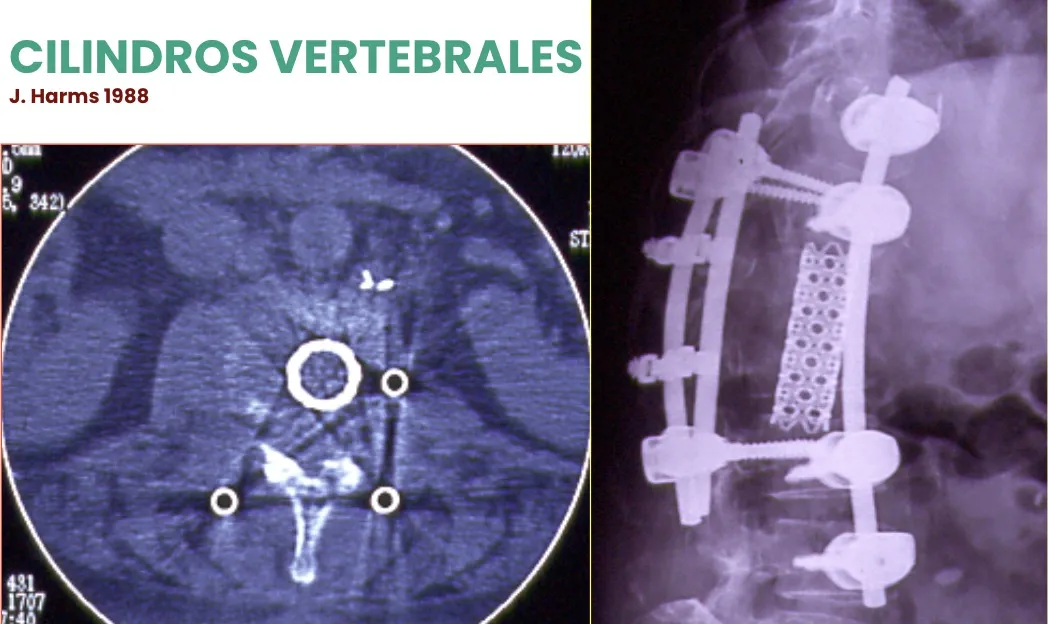
Cilindros vertebrales expandibles
También es posible colocar sustitutos de los cuerpos vertebrales en forma de cilindros-cajas expandibles, descritos por J. Harms en 1988. De este modo, en fracturas muy graves e inestables, resulta posible reconstruir la columna.
Neurofisiología intraoperatoria
Por último, hay que añadir la posibilidad de conocer la función medular y radicular durante todo el acto quirúrgico, gracias al control neurofisiológico intraoperatorio.
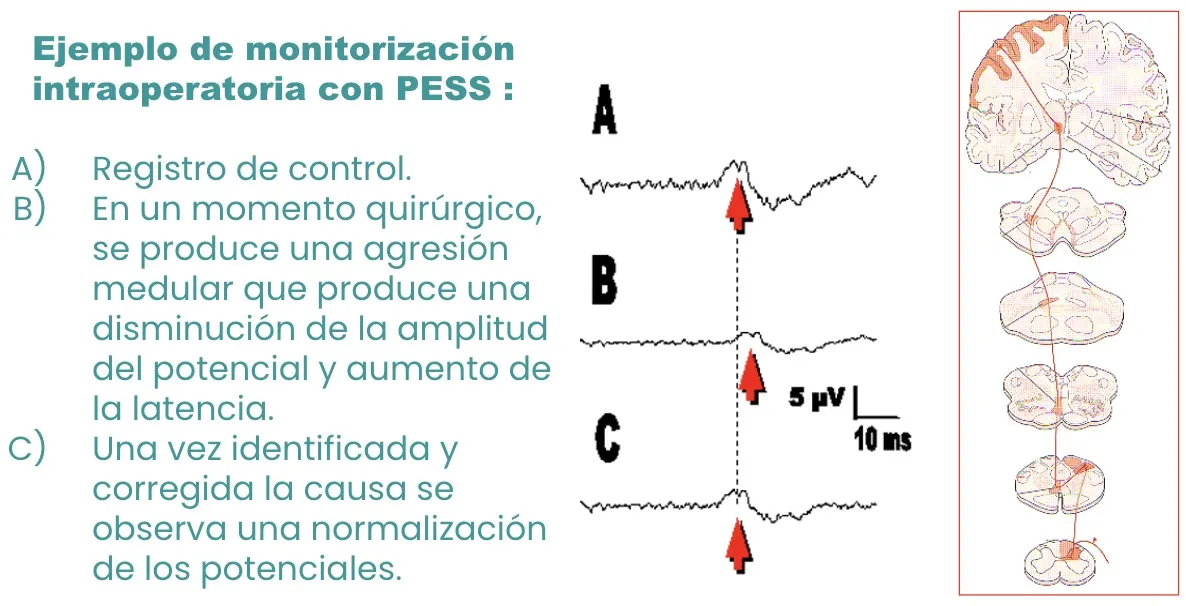
Potenciales evocados somato-sensoriales (PESS)
Es posible estimular nervios sensitivos y recoger la actividad cerebral resultante en el cuero cabelludo. Son los potenciales evocados somato-sensoriales. En un registro de control normal, si durante la cirugía se produce una agresión medular, los potenciales muestran una disminución de la amplitud y un aumento de la latencia. Una vez identificada y corregida la causa, los potenciales se normalizan.
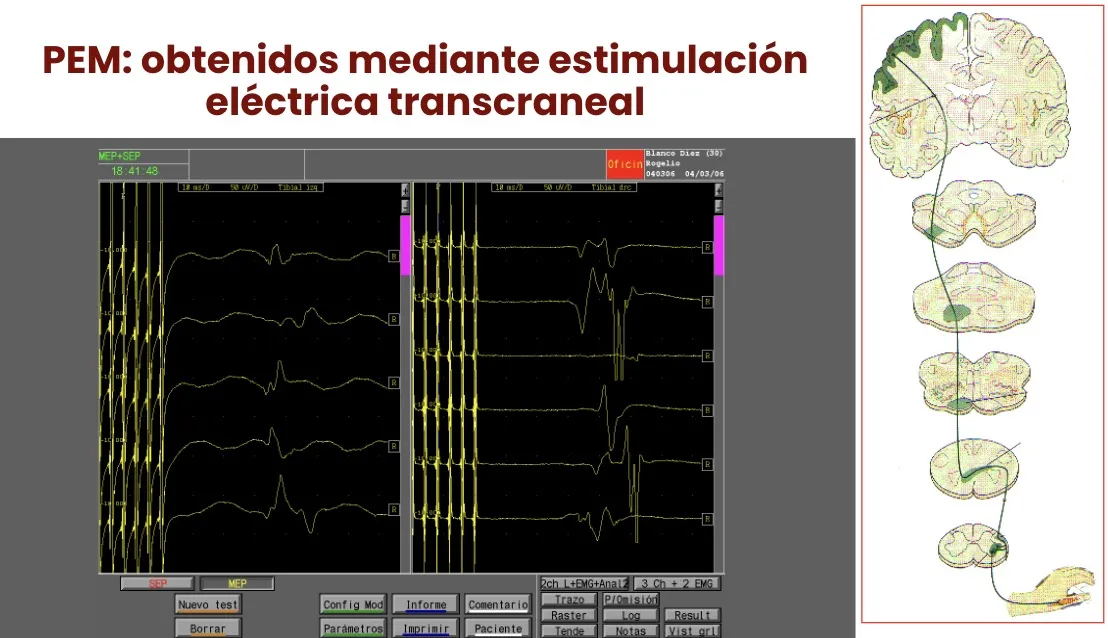
Potenciales evocados motores (PEM)
En sentido inverso, se puede estimular la corteza motora cerebral a través de la piel y recoger la actividad EMG en los músculos. Son los potenciales evocados motores, obtenidos mediante estimulación eléctrica transcraneal.
Estas señales tienen que pasar por la zona medular en la que se está actuando quirúrgicamente. De manera que el neurofisiólogo puede informar al cirujano en cualquier momento sobre si la señal está mejorando o empeorando, y si conviene corregir o no las maniobras quirúrgicas.
Ejemplos clínicos de tratamiento quirúrgico
Corrección de una fractura grave a nivel D12
Corrección de una fractura grave a nivel de D12, en la charnela tóraco-lumbar. Gracias a la mesa de Jackson y a las maniobras de cifoplastia (distribución de cemento) y de fijación con tornillos pediculares, se consigue corregir la alineación y estabilizar el segmento afectado.
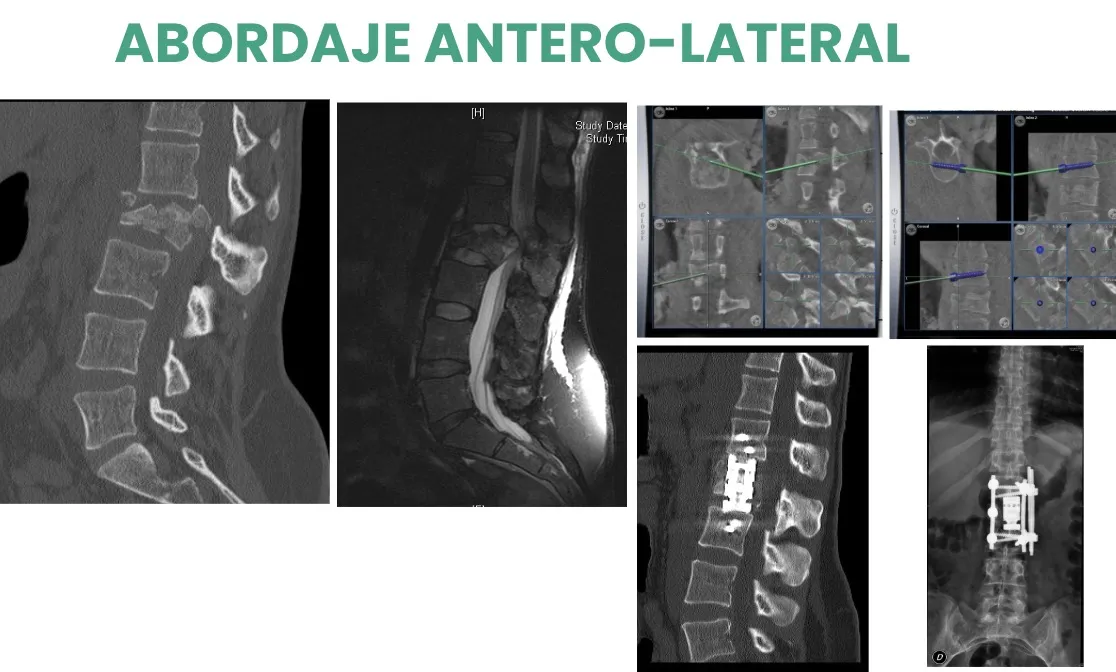
Extirpación del cuerpo vertebral de L2
Otro ejemplo es la necesidad de realizar la extirpación del cuerpo vertebral de L2, que se ha introducido en el canal medular. Se realiza —con ayuda del microscopio— una sustitución mediante un cilindro expandible, que facilita la reducción de la fractura y permite una mejor alineación vertebral. La fijación final se completa con tornillos pediculares y barras.
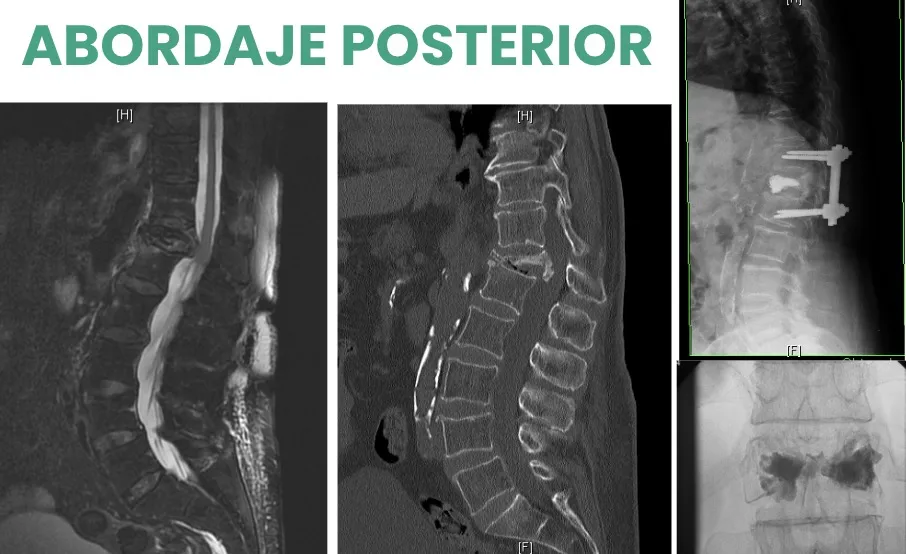
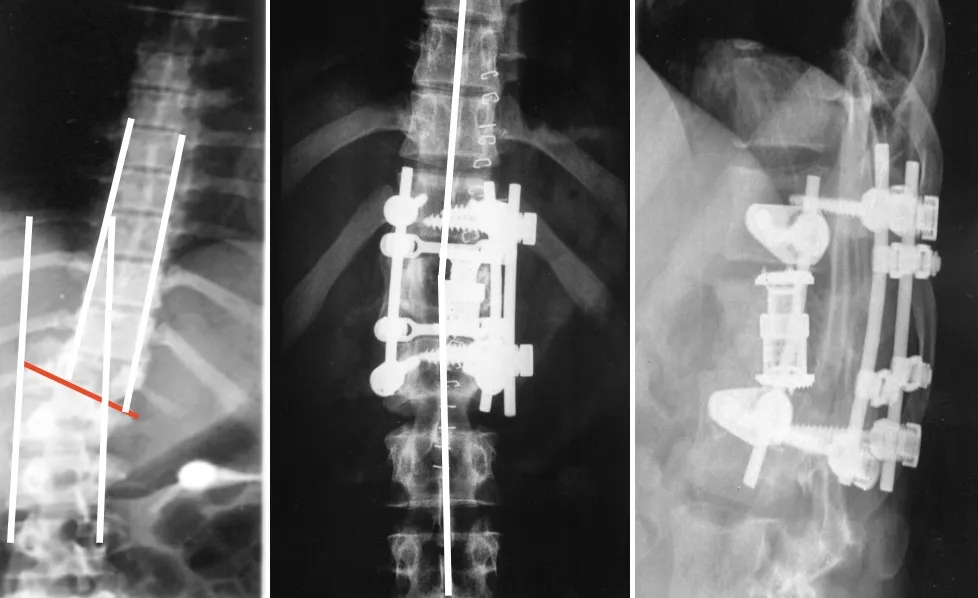
Fractura por cizallamiento tóraco-lumbar
Tercer ejemplo: paciente con una fractura muy grave de cizallamiento a nivel tóraco-lumbar, afortunadamente sin lesión neurológica. Se realizó una corrección de la fractura, con una correcta alineación de la columna, y una fijación aún más completa que en los casos anteriores, mediante sistemas de mayor potencia.
La columna se merece la misma delicadeza que el cerebro
En conclusión, hoy puede decirse que, con los medios puestos a nuestro alcance, la columna se debe tratar con la misma delicadeza que el cerebro. Esta idea, lejos de ser un eslogan, refleja la integración real de tecnología, técnica quirúrgica y trabajo en equipo que caracteriza la cirugía raquimedular actual.

Conclusión
El síndrome de sección medular representa una de las patologías neuroquirúrgicas más graves, con consecuencias que pueden ser permanentes y devastadoras para la vida del paciente. Su comprensión exige conocer la anatomía y función de la médula espinal —con sus astas, cordones y haces específicos para la motricidad, la sensibilidad profunda y la sensibilidad al dolor y la temperatura— así como las fases clínicas que la lesión atraviesa: shock medular, recuperación y, en los casos más graves, lesión establecida completa o incompleta.
Los traumatismos raquimedulares siguen siendo la causa principal, afectando preferentemente a varones jóvenes y a determinadas regiones vertebrales (cervicales altas y transición tóraco-lumbar). Aunque su incidencia ha disminuido gracias a las medidas preventivas en el tráfico y el ámbito laboral, su gravedad obliga a una atención precoz y multidisciplinar, en la que el diagnóstico por imagen, el control neurofisiológico y el tratamiento quirúrgico desempeñan un papel decisivo.
El tratamiento quirúrgico actual descansa sobre una integración armónica de medios técnicos —mesa de Jackson, neuronavegador, TAC intraoperatorio, microscopio, motores, sistemas de instrumentación y neurofisiología intraoperatoria— que permite operar la columna con la misma precisión y delicadeza con que se opera el cerebro. Tras la fase aguda, la rehabilitación en centros especializados resulta fundamental para preservar la máxima calidad de vida posible.