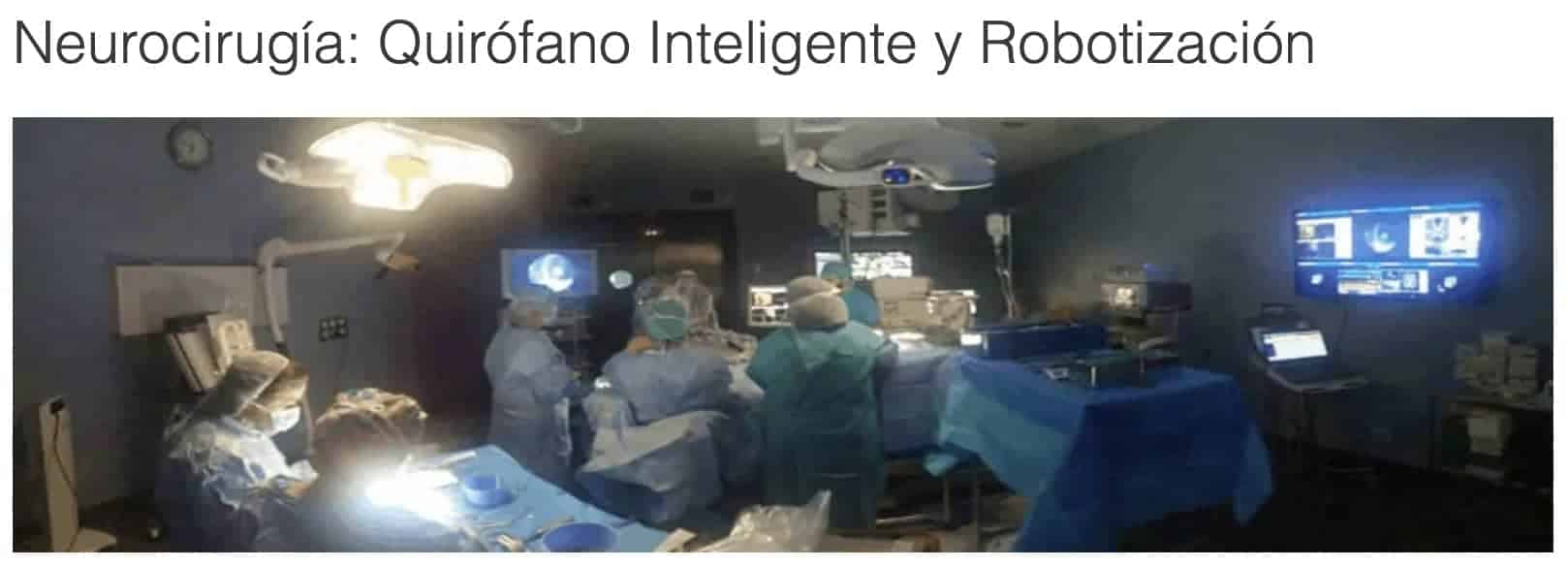
Formas de ver el campo quirúrgico en la cirugía de columna
El Dr. Rafael García de Sola describe ccómo se puede visualizar el campo quirúrgico en la cirugía de columna. Hay diferentes posibilidades e indicaciones de los equipos médicos que permiten ver mejor los detalles anatómicos quirúrgicos (lupas, microscopio, endoscopio y exoscopio). El objetivo de este artículo es que se pueda comprender las ventajas y límites de cada tipo de visión, así como el esfuerzo que ha ido haciendo la tecnología y el médico para ir hacia una cirugía cada vez menos invasiva y agresiva.
Rafael García de Sola
Director de la Cátedra UAM “Innovación en Neurocirugía”
Jefe del Servicio de Neurocirugía
Hospital Ntra. Sra. del Rosario
Madrid
Introducción
Para llevar a cabo la cirugía raquimedular se precisa una perfecta armonía (García de Sola, 2014) entre componentes muy complejos:
- A.- El equipo humano (Cirujanos, Anestesistas, Enfermería, Técnicos de Rx…), que han de trabajar al unísono.
- B.- Equipamiento neuroquirúrgico.
- C.- Instrumental quirúrgico e instrumental para implantación de prótesis.
En anteriores comunicaciones hemos definido 5 pilares de la Neurocirugía actual: 1.- Imagen. 2.- Neuronavegación. 3.- Función. 4.- Robotización. 5.- Visión.
Más información:
1.- Imagen: Hay que destacar, en primer lugar, que los estudios de imagen preoperatorios permiten hoy día obtener un alto nivel de información. De esta forma podremos diseñar la intervención a llevar a cabo, de acuerdo con la clínica y los datos anatómicos de cada paciente concreto.
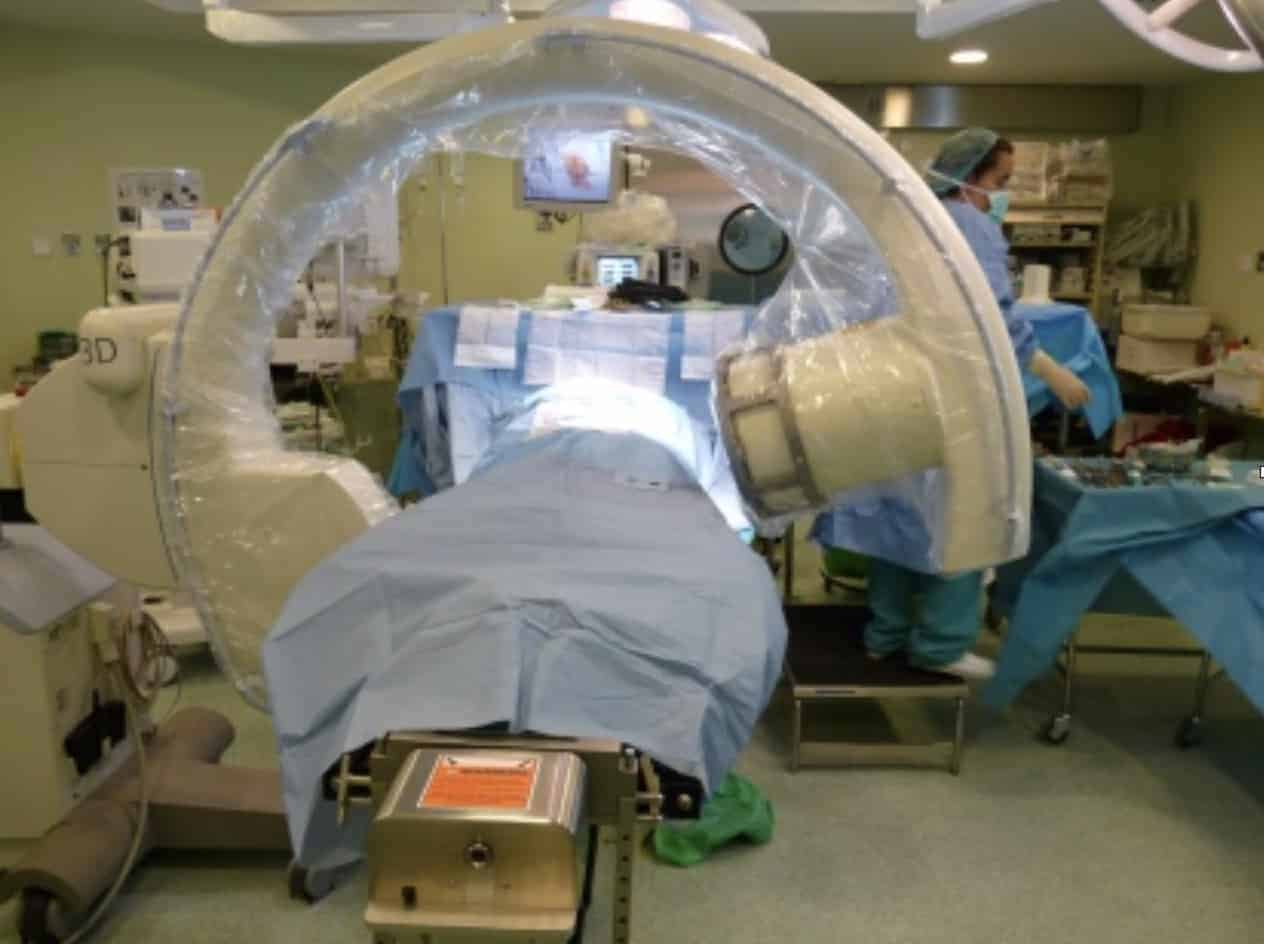
2.- Neuronavegación: En segundo lugar, la neuronavegación de columna. El primer equipo aparece en 2002, tratándose de un equipo Siemens de imagen 3D intraoperatorio, basado en un arco en C motorizado (Arcadis). Sus imágenes podían pasarse a un equipo de neuronavegación similar al neuronavegador cráneo-encefálico. Esto supuso un gran avance y ventajas con respecto a la utilización del arco en C 2D convencional: a) Obtención de imágenes de TAC intraoperatorias, antes de ejecutar la intervención quirúrgica, de gran precisión anatómica. El cirujano va a disponer en cualquier momento de imágenes 3D, en los tres planos del espacio, del lugar donde está actuando. b) Posibilidad de control intraoperatorio, tras la implantación de tornillos pediculares u otra instrumentación.
En 2006 aparece el O-Arm (Medtronic). En esta última década están apareciendo diferentes dispositivos de TAC intraoperatorio neuronavagado.
Nosotros incorporamos esta tecnología en 2008, siendo los pioneros en neuronavegación 3D en España (Pulido, 2014)
Gracias a estos equipos, junto a la mesa de Jackson radiotransparente para cirugía de raquis, se han podido realizar, por ejemplo, fijaciones muy complejas (ver-> Delgado, et al., 2021), sin complicaciones de malposición de tornillos.
3.- Función: Durante las intervenciones quirúrgicas a nivel raquimedular, el control neurofisiológico intraoperatorio es, en muchas ocasiones esencial, sobre todo para abordar las lesiones intramedulares (García de Sola, 2014).
4.- Robotización: Llama la atención la aparición casi explosiva de la idea de robotización en este tipo de cirugía. La atracción que produce en médicos y pacientes es extraordinaria. Todo este movimiento está siendo promovido por una idea superior: hacer la cirugía lo mínimamente invasiva posible.
El robot se utiliza en conjunción con la navegación intraoperatoria y su brazo sirve como soporte fijo y seguro para los instrumentos que se utilizan en la implantación de tornillos pediculares, por ejemplo. Una de las ventajas colaterales que está ofreciendo es que los conceptos de neuronavegación están siendo asumidos por cirujanos ortopédicos, reacios hasta ahora a la neuronavegación en la cirugía de columna, que es, por el contrario muy familiar en Neurocirugía. Pero son asistentes al cirujano más que máquinas autónomas. También ayudan a trazar la trayectoria. Podrían colaborar en sostener el canal de trabajo o el endoscopio.
5.- Visión: En este contexto, una visión correcta del campo quirúrgico es esencial, por lo que se han ido desarrollando equipos muy complejos que posibilitan llegar a estructuras profundas, a través de canales de trabajo muy estrechos. Pasamos a describir con más detenimiento esta tecnología.
Historia
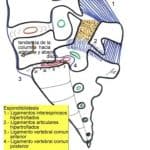
Se atribuye a Adson, en 1922, la primera intervención quirúrgica para extirpar un núcleo pulposo herniado. Aunque fueron Mixter y Barr los que describieron la primera serie de tratamiento quirúrgico de hernias discales lumbares, mediante laminectomía.
En 1977, Yasargil describe la aplicación del microscopio quirúrgico para la discectomía lumbar. Yasargil, con una serie de más de 100 pacientes, habla también de utilizar la coagulación bipolar para facilitar la hemostasia.
Este tipo de abordaje quirúrgico, la microdiscectomía lumbar, en el ámbito neuroquirúrgico, se convirtió en el gold standard del tratamiento quirúrgico de la hernia discal lumbar (Mayer, 2019).
Hace poco más de 20 años, se inician las técnicas de abordaje endoscópico, denominándolo Microendoscopia Lumbar, aunque utiliza la misma vía de abordaje que en la microcirugía (Perez-Cruet, et al., 2002). Ambas técnicas tienen resultados similares.
Pero la técnica no se popularizó por la necesidad de una amplia curva de aprendizaje, junto a una dificultad de visión del campo quirúrgico. Hasta que, al final de los años 90, se propone utilizar la misma idea de las técnicas artroscópicas: doble vía para tener irrigación continua.
Lupas
La compañía Carl Zeiss fue la primera en disponer de una lupa binocular, adaptadas a gafas especiales, con una distancia de trabajo de 25 cm. Pero estos sistemas tienen los inconvenientes de ser inestables, precisan de un casco con luz (fotóforo) y pueden ser muy incómodos para el cirujano. Aunque muchos cirujanos adquieren experiencia y lo utilizan de forma rutinaria en la cirugía de raquis.
Los cirujanos que utilizan lupas están forzados a mantener el cuello en flexión, con mayor fatiga e incluso dolor. A diferencia con el microscopio, con el que la maniobrabilidad y ergonomía es extraordinariamente superior.
Por último, con las lupas el ayudante no puede ver el campo quirúrgico bien, mientras que el microscopio permite una visión incluso cara a cara (Fig. 1). Además, con el microscopio, como después veremos, las imágenes puedan ser vistas por el personal de enfermería, anestesia, etc., aparte de poder grabarlas para docencia y revisión de casos.
Por todas estas razones, no vale la pena invertir tiempo en el aprendizaje y uso de esta forma de visión, con lupas, muy extendida en quirófanos de otros países.
Microscopio
El microscopio quirúrgico fue utilizado por primera vez en 1922, en Otorrinolaringología (ORL). Pero utilizando un microscopio monocular. Un año después Holmgren tuvo la idea de utilizar un microscopio binocular, junto a una fuente de luz (Uluç, et al. 2009). Esto permitió dar profundidad de campo.
La primera aplicación en Neurocirugía del microscopio quirúrgico no se produjo hasta 1957, por Theodor Kurze. Tuvo un gran impacto, puesto que la magnificación, iluminación y la mejor visualización (visión estereoscópica) de las estructuras anatómicas y tejido patológico mejoraron extraordinariamente la seguridad y resultados quirúrgicos.
A lo largo del tiempo, gracias, sobre todo, a la influencia de grandes neurocirujanos, se fueron modificando sus diversos componentes: estativo, brazo articulado, compartir la visión del campo quirúrgico con el ayudante, distancia focal o de trabajo, magnificación y foco variables, iluminación coaxial, integración con los sistemas de navegación, fluorescencia, plataformas robotizadas, asistencia endoscópica, etc.
Los microscopios quirúrgicos presentan varias ventajas (Uluc, et al., 2009):
1.- Óptica de alta precisión. 2.- Iluminación coaxial de alto rendimiento. 3.- Zoom para magnificación variable. 4.- Foco variable, con gran distancia de trabajo. 5.- Amplia visión del campo quirúrgico sin obstrucción. 6.- Estabilidad y amplia variabilidad del sistema de soporte. 7.- Estereoscopia, con capacidad de visión en tercera dimensión del campo quirúrgico.
Componentes
El microscopio consta esencialmente de varios componentes: Sistema óptico, fuente de luz, estructura de soporte y sistemas de visualización. A lo que hay que añadir las imágenes por fluorescencia (5-ALA, Fluoresceina o Verde Indiocianina).
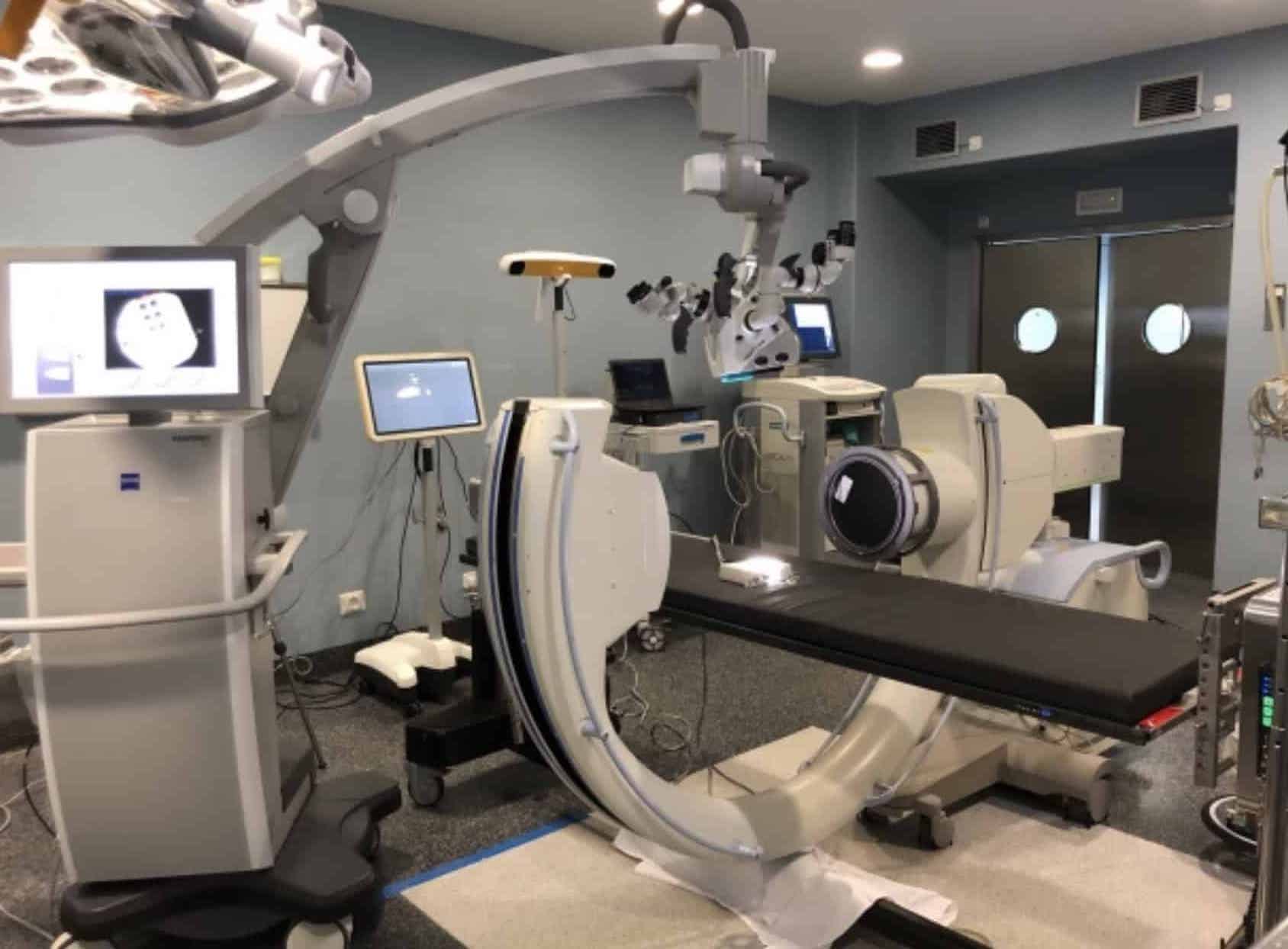
A.- Sistema óptico.
Da la posibilidad de visión binocular, con capacidad estereoscópica o sensación tridimensional de profundidad de campo.
En relación con la magnificación, hay que tener en cuenta que el ojo humano puede llegar a distinguir dos líneas separadas hasta 0’2 mm. Por debajo de esta distancia, se ve una sola línea. Por lo que el microscopio mejora la disección fina de estructuras de riesgo (Damadoran, et al., 2013). El zoom varía en algunos microscopios de 6:1 a 8:1. De manera que la resolución del ojo humano de 0’2 mm. puede aumentar a 0’01 mm., con una magnificación de 20x. Esto permite realizar técnicas quirúrgicas muy delicadas, con mucha precisión, ayudados con instrumentos muy finos.
Otra de las características que han evolucionado es la capacidad de enfocar correctamente. Hay una mayor profundidad de campo (área quirúrgica que es posible ver con nitidez, por abajo y por encima del punto de perfecto enfoque) y se han desarrollado mecanismos de enfoque automático o autofocus, basados en rayos láser activos. Ayudan, por ejemplo, a mantener una visión adecuada para el ayudante y los sistemas de visión conectados al microscopio (pantallas, video, fotografía…).
B.- Iluminación.
Tienen que aportar una buena luz, similar a la temperatura e intensidad de la luz solar. Estable, a pesar de los cambios en el foco o en la magnificación.
En Neurocirugía se utilizan, como fuentes de luz, las lámparas de xenón o halógenas, con filtros adecuados para los espectros de infrarrojo y ultravioleta. Para evitar al máximo el calor que se produce en la fuente de luz, ésta es transmitida por fibra óptica.
La iluminación es coaxial, lo que evita las sombras, aparte de poder dirigir la luz a cavidades profundas. Es muy estable, de manera que los modernos microscopios ajustan automáticamente la intensidad luminosa con los cambios focales o de magnificación.
C.- Estativo
Se ha conseguido una gran estabilidad, sin vibraciones. Para eso se ha llegado a sofisticados mecanismos de compensación y balance en 6 ejes. A lo que hay que añadir la más reciente complejidad, mediante la robotización, que permite autoposicionarse, cambiar de ángulo manteniendo el mismo target, o combinarse con los dispositivos de neuronavegación. Estos movimientos pueden llevarse a cabo manualmente, a través de joystick, pedal, boca o sistemas de manos libres.
Los microscopios están dotados de coberturas de plástico transparente, de un solo uso, para mantener la esterilidad.
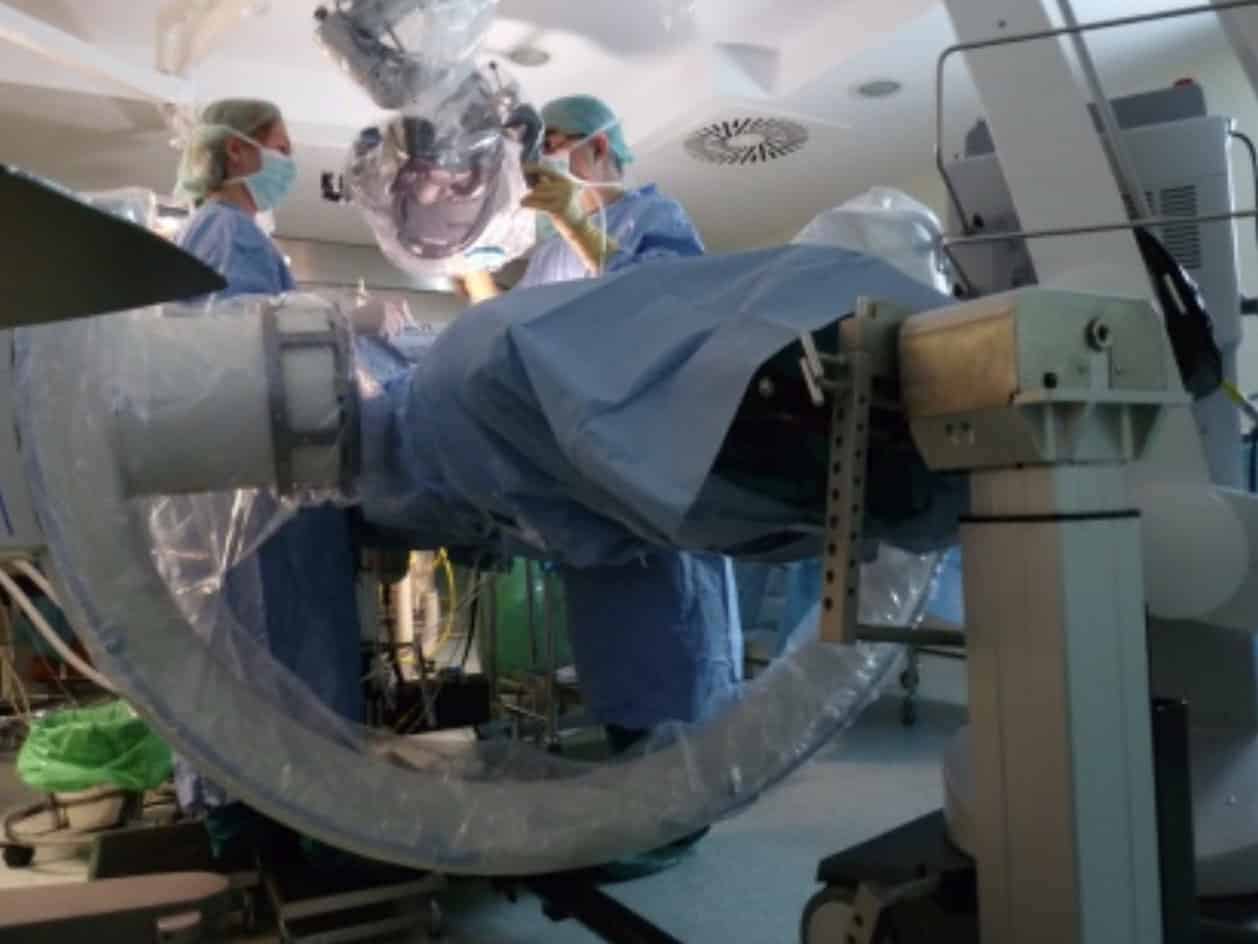
Todos estos mecanismos permiten un alto nivel ergonómico. Ya hay microscopios con una distancia focal de hasta 600 mm. Lo que permite introducir instrumentos más largos, como los necesarios en cirugía de raquis. Y, gracias a su largo brazo, es posible colocar el estativo por detrás del cirujano, esté de pie o sentado, dejando libre todo el espacio quirúrgico a su alrededor (Fig. 1, 2).
D.- Sistemas de visualización
Ya hemos comentado la estereoscopia, como una de las enormes ventajas que ofrece el microscopio quirúrgico. A lo que habría que sumar la posibilidad de que el ayudante pueda colaborar activamente, incluso con la misma visión que el cirujano, con la posición cara a cara de los oculares (Fig. 1).
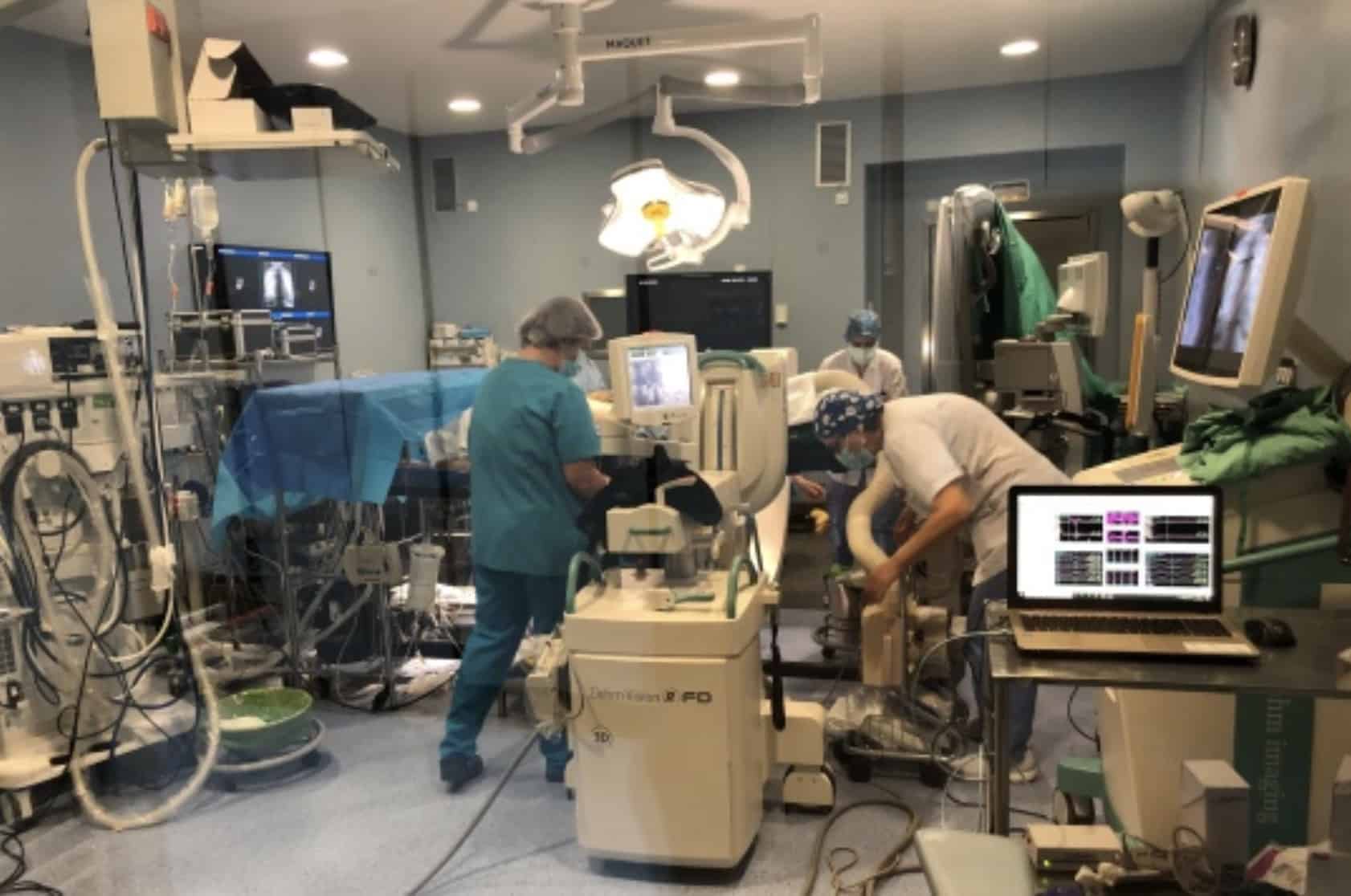
Permite añadir otros coobservadores o enviar las imágenes HD a pantallas colocadas en el mismo equipo o fuera, en el ambiente de quirófano. Esto posibilita la visión del campo quirúrgico, incluso en 3D, por el equipo quirúrgico (anestesista, enfermeras, personal auxiliar…). Toda esta información es posible registrarla y guardarla, de manera que pueda servir para docencia, recogida de datos y experiencia o, incluso, para realizar programas de realidad virtual (Fig. 3, 4).
Entre los inconvenientes que se citan para el microscopio, destacan:
- 1.- Su alto coste.
- 2.- Teórico riesgo de contaminación del campo quirúrgico.
- 3.- La necesaria curva de aprendizaje. Aunque esto último no es óbice en Neurocirugía, dado su frecuente uso desde el periodo de Residencia.
Sin embargo, en la cirugía de raquis no se utiliza con la frecuencia que se supone por los beneficios que aporta. Uno de los factores que puede influir es la cultura quirúrgica durante el periodo de Residencia y el menor uso en la especialidad de Cirugía Ortopédica, en comparación con la endoscopia. Así como lo contrario, la mayor experiencia en endoscopia por parte de la Cirugía Ortopédica.
Basques et al (2015) realizaron una evaluación en más de 25.000 intervenciones quirúrgicas a nivel de raquis, en EEUU, en 2011 y 2012. A pesar de que el microscopio ha tenido una aceptación cada vez mayor, no llegaba al 10% el porcentaje de cirujanos que utilizaban microscopio.
El microscopio facilitó, además, el hacer incisiones y abordajes menos agresivos, colaborando en la evolución de la cirugía mínimamente invasiva. Hace, por ejemplo, mucho menos arriesgadas las maniobras de descompresión ósea con motor para fresado óseo y laminotomos.
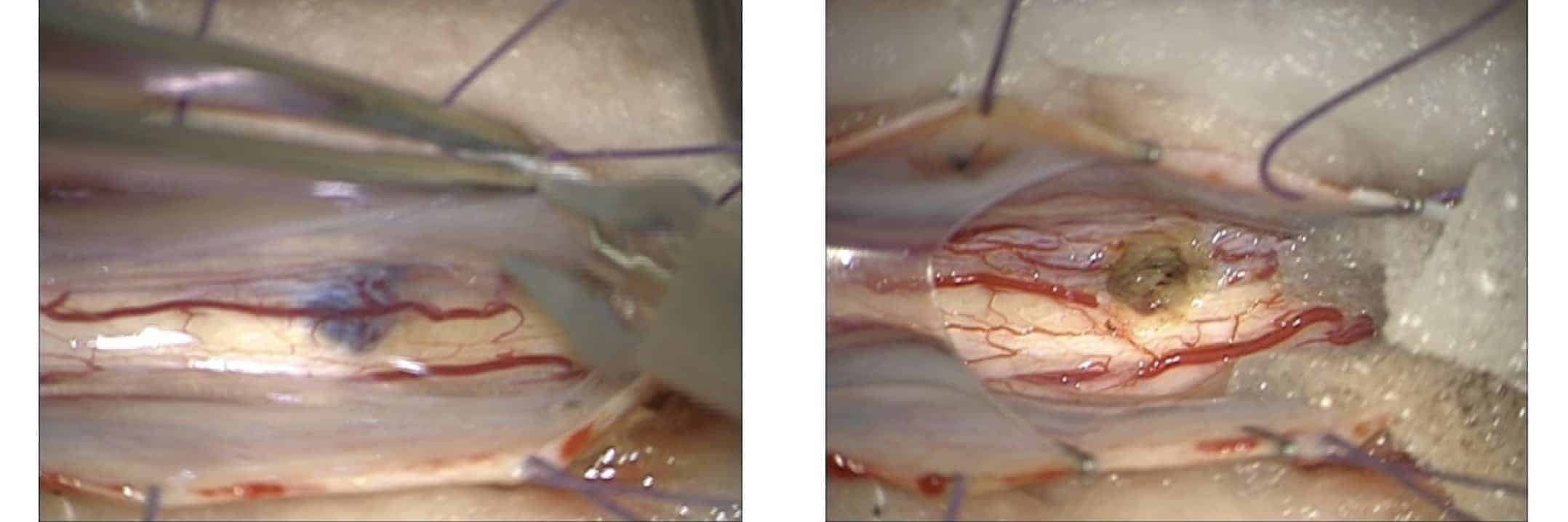
Endoscopia
La posibilidad de acceso percutáneo guiado por imagen y la tecnología endoscópica han revolucionado la cirugía mínimamente invasiva (Mayer, 2019). A finales de los 90, Foley et al. proponen las técnicas endoscópicas frente a la utilización del microscopio quirúrgico, para abordar las hernias discales lumbares (“microendoscopic discectomies”), con especial aplicación a las hernias extraforaminales (Pérez-Cruet, et al., 2002).
La discectomía endoscópica ha ido mostrando algunos beneficios en comparación con la microdiscectomía: menos estancia media, así como incorporación más precoz a la actividad normal. Aunque no hay diferencias en cuanto a escalas postquirúrgicas como VAS y ODI, complicaciones, recurrencia y reoperaciones (Choi, et al., 2018).
Pero su teórica mayor ventaja es que disminuye la presión sobre tejidos blandos, debido a la tracción continuada de los retractores, con conservación máxima de hueso y ligamentos, consiguiendo una descompresión óptima sin destrucción tisular excesiva (Kim, et al., 2020).
Con el endoscopio podemos variar: 1.- El poder de iluminación. 2.- El campo de visión o cono de visualización centrado en la cámara. 3.- El ángulo óptico, entre el eje de la cámara y el eje del endoscopio. Varía de 0º a 30º. A mayor ángulo, mayor riesgo de desorientación. 4.- Distancia focal. La mayoría varía de 10 a 40 mm. Con una distancia focal mayor, la imagen se mantiene más nítida con los movimientos.
Las técnicas endoscópicas son útiles para manipulaciones quirúrgicas en espacios quirúrgicos muy confinados. Pero tienen sus límites cuando las paredes son rígidas (hueso) o las estructuras circundantes tienen riesgo de ser lesionadas (vasos, estructuras nerviosas). Sus riesgos y limitaciones son (Basil, et al., 2021): Campo de visión limitado y pérdida de resolución, con dificultad para reconocer las estructuras anatómicas; desorientación del cirujano y pérdida de perspectiva, dada la orientación angulada; así como limitaciones de movimiento por el túnel de trabajo y diseño de los instrumentos. Otros límites son el trabajo con una sola mano, a diferencia del microscopio, la necesidad de nuevos diseños de instrumentación y una prolongada curva de aprendizaje (Kim HS, et al., 2020).
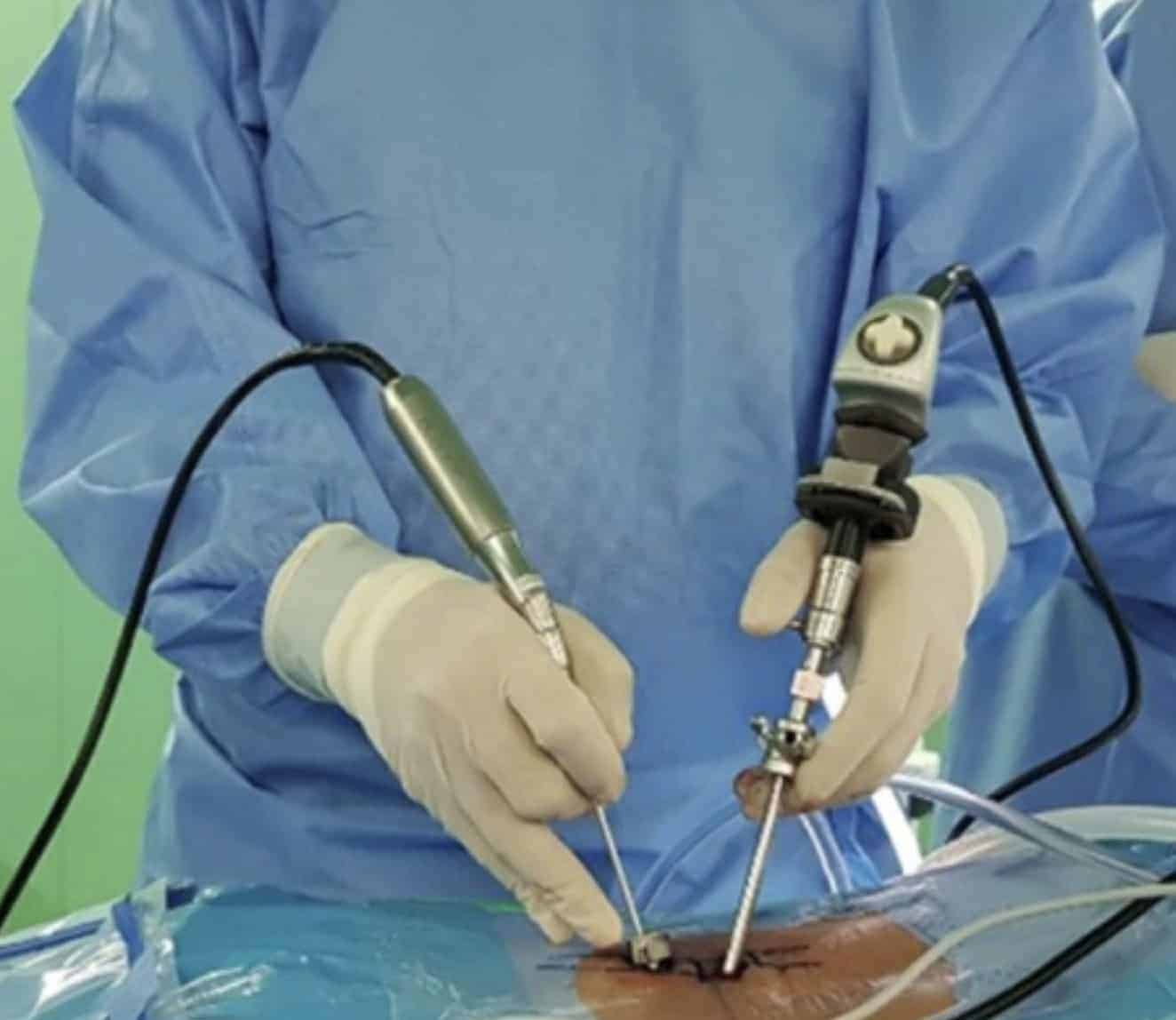
Principales indicaciones
- A.- La discectomía endoscópica uniportal, en comparación con la microdiscectomía, parece mostrar una estancia hospitalaria menor y menos dolor radicular a los dos años postoperatorios. El abordaje puede ser transforaminal o interlaminar. Aunque, al final, puede requerir el mismo tipo de exposición y manipulación de músculo y hueso que la microdiscectomía, en cuanto a dilatadores y retracción tubular (He, et al., 2016).
Como ventajas: Disminución de costes, al ser el tratamiento ambulatorio; mayor facilidad en los casos de hernia foraminal y extraforaminal; menos herida quirúrgica; mayor facilidad en pacientes obesos. Como inconvenientes, la técnica es difícil de aprender, el campo de visión es estrecho y precisa más tiempo quirúrgico, así como menor capacidad de resección discal. - B.- La discectomía endoscópica biportal presenta resultados similares a la microdiscectomía, con menor pérdida de sangre, estancia hospitalaria y dolor postoperatorio. Aunque se excluyen las hernias discales foraminales y extraforaminales. Uno de los portales se utiliza para una irrigación continua. El otro portal permite utilizar una instrumentación similar a la microdiscectomía, con instrumentación adaptada (fresas, laminotomos, coagulación, pinzas de hipófisis…). Por lo que ofrece mayor libertad de movimientos que el abordaje uniportal. Desde el punto de vista técnico, en relación a la microdiscectomía, puede tener mayor dificultad en controlar la hemorragia y extirpar por completo los fragmentos discales extruidos (Kim, et al., 2018).
Al ser un abordaje similar, podría ser más fácil adquirir experiencia por un cirujano experimentado en microcirugía (Choi, et al., 2018).
Otras indicaciones
- 1.- Estenosis lumbar. Se puede realizar una descompresión bilateral (Kim et al., 2020), a través de una laminotomia unilateral, con técnicas MIS y retractores tubulares.
2.- Técnicas de fusión intersomática lumbar, a través de una vía transforaminal, siguiendo el triángulo de Kambin (Kang, et al., 2021). Con el inconveniente de limitación de movimientos por el canal de trabajo y riesgos de lesión radicular (Park et al., 2020). O utilizando una vía postero-lateral (Kim, et al., 2020).
El abordaje tubular MIS con microscopio es igual, en cuanto a resultados quirúrgicos, al abordaje endoscópico biportal (Kang, et al., 2021) para la fusión intersomática.
3.- Patología discal cervical. Por vía posterior, para realizar foraminotomías o discectomia (Reutten, et al., 2007), así como laminectomias y descompresión bilateral en mielopatías por estenosis (Lin, et la., 2019). O por vía anterior, para realizar discectomía, aunque con menor difusión entre la comunidad quirúrgica (Kim et al., 2020), por su dificultad y riesgo quirúrgico.
4.- Columna torácica. El abordaje transforaminal e interlaminar a las hernias discales y estenosis han sido los más utilizados. Esto está suponiendo el abandono progresivo de la vía intratorácica (Kim, et al., 2020).
Nuevos avances
A.- Procesamiento de la Imagen
Cada vez se mejora más la capacidad de obtención de imágenes para exportarlas a una pantalla, registrarlas y manipularlas, con mejor resolución, luminosidad, menor relación señal/ruido y mayor rapidez de refresco de la imagen.
(Basil, et al., 2021).Destacando la visualización de alta definición (HD), desde 2007.
B.- Fluorescencia
También se están incorporando a las técnicas endoscópicas la Fluorescencia a 5-ALA, Verde Indiocianina y Fluoresceina intratecal, con la finalidad de distinguir mejor las estructuras durales (más vascularizadas) y para reparación de fístulas de LCR.
C.- Imagen 3D
La idea es permitir una mejor percepción de profundidad. El equipo consta de, al menos, dos cámaras orientadas en ángulos diferentes. Se precisan gafas especiales. La cámara izquierda proyecta sobre el ojo izquierdo y la cámara derecha, sobre el ojo derecho. También se pueden utilizar equipos de realidad virtual.
Pero tiene el inconveniente de que la periferia de la imagen está fuera de foco o incluso que el punto focal de las dos cámaras no coincide exactamente con la distancia real. Lo que hace que la orientación intraoperatopria del cirujano sea difícil, aunque la visión de los ayudantes sea aparentemente mucho mejor.
El futuro de la endoscopia espinal pasará por la mejoría en la instrumentación, navegación 3D y robótica (Kim, et al., 2020). En este sentido, la aplicación del robot como brazo de sostén del endoscopio puede ser un gran avance. En cirugía craneal lo hemos utilizado y supone un gran alivio, con liberación de las manos del cirujano y ayudante (ver https://neurorgs.net/?s=robot) (Fig. 6).
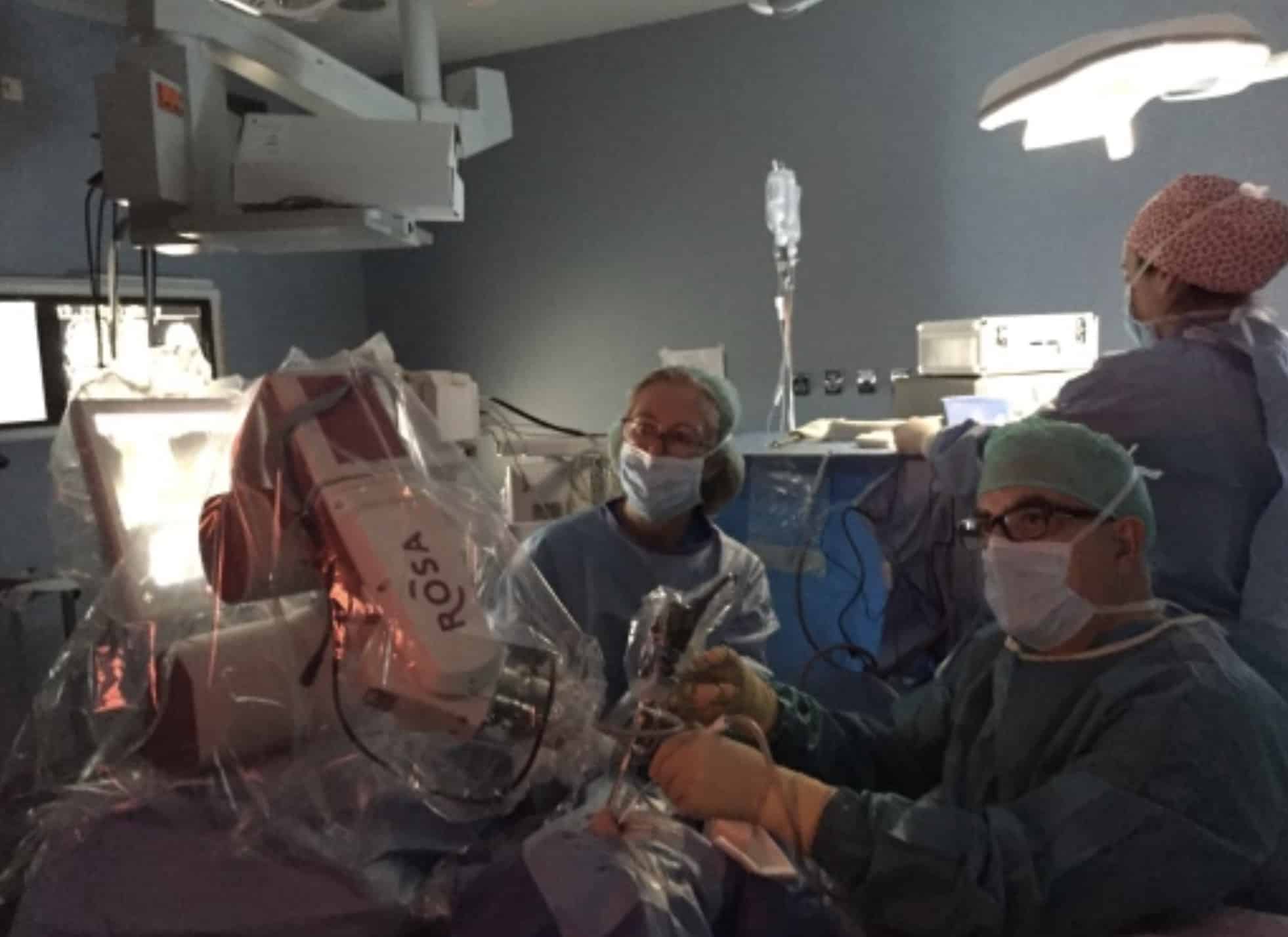
Exoscopia
Hay muchos tipos. Hablaremos de los que hemos tenido ocasión de probar en el Laboratorio de Anatomía Quirúrgica (en cirugía craneoencefálica y de raquis), en cadáver (Synaptive, Kinevo) o en el quirófano real (Storz).
Hay que partir de la base de que se trata de equipos y forma de operar totalmente diferentes al microscopio o endoscopio. La sensación es que, mientras éstos han sido diseñados gracias a la presión de los cirujanos, los exoscopios se nos presentan como una brillante idea de ingeniería a la que el cirujano se ha de adaptar.
Synaptive
La cámara está rodeada por cuatro fuentes de luz LED. Permite una muy buena calidad de imagen. Está montada sobre un pie robotizado que, además, puede neuronavegar. De manera que permite movimientos automáticos o controlados de la cámara, a manos libres. Guiados, por ejemplo, por la posición del aspirador o de la pinza bipolar, a los que se les ha colocado detectores para las cámaras del neuronavegador. De manera que se mantiene la posibilidad de un autofoco del campo quirúrgico.
Puede llegar a zonas quirúrgicas que no llega el microscopio convencional.
Tiene una distancia de trabajo de hasta 65cm. Y una capacidad de zoom de 12’5. Una gran pantalla-monitor 4K ofrece una imagen óptima del campo quirúrgico.
Pero tiene varios inconvenientes (Muhammad, et al., 2019): 1.- La percepción de profundidad es pobre, lo que precisa entrenamiento previo. 2.- Otro detalle a tener en cuenta es la necesidad de conseguir un campo quirúrgico exangüe, para que no se pierda la percepción en profundidad que depende de la textura y colores de las estructuras.
La gran pantalla externa atrae la atención del personal, lo que hace que la intervención sea más interactiva con el ayudante quirúrgico, enfermeras y anestesistas. (Fig 7).
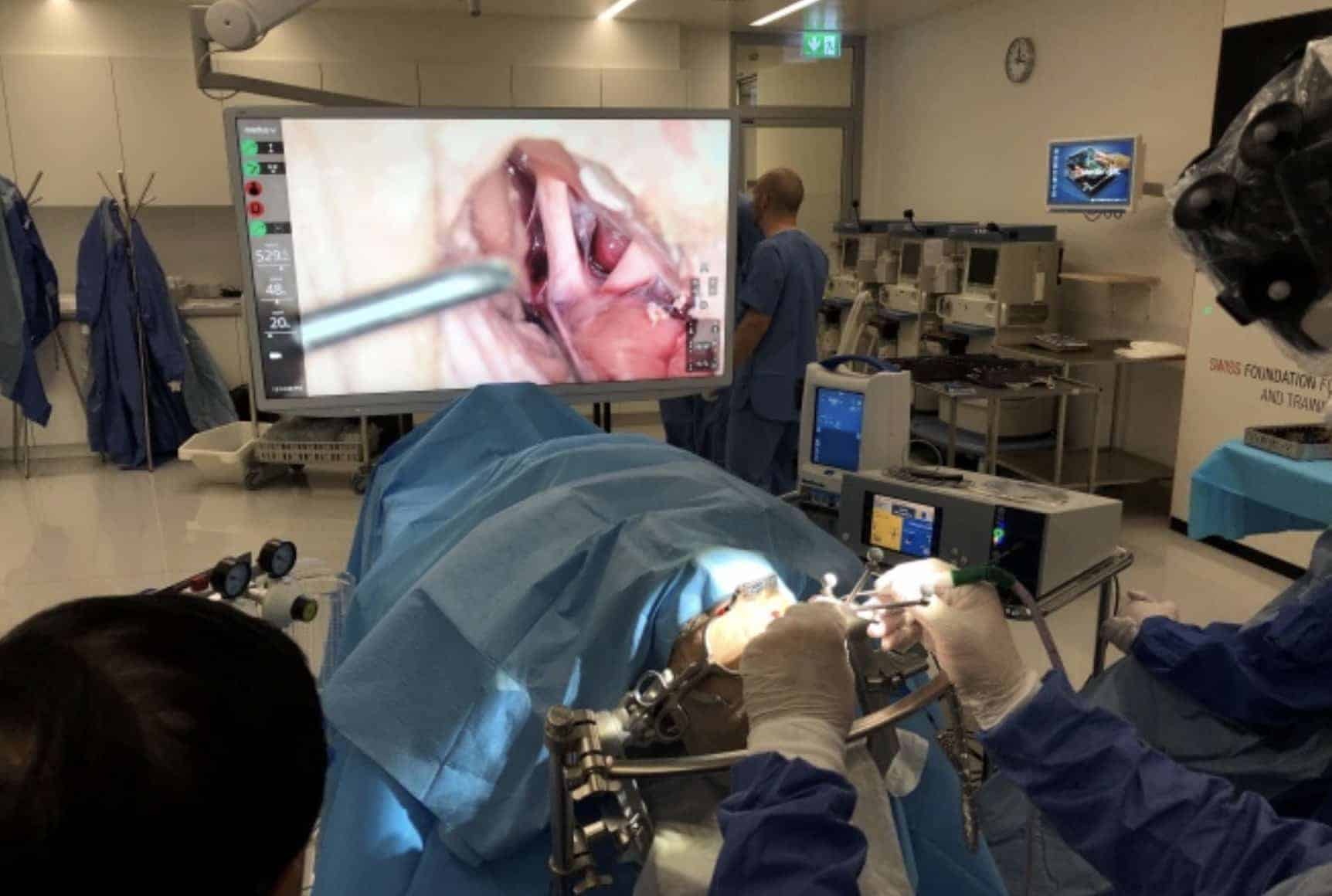
Kinevo-Brainlab
Zeiss, en combinación con BrainLab ha lanzado también su exoscopio (Kinevo). Con posibilidad de reconvertirlo inmediatamente, en cualquier momento, en un microscopio. El conjunto de oculares y cámara está montado también sobre un brazo robotizado y con capacidad de neuronavegar. A lo que se añade la posibilidad de un pequeño terminal endoscópico de exploración.
Es interesante su éxito en el mercado, puesto que mejora la capacidad técnica los equipos microquirúrgicos precedentes de la misma marca. Pero no se habla aún mucho de su capacidad “exoscópica” (Fig. 8).
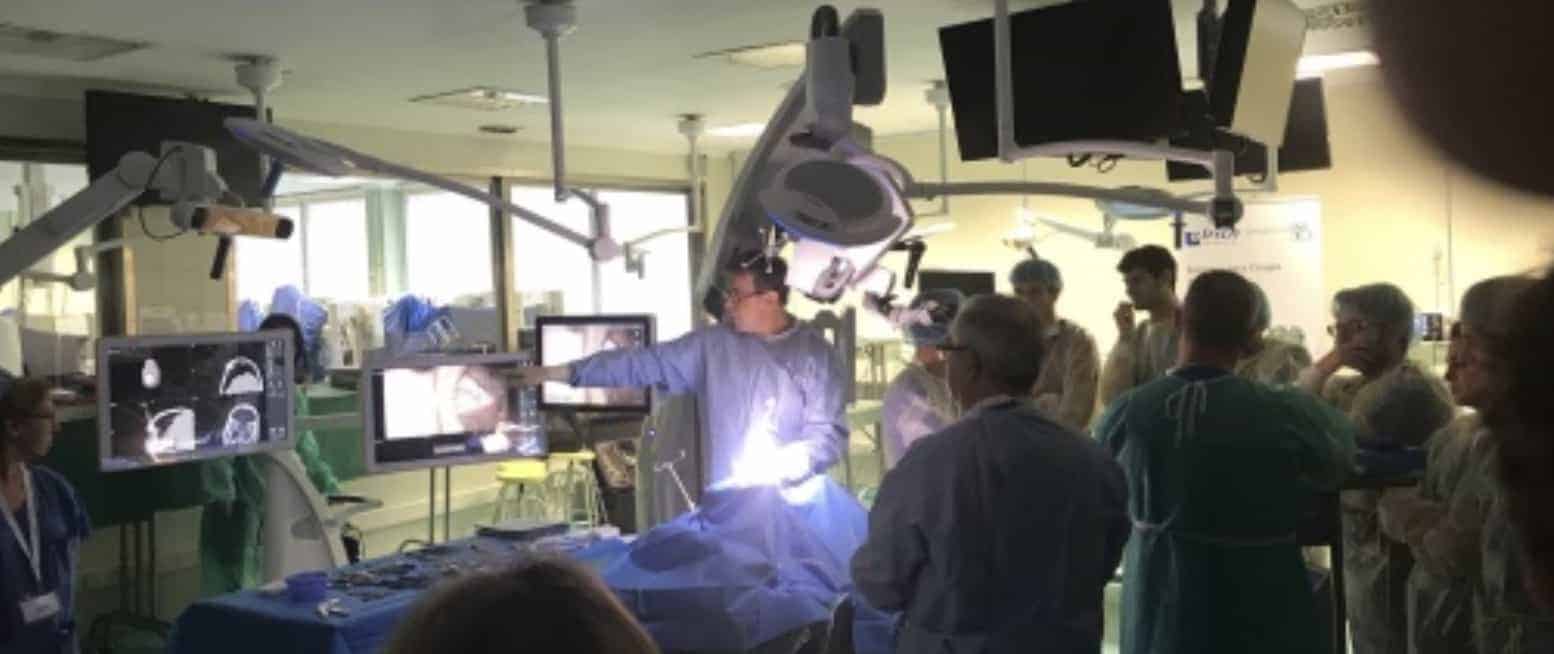
Vitom
Storz ofrece dos posibilidades, más sencillas. El exoscopio 2D, montado sobre un brazo mecánico, sujeto a la mesa quirúrgica. Muy útil como equipo para docencia.
Al ir conectado a los equipos de luz y pantallas de endoscopia, facilita mucho la vía de aprendizaje.
En nuestro entorno lo estamos utilizando en dos circunstancias:
-
1.- Como equipo de docencia, durante la realización de técnicas quirúrgicas en cadáver, en los Cursos que se están realizando en la Facultad de Medicina de la UAM y en la institución IAVANTE, en Granada Fig. 9).
2.- En nuestro quirófano, para grabar las aperturas quirúrgicas (Fig. 10).
En ambos casos, se utiliza como fase de aprendizaje para ir adquiriendo habilidad en el manejo del instrumental quirúrgico con este tipo de visión.
El exoscopio 3D, VITOM-3D presenta las mismas limitaciones que las referidas con el endoscopio 3D.
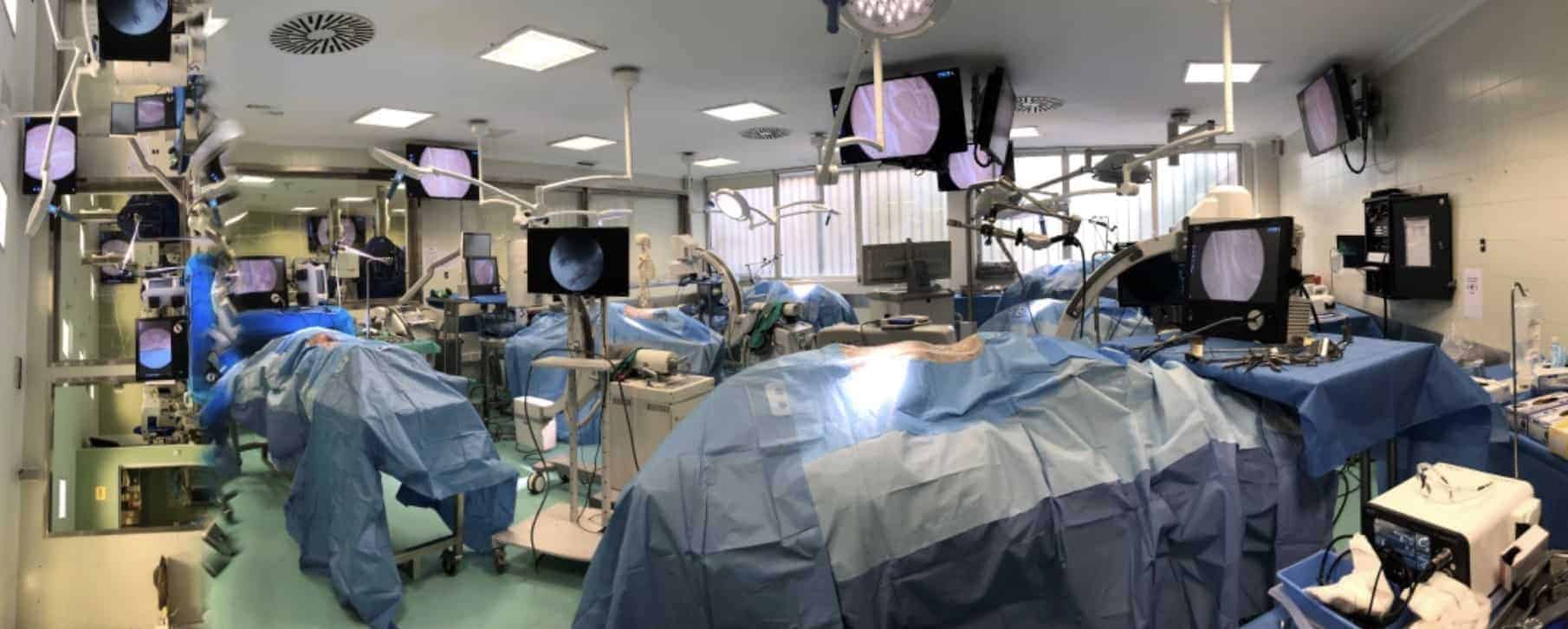
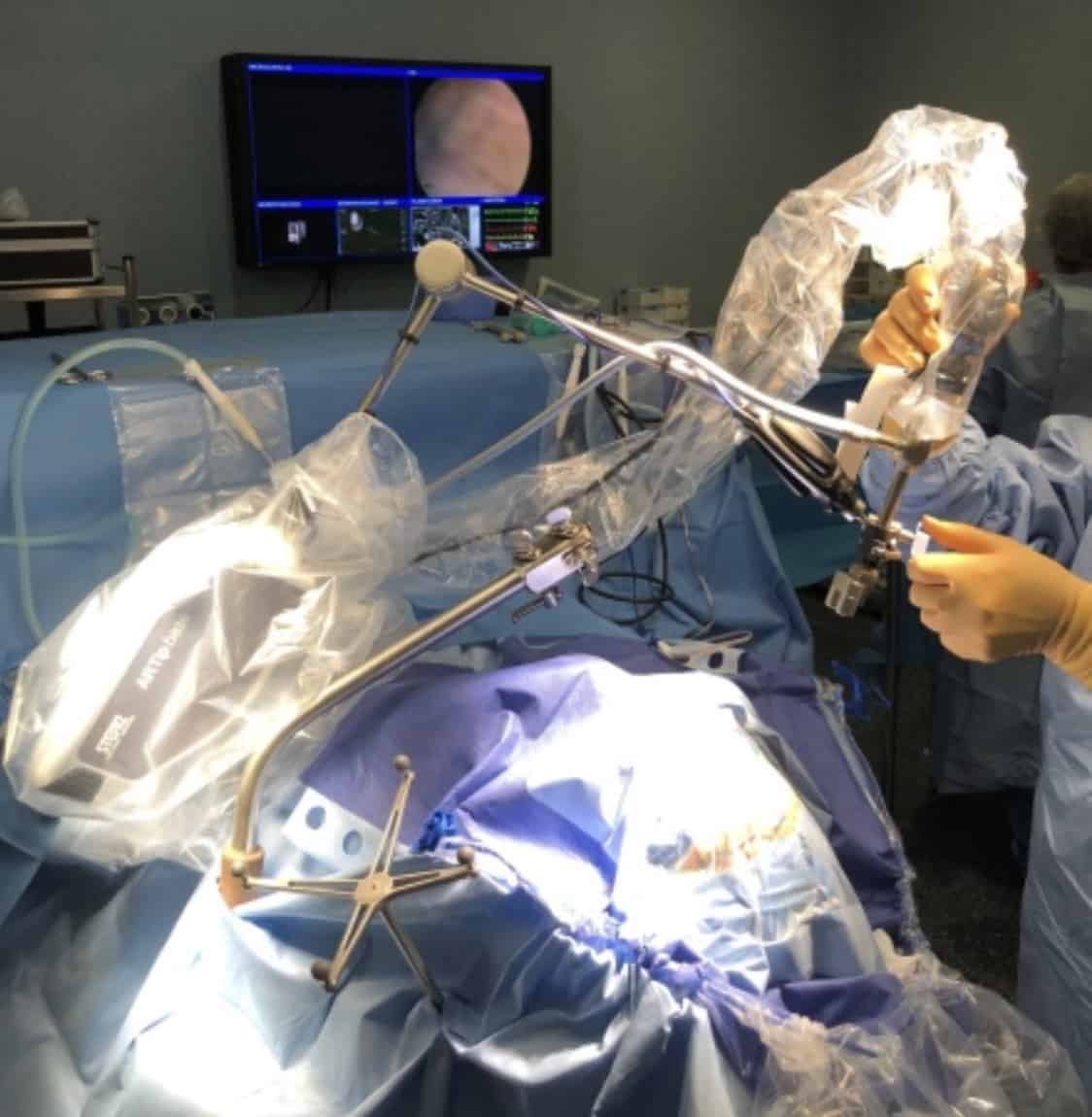
Futuro
La fusión de imágenes de RM y TAC preoperatorio, junto con las imágenes de TAC intraoperatorio, permite conjugarlas con las imágenes del microscopio. Incluso inyectar dichas imágenes en el campo de visión del cirujano (Carl, et al., 2019). Con ideas similares a los pioneros de esta tecnología de realidad aumentada, aplicada a la cirugía craneal (Pulido y Sola, 1996).
El objetivo es llevar a cabo una técnica quirúrgica guiada por la imagen (Ma, et al., 2021), en combinación con los equipos de neuronavegación.
Para esto se precisa generar, en primer lugar, las imágenes virtuales obtenidas en 3D de las imágenes preoperatorias. En el caso de cirugía de raquis, conjugarlas con las imágenes 3D intraoperatorias. En segundo lugar, hay que combinar adecuadamente dichas imágenes en 3D con la situación anatómica real. Esto se puede hacer en un monitor externo , en inyección en la óptica del microscopio y con otros dispositivos (gafas), superficies transparentes, etc.
Hay muchas vías para la fantasía y nuevos desarrollos: 1.- Imágenes 3D de gran precisión, para trabajar en profundidad. 2.- Adaptación del brazo robótico a instrumentos, para acompañas al cirujano, como lo hace un buen ayudante. 3.- Los quirófanos han de ser diseñados con mayor tamaño, para incorporar toda esta tecnología (Neuronavegador, TAC, Pantallas…). 4.- Maduración de las técnicas de realidad virtual, con generación de otros dispositivos interactivos con los equipos ya existentes. 5.- Integración de imágenes quirúrgicas: NFL, NNV, TAC. Con entorno wifi que suprima cableado y de amplia libertad a la colocación de los equipos alrededor del paciente-cirujano…
Reflexiones
Por un lado, pocos neurocirujanos son entrenados en técnicas endoscópicas espinales durante su residencia (Teleian, et al., 2016).
Mas todos hablan de curva de aprendizaje, mayor a medida que las técnicas son más complejas. Esto está ligado a complicaciones que, a veces, no son claramente descritas.
Qué hacer? Lo mejor, tener una mente abierta. Ir a la penúltima moda. Hay que sopesar la demanda real que se va a tener. Y la necesidad de modificar las técnicas que se dominan, con muy buenos resultados.
En caso de decidir aplicar técnicas endoscópicas, ir de técnicas menos complejas (abordaje endoscópico interlaminar) hacia más complejas (abordaje endoscópico biportal para fusión intersomática). Pero no abandonar el microscopio.
Dar paso al exoscopio, como ayuda a las técnicas a cielo abierto.
En resumen, el cirujano se ha de entrenar en los tres tipos de visión y adaptarlos a cada diseño quirúrgico. Incluso tener la posibilidad de intercambio entre éstos durante la misma intervención quirúrgica.
Todo lo anterior ha de pasar por un entrenamiento quirúrgico en cadáver, en los Departamentos de Anatomía de las Facultades de Medicina.
Otro aspecto muy importante es tener un quirófano altamente dotado. Podría ser, por ejemplo, una gran incongruencia abordar técnicas complejas y de alto coste, como es el robot, con una dotación simple de un arco de Rx 2D convencional y sin mesa específica para cirugía de columna.
Por último, no caer en la tentación de empeñarnos en ser los mejores porque hacemos lo más difícil. Y sí hacer hincapié en que hay que revisar y publicar los resultados reales propios, desde el primer caso que se lleve a cabo.
Bibliografia
Basil GW, Kumar V, Wang MY. Optimizing visualization in endoscopic spine surgery. Operative Neurosurgery 2021. Vol 21. Suppl 1. S59-S66.
Basques B, Golinvaux NS, Bohi DD, et al. Use of an operating microscope during spine surgery is associated with minor increases in operating room times and no increased risk of infection. Spine (Phila Pa 1976) 2014, 39: 1910-1916.
Carl B, Bopp M, Sabβ , Nimsky C. Microscope-based augmented reality in degenerative spine surgery: initial experience. World Neurosurgery 2019, 28: E541-E551
Choi KC, Shim HK, Hwang JS, et al. Comparison of surgical invasiveness between microdiscectomy and 3 different endoscopic discectomy techniques for lumbar disc herniation. World Neurosurg 2018, 116: e750-e758.
Delgado-Fernández J, Pulido Rivas P, García de Sola R, et al. Long term outcome and fusion rate of transdiscal fixation for L5-S1 high grade spondylolisthesis. Clinical Neurology and Neurosurgery 2021, 208: 1-8.
García de Sola R. Infraestructura convencional de un quirófano para cirugía raquimedular. En: Cirugía Raquimedular (García de sola, et al., Eds). Viguera Ed. Barcelona. 2014. Pp 123- 130.
García de Sola R. Tumores Intramedulares. En: Cirugía Raquimedular (García de sola, et al., Eds). Viguera Ed. Barcelona. 2014. Pp 1111-1128.
He J, Xiao S, Wu Z, Yuan Z. Microendoscopic discectomy versus open discectomy for lumbar disc herniation: a meta-analysis. Eur Spine J 2016, 25: 1373-1381
Kang MS, Yiou KH, Choi JY, et al. Minimally invasive transforaminal lumbar interbody fusion using the biportal endoscopic techniques versus microscopic tubular technique. The Spinal Journal 2021, 21: 2066-2077.
Kim SK, Kang SS, Hong YH, et al. Clinical comparison of unilateral biportal endoscopic technique versus open microdiscectomy for single-level lumbar discectomy: a ulticenter, retrospective analysis. J Orthop Surg Res 2018, 13: 22, 1-8.
Kim HS, Wu PH, Jang IT. Current and future of endoscopic spine surgery: What are the common procedures we have now and what lies ahead?. World Neurosurg 2020, 140: 642-653.
Lin Y, Rao S, Li Y et al. Posterior percutaneous full-endoscopic cervical laminectomy and decompression for cervical stenosis with myelopathy: a technical note. World Neurosurg. 2019, 124:350-357.
Ma L, Fei B. Comprehensive review of surgical microscopes: technology development and medical applications. J Biomed Optics 2021, 26: 010901, 1-74.
Mayer HM. A history of endoscopic lumbar spine surgery: what have we learnt?. BioMed Res Internat 2019, 4583943: 1-8.
Muhammad s, Lehecka M, Niemelä. Preliminary experience with a digital robotic exoscope in cranial and spinal surgery: a review of the Synaptive Modus V system. Acta Nerochirurgica 2019, 161: 2175-2180.
Park SM, Siong KS, Park SY, et al., Comparing the efficacy and safety of minimally invasive biportal endoscopic spine surgery versus conventional microscopic discectomy in single-level lumbar herniated intervertebral disc (ENDO-BH Trial): a multicenter, prospective, randomized controlled equivalence trial study protocol. BMC 2022, 23:172, 1-9. https://doi.org/10.1186/s13063-022-06094-2.
Perez-Cruet MJ, Foley KT, Isaacs RE, et al. Microendoscopic lumbar discectomy: technical note. Neurosurgery 2002, 51: S129-S136.
Pulido Rivas P, Sola RG. Localización anatomo-funcional en la corteza cerebral. Aplicación de un sistema de integración de imáge¬nes como guía para la resección de lesiones cerebrales corticales. Rev Neurol. 1996; 24 Suppl 1:S5-61.
Pulido Rivas, P. Neuronavegador. En: Cirugía Raquimedular (García de sola, et al., Eds). Viguera Ed. Barcelona. 2014. Pp 143-151.
Pulido Rivas P.. Cirugía del raquis guiada por imagen 3D. En: Cirugía Raquimedular (García de sola, et al., Eds). Viguera Ed. Barcelona. 2014. Pp 179-190.
Reutten S, Komp M, MeRk H, Godolias G. A new full-endoscopictechnique for cervical posterior foraminotomy in the treatment of lateral disc herniations using 6.9mm endoscopes: prospective 2-years results of 87 patients. Minim Invasive Neurosurg 2007, 50: 219-226.
Telfeian AE, Veeravagu AV, Oyelese AA, Gokasian ZL. A brief history of endoscope spine surgery. Neurosurgical Focus 2016, 40: E2.
Uluç K, Kujoth GC, Baskaya MK. Operating microscopes: past, present and future. Neurosurg Focus 2009, 27: E4.
Yasargil MG. Microsurgical operation of herniated lumbar disc. En: Advances in Neurosurgery. Vol 4. Lumbar Disc – Adult Hydrocephalus. Springer. Berlin. 1977 pp 81-91.