HIPERTENSION INTRACRANEAL. HIDROCEFALIA.
Tema I: Temario de Neurocirugía 2020 para alumnos de Facultad de Medicina de la UAM: 2020
Facultad de Medicina de la Universidad Autónoma de Madrid.
Directores:
PARTE I: INTRODUCCIÓN A LA NEUROCIRUGÍA
(nota para el alumno: opcional pero se recomienda leer)
CONCEPTO DE SISTEMA NERVIOSO
El sistema nervioso es el conjunto de estructuras que dirige y regula el funcionamiento correcto del organismo. Dentro de la escala de evolución de las especies, es el sistema o estructura más evolucionada de la Naturaleza y extraordinariamente complejo.
Clásicamente se le divide en tres partes:
1.- Sistema Nervioso Central (SNC)
Compuesto por encéfalo y médula espinal; a su vez, el encéfalo está compuesto por el cerebro, estructuras talámicas, tronco cerebral y cerebelo.
El cerebro es la parte más evolucionada y comprende la corteza cerebral, donde se sitúan las neuronas que van a realizar las funciones más conscientes del individuo (inteligencia, memoria, movilidad, sensibilidad, lenguaje, visión, etc.). Las neuronas se ordenan en láminas. Y las estructuras subcorticales, más en profundidad, donde se sitúan las neuronas, ordenadas en núcleos, que realizan funciones más automáticas (coordinación de movimientos, por ejemplo).
El tálamo, subtálamo e hipotálamo están constituidos por conjuntos de núcleos de neuronas cuya función es servir de conexión en la elaboración de la información desde el cerebro al resto de las estructuras encefálicas y viceversa. Las funciones que regulan son múltiples, desde la información sensitiva y sensorial, incluyendo la información dolorosa, a los controles de comportamientos fundamentales para el funcionamiento del organismo, como puede ser la sensación de hambre o de sed.
El cerebelo está más en relación con la coordinación de movimientos y está en íntima interconexión con el tálamo y núcleos subcorticales. Tiene, como la corteza cerebral, una estructura superficial cortical y una estructura profunda nuclear.
El tronco cerebral es una zona obligada de paso entre encéfalo y médula espinal. Pero además tiene núcleos y redes neuronales (substancia reticular) que mantienen funciones vitales como la respiración, el ritmo cardíaco o la conciencia.
La médula espinal, alojada ya fuera del cráneo y dentro del canal vertebral, está formada por las vías nerviosas que vienen y van hacia el encéfalo. Y además tiene una estructura neuronal diferente (astas y substancia reticular) que recibe y emite información desde la periferia, así como ejecuta las órdenes que le envía el encéfalo.
2.- Sistema Nervioso Periférico (SNP)
Lo constituyen los nervios craneales que salen del tronco cerebral, las raíces nerviosas que salen de la médula espinal y los nervios periféricos que se forman a partir de la unión o como continuación de las raíces nerviosas medulares. Este sistema de cableado es ya más simple y tiene fundamentalmente tres tipos de fibras nerviosas: dolorosas, sensitivas y motoras. Todas estas fibras son prolongaciones de las neuronas que se localizan a nivel de la médula o del tronco cerebral.
3.- Sistema Nervioso Autónomo (SNA)
Es algo más complejo que el anterior y está a caballo entre el Central y el Periférico. Las neuronas o grupos neuronales que lo constituyen están a nivel del tronco cerebral y al final de la médula espinal (parasimpático); y en una cadena de ganglios situados por fuera de la médula, aunque en estrecha conexión con ella (simpático). Es el que mantiene el correcto funcionamiento de órganos como el aparato digestivo, corazón, respiración, función sexual, etc., adaptándolos de forma automática a las situaciones que percibe el Sistema Nervioso Central.
CONCEPTO DE NEUROCIRUGÍA
La Neurocirugía (NCR) es la ciencia médica que estudia las enfermedades que afectan al Sistema Nervioso que requieren o pueden requerir un tratamiento quirúrgico en algún momento de su evolución.
Por tanto, tiene una conexión muy estrecha con la Neurología, puesto que muchas de las enfermedades a estudiar y tratar son comunes para ambas especialidades.
El tratamiento quirúrgico se realiza en lugares muy específicos del hospital, requiriendo una infraestructura de quirófanos, anestesia y reanimación, así como unidades de cuidados intensivos, que son también compartidas con otras especialidades quirúrgicas y médicas.
Pero además, precisa de otros recursos humanos e infraestructura hospitalaria que los aportan otras especialidades o subespecialidades en relación con el Sistema Nervioso. Todas juntas forman el grupo de las Neurociencias Clínicas.
NEUROCIENCIAS
En un Hospital de alto nivel tecnológico, como para poder acoger a la Neurocirugía, se precisa la existencia y correcto funcionamiento de multitud de especialidades. Su calidad asistencial repercutirá de forma muy directa sobre la calidad y nivel científico de la propia Neurocirugía. Aunque ya han recibido o van a recibir una información más completa, directamente de los especialistas, vamos a destacar los campos más conectados con la Neurocirugía:
1.- NEUROLOGÍA (NRL):
Es la especialidad encargada del estudio y tratamiento de las enfermedades del Sistema Nervioso. Es muy amplio el campo que abarca y va desde el diagnóstico clínico y tratamiento médico de enfermedades muy comunes, como la epilepsia, enfermedad de Parkinson, Alzheimer, cefaleas, infarto cerebral… a la generación de líneas de actuación e investigación clínica muy complejas en patologías muy precisas, en las que puede estar implicada también la Neurocirugía: Tratamiento quirúrgico de la Epilepsia, de la Enfermedad de Parkinson, Ictus-Accidente Cerebrovascular, Dolor …
Aunque hay una sola especialidad, en el momento actual hay dos campos claramente delimitados: Neurología Pediátrica (Neuropediatría) y Neurología de Adultos. Debido a la alta complejidad de los problemas a tratar, por lo general dentro de cada equipo o Servicio, dependiendo de su capacidad asistencial, suele haber especialistas en Neurología dedicados más intensamente a algún tipo de patología: Trastornos del Movimiento, Enfermedades Degenerativas, Unidad de Ictus Cerebral, Epilepsia, Cefaleas…
2.- NEUROFISIOLOGÍA:
La Neurofisiología Clínica (NFL) se define como una especialidad médica que, fundamentada en los conocimientos de la Neurociencias básicas, tiene como objetivo la exploración funcional del SN central, periférico y autónomo, utilizando tecnología altamente especializada con fines diagnósticos, pronósticos y orientación terapéutica. En el momento actual, la tecnología dominante se centra en el registro directo o indirecto, conversión, procesamiento y análisis de los fenómenos bioeléctricos de los sistemas mencionados. Se incluyen también aquellas técnicas que, aunque en periodo de desarrollo, permiten el análisis cuantitativo de variables neurobiológicas de aplicación clínica. La NFL, por tanto, es el conjunto de técnicas de estudio y valoración de las funciones fisiológicas y patológicas del SN (central, periférico, vegetativo) y aparato muscular.
Las técnicas exploratorias a las que nos vamos a referir a continuación son las que van a estar en estrecha conexión con la Neurocirugía y pueden dividirse en varios apartados:
a) Técnicas de realización ambulatoria
Se llevan a cabo en el gabinete o consulta de Neurofisiología:
a. Electroencefalografía.- Las siglas que lo definen son: EEG. Consiste en el registro de la actividad eléctrica neuronal de la corteza cerebral. Hoy día es una técnica muy sofisticada y, además de los trazados convencionales, se utilizan otras herramientas analíticas más complicadas, gracias a la aplicación de ordenadores potentes y software apropiado. Destacan:
i. Mapas de actividad eléctrica cerebral (mapping).- Pueden ser de voltaje o de frecuencia. Resultan muy útiles para obtener información relevante que se escapa a la inspección visual clásica.
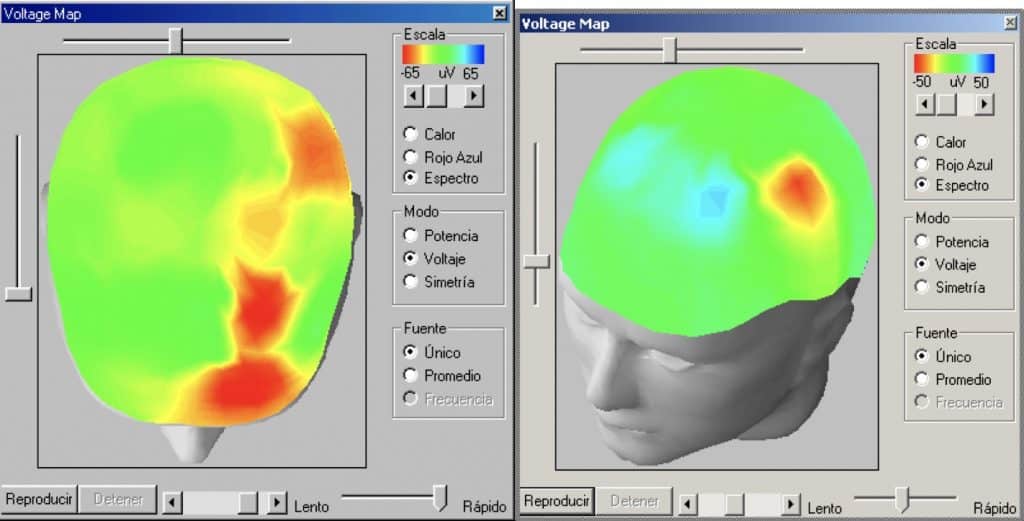
ii. Estudio de Dipolos.- Consiste en calcular de forma tridimensional, el punto de la esfera cerebral donde se sitúa un teórico dipolo eléctrico que produciría la alteración eléctrica que se observa en el EEG convencional. Es útil en el estudio de la epilepsia focal con posibilidades quirúrgicas.
b. Electromiografía (EMG) y electroneurografía (ENG).- Estudian la fisiología y fisiopatología del nervio periférico, el músculo y la unión neuromuscular. Es útil para diagnosticar enfermedades neuroquirúrgicas que afecten a las raíces que salen de la médula (hernias discales, tumores…), en enfermedades de los propios nervios periféricos (traumatismos, tumores…) y para seguir la evolución de afectaciones nerviosas periféricas, tras la intervención quirúrgica reparadora o tras accidente espontáneo o quirúrgico (por ejemplo, la parálisis del nervio facial).
c. Potenciales Evocados.- La finalidad es estudiar la integridad o la existencia de anomalías en la funcionalidad de determinados sistemas sensoriales o vías del sistema nervioso. Consiste esencialmente en dar un estímulo conocido y observar la respuesta al final del circuito. Dependiendo de cómo sea dicha respuesta, el neurofisiólogo nos puede decir qué zona de dicho circuito está alterada. Hay varios tipos de potenciales evocados:
i. Visuales.- Las siglas que lo definen son: PEV. Se estimula la retina, mediante la emisión de un determinado tipo de luz y se recoge la actividad eléctrica de la corteza cerebral occipital. Estudia el estado de la retina, nervios ópticos, quiasma, vía óptica y corteza cerebral occipital.
ii. Auditivos.- Las siglas que lo definen son: PEAT. Se estimula el oído, mediante la emisión de un sonido determinado y se recoge la actividad eléctrica de la corteza cerebral auditiva. Estudia el estado de cóclea, nervio auditivo, tronco cerebral, vía auditiva y corteza cerebral temporal.
iii. Somatosensoriales.- Las siglas que lo definen son: PESS. Se estimula un nervio periférico, mediante un estimulo eléctrico determinado, y se recoge la actividad eléctrica de la corteza cerebral parietal. Estudia el estado de los nervios periféricos, raíces medulares, médula, vía sensitiva y corteza cerebral parietal.
iv. Motores.- Las siglas que lo definen son: PEM. Se estimula la corteza cerebral motora, mediante un estímulo eléctrico transcraneal y se recoge la actividad motora periférica mediante un EMG. Estudia el estado de la corteza motora frontal, vía piramidal motora, médula, raíces y nervios periféricos.
b) Técnicas complejas de EEG
Precisan una estancia más prolongada en el Hospital:
a. Estudios polisomnográficos (PSG).- El paciente ha de permanecer varias horas en estudio, mientras le realizan una polisomnografía que incluye estudio EEG (para el análisis del sueño) y otros parámetros como son las variables respiratorias, EMG o ECG. Estos estudios son de gran importancia en diversas patologías como la epilepsia o los trastornos del sueño.
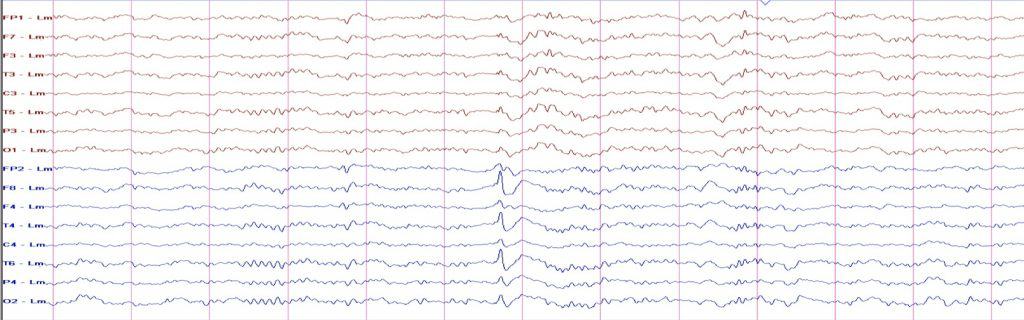
b. EEG activado mediante el sueño.- Tanto el sueño, como la falta del mismo, son potentes activadores de las manifestaciones irritativas del córtex cerebral. Por ello, esta modalidad de EEG resulta muy importante en estudios de pacientes epilépticos con una tasa baja de actividad interictal. El paciente acude tras haber pasado una noche sin dormir.
c. Video-EEG (v-EEG).- Mientras se realiza el EEG, de forma simultánea y sincronizada se está recogiendo la imagen en video del paciente. Su aplicación fundamental es en el diagnóstico de la epilepsia, aunque resulta fundamental para filiar otro tipo de manifestaciones paroxísticas de los pacientes, como son las pseudocrisis o crisis no epilépticas, con apariencia de epilepsia. Permite recoger la actividad clínica y eléctrica simultánea durante una crisis epiléptica. Este tipo de estudio necesita el ingreso hospitalario, al menos 24-48 horas, dependiendo de la intensidad y frecuencia de crisis epilépticas que se tengan. Puede ser de dos tipos: v-EEG no invasivo (con electrodos de scalp) y v-EEG invasivo (ver a continuación). La idea en ambos casos es la misma, aunque varía el grado de agresividad o riesgo del estudio.
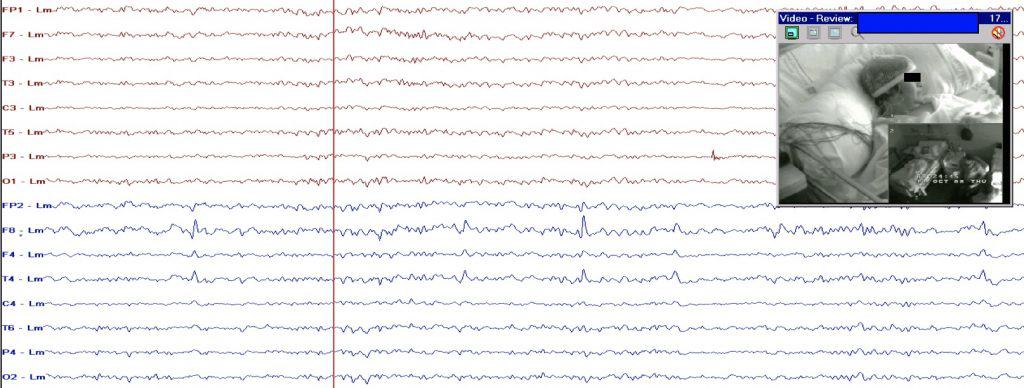
c) Técnicas invasivas de EEG
Consisten en la implantación de electrodos intracraneales, mediante la adecuada intervención quirúrgica. Con los electrodos implantados, se realiza a continuación un estudio v-EEG.
Se aplica exclusivamente en pacientes epilépticos graves que tienen posibilidades quirúrgicas. Los electrodos se colocan sobre o cerca de la zona que teóricamente produce la crisis epiléptica y el objetivo es conseguir el registro del inicio de dicha crisis y toda la actividad cerebral, eléctrica y clínica, que se produce a continuación. Además es preciso analizar con detenimiento la actividad interictal y otras manifestaciones clínicas funcionales. Únicamente cuando todas estas facetas se engarzan en un todo coherente, se considera correctamente identificado el foco epiléptico. Se obtiene así un mapa muy claro de la zona de corteza cerebral que hay que extirpar para controlar la epilepsia. También se consigue (mediante técnicas de estimulación eléctrica en los electrodos y recogida de potenciales evocados) conocer la función de la zona que produce la epilepsia y de las zonas adyacentes. El objetivo es diseñar una intervención que cure la epilepsia, pero que respete funciones importantes cerebrales, de manera que no se altere la calidad de vida de la persona. Hay tres tipos fundamentales de electrodos intracraneales:
a. Electrodos del Foramen Oval.- Se introducen a través de un orificio de la base de cráneo (agujero oval), por donde sale la tercera rama del nervio trigémino, mediante una punción a través de la mejilla. Se trata de un electrodo de 1 mm de diámetro, que tiene varios contactos activos de platino, separados 1 cm. Se quedan colocados junto a la cara interna de ambos lóbulos temporales, que es la zona epileptógena más frecuente y con mejor pronóstico quirúrgico.
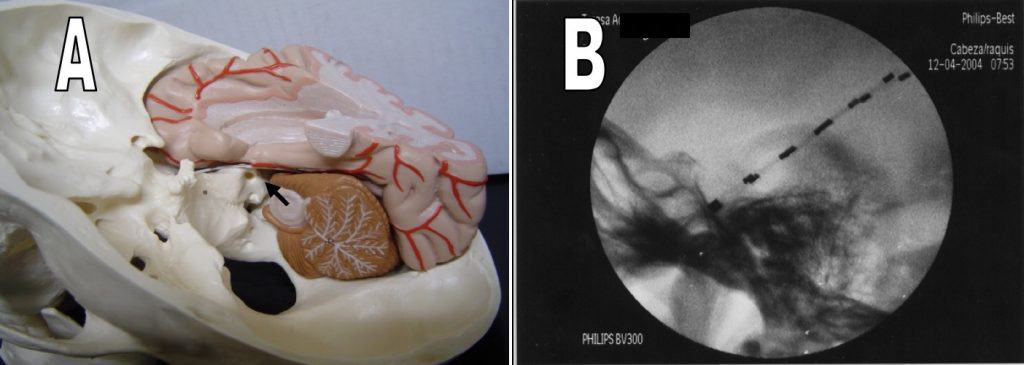
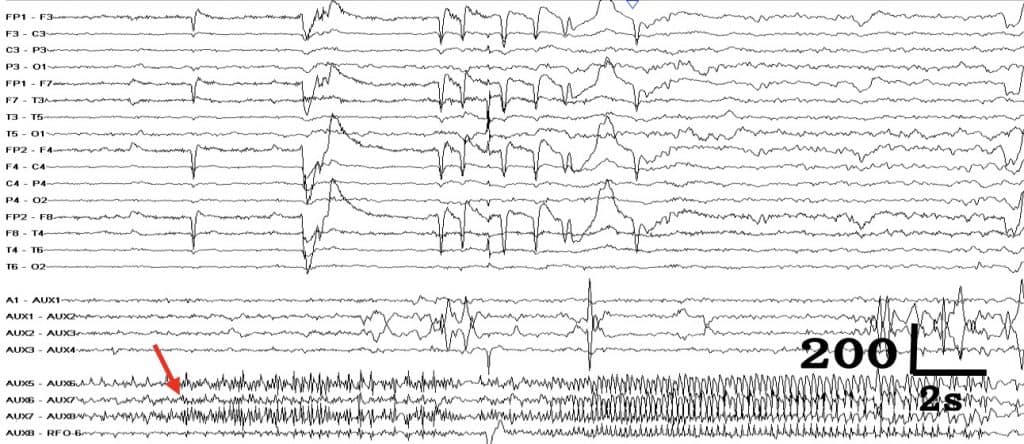
b. Electrodos subdurales.- Precisan la realización de una craneotomía. Es como una malla o “manta” de Silastic® (material muy elástico), que se adapta sobre la corteza cerebral. En dicha manta hay varios contactos circulares de platino, que recogen la actividad eléctrica. La forma puede ser desde una tira de 4 a 12 electrodos, separados 1 cm.; a un cuadrado o rectángulos de 4×5, 4×8, 8×8. Una vez colocados los electrodos, se cierra la craneotomía, se despierta al paciente y se le lleva a la sala de registro v-EEEG. Permiten, con bastante fidelidad, el estudio de la actividad eléctrica y de la función de la corteza cerebral (mediante estimulación eléctrica de estos electrodos).
En los últimos años se ha planteado la utilización de este tipo de exploración para conocer la función cerebral en pacientes con gliomas en zonas elocuentes de la corteza cerebral.
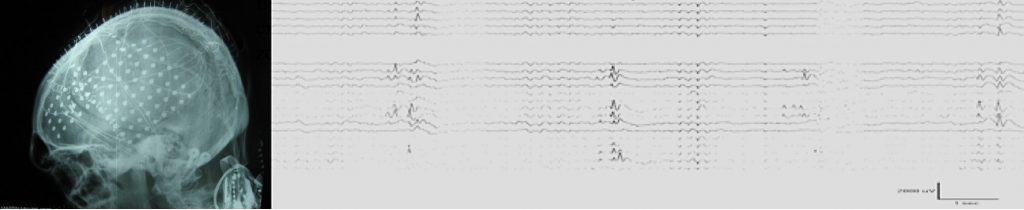
c. Electrodos profundos.- Son electrodos de 1-2mm de diámetro, que se introducen a través del cráneo mediante técnicas complejas estereotáxicas. Se alojan dentro del cerebro y se suelen colocar de forma ortogonal y paralela entre ellos. Permiten el estudio de zonas a las que no se llega con las anteriores técnicas, sobre todo las caras mediales hemisféricas. El EEG que se obtiene a través de registro con estos electrodos es un EEG tridimensional, muy complejo, pero necesario en epilepsias de alta dificultad diagnóstica.
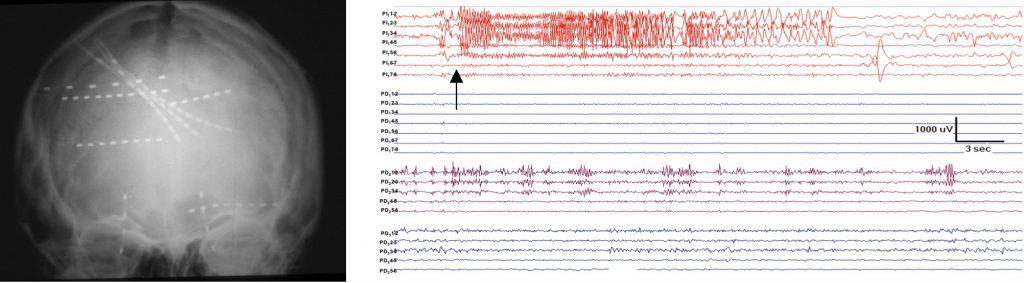
d) Mapeo cortical (Mapping)
En determinados pacientes es imprescindible identificar aquellas áreas corticales elocuentes que es imprescindible proteger durante la cirugía. Para ello se pueden realizar técnicas de estimulación cortical eléctrica, aplicando determinados trenes de estímulos a través de los electrodos subdurales, con el fin de observar los efectos que la corriente eléctrica tienen en esa región sobre la movilidad o sobre el lenguaje. La otra variante es el registro de potenciales evocados somatosensoriales, auditivos o visuales en los electrodos subdurales, para delimitar zonas sensoriales.
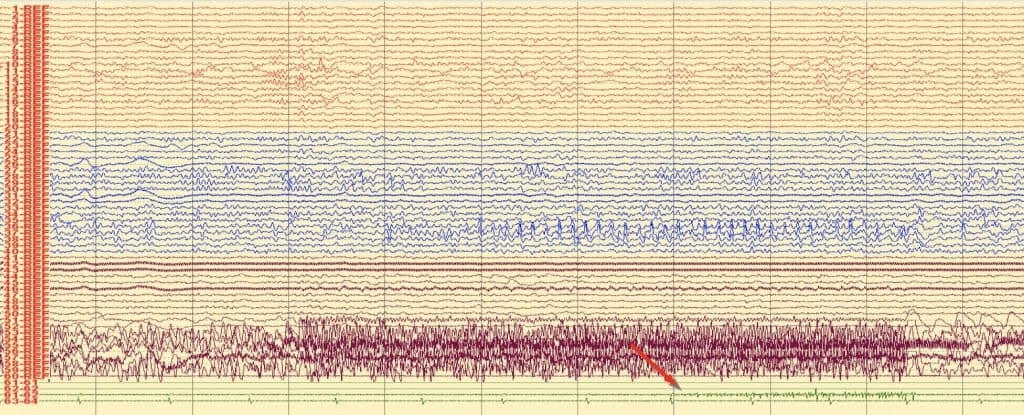
e) Técnicas de monitorización neurofisiológica intraoperatoria (MNIO)
Durante la intervención quirúrgica, podemos servirnos de las técnicas anteriores para conocer la función de las zonas próximas a la lesión quirúrgica que se pretende extirpar. Esto hace que el acto quirúrgico sea muy seguro. Estas técnicas se pueden llevar a cabo por el propio cirujano, co el paciente despierto. O, mejor, con ayuda de NFL, con el paciente despierto o anestesiado, dependiendo de la zona a intervenir y del protocolo o experiencia del equipo NCR-NFL. Entre estas técnicas, destacaremos:
a. Electrocorticografía (EcoG).- Consiste en el registro de la actividad eléctrica de la corteza cerebral. Se puede utilizar una manta de electrodos subdurales, que se coloca cubriendo la zona de corteza cerebral que hay que estudiar. A partir de aquí, se pueden hacer varios tipos de estudios:
i. Registro eléctrico.- Permite diferenciar zonas alteradas (tumor, por ejemplo) de zonas funcionales normales.
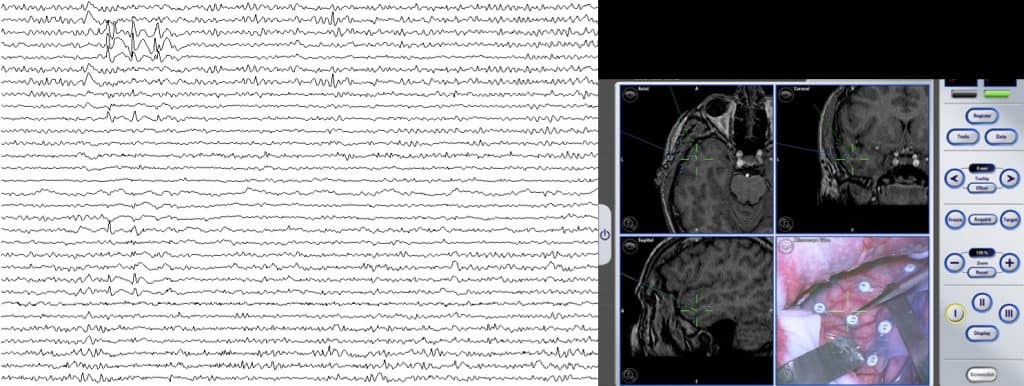
ii. Estimulación cortical motora.- El neurofisiólogo estimula los contactos de dichas mantas de electrodos. De esta forma se puede obtener respuesta motoras en las extremidades, visibles o registrables mediante un EMG.
iii. Potenciales evocados sensoriales.- PESS, PEV o PEAT. Igual que los PESS, solo que la actividad eléctrica es recogida en la manta de electrodos. Permite reconocer las zonas corticales sensoriales sensitivas, visuales o auditivas, respectivamente.
iv. Estimulación eléctrica de zonas del lenguaje.- Esta exploración ha de realizarse durante intervenciones en que el paciente puede estar despierto en el momento de la exploración. Se requiere un anestesista entrenado y un neuropsicólogo. El objetivo es identificar la zona de corteza cerebral que tiene algún tipo de función sobre el lenguaje, con la finalidad de respetarla durante el acto quirúrgico.
b. Potenciales evocados.- Las diferentes técnicas de potenciales evocados pueden realizarse durante el acto quirúrgico. Están indicados sobre todo en cirugía de la base de cráneo. Por ejemplo:
i. PEV.- En tumores que afecten los nervios ópticos o el quiasma (Meningiomas, craneofaringiomas, adenomas de hipófisis…). Evita que la manipulación excesiva del cirujano durante el acto quirúrgico provoque una lesión irreversible de la vía óptica. Así como observar lo contrario: cómo la extirpación cuidadosa va manteniendo la actividad de la vía óptica o incluso mejorándola.
ii. PEAT.- Se aplican en cirugía de la base de cráneo, a nivel de la fosa posterior (meningiomas, neurinomas del acústico…). Controla la actividad del nervio acústico, pero también la integridad del tronco cerebral, dado que se puede realizar bilateralmente. Es un control muy positivo, hoy día imprescindible, en este tipo de cirugía de alto riesgo.
iii. PESS.- Se utiliza, sobre todo, en cirugía de tumores intramedulares, por las mismas razones expuestas para las anteriores pruebas.
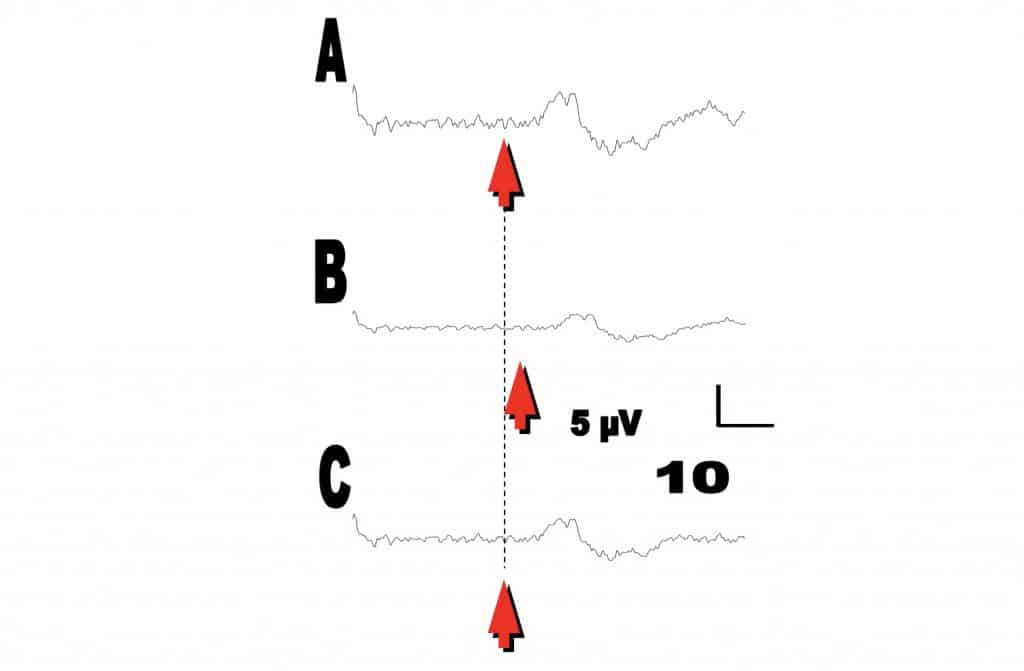
iv. PEM.- Permite conocer la vía motora. Se hace durante la cirugía medular y, junto a los PESS, permiten tener controlada una zona medular más amplia.
c. EMG.- El Neurofisiólogo puede tener controlado, mediante EMG, una gran cantidad de músculos, que depende de la función correcta de sus correspondientes nervios. Estos nervios pueden ser los pares craneales (oculomotores, facial y pares bajos [que controlan la deglución, la articulación de la palabra, el movimiento de hombro y lengua]) a nervios periféricos. El registro de la actividad espontáneo o tras estimulación, que hace el propio cirujano, permite impedir que la manipulación quirúrgica deteriore el funcionamiento de dicho nervio. Esta técnica es imprescindible en cirugía de tumores como el neurinoma del acústico o meningiomas de la base del cráneo.
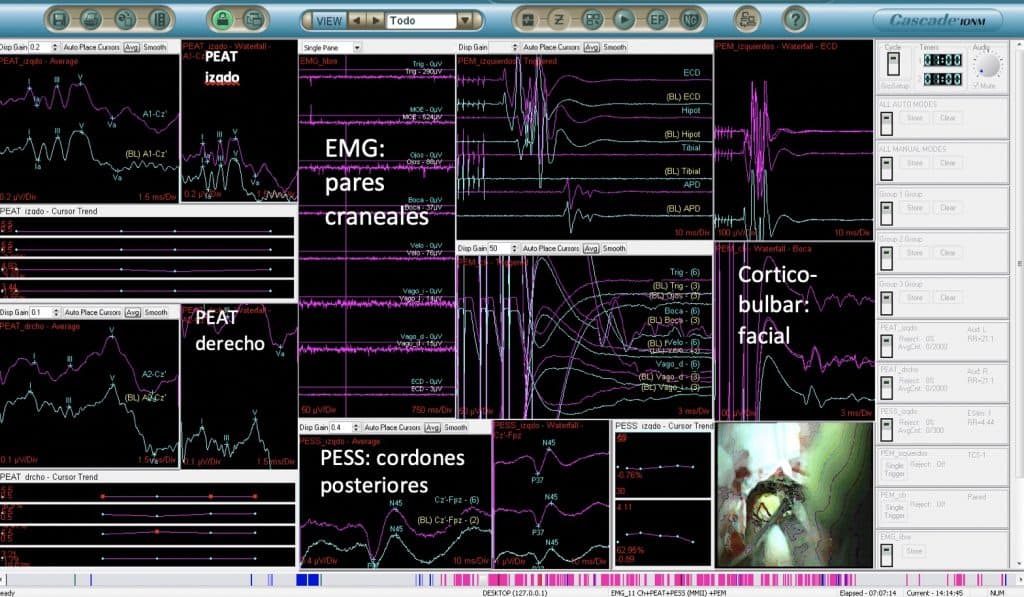
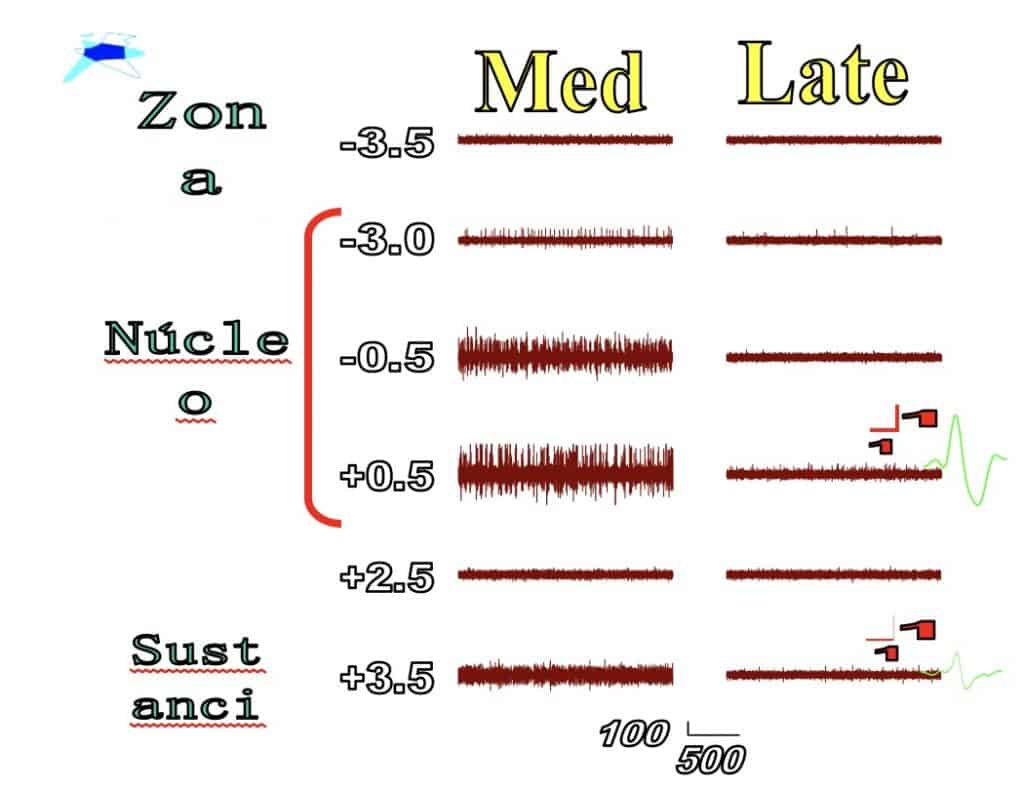
d. Registro de la actividad unitaria neuronal.- Es una técnica que permite el registro de la actividad eléctrica de una sola neurona o de un pequeño grupo de ellas. Permite distinguir grupos neuronales que forman diferentes núcleos del encéfalo. Se emplea como exploración imprescindible en los procedimientos de Estimulación Cerebral Profunda, para colocar correctamente los electrodos en los núcleos basales elegidos. Se aplica en múltiples procesos, que se verán en la lección de Neurocirugía Funcional.
f) Otras técnicas
La Neurofisiología es una de las especialidades que están teniendo mayor auge tecnológico. Entre los más recientes avances hay que destacar la Magnetoencefalografía (MEG).
La MEG consiste en el registro de las variaciones del campo magnético que se produce en el cerebro, debido a los cambios en la actividad eléctrica neuronal. En teoría, con respecto al EEG convencional, presenta varias ventajas: Tiene una capacidad tridimensional más acusada, la actividad es más real y con menor artefacto de registro y, sobre todo, puede acusar cambios mucho más sutiles.
Esto hace que la MEG, aunque en el momento actual sigue en fase de experimentación clínica, pueda tener grandes aplicaciones en Neuropsicología (para estudio de la función cortical cerebral), Psiquiatría (relación trastornos psicóticos-corteza cerebral), Neurología (estudios de memoria, demencias…) e incluso Neurocirugía (conocimiento de actividad funcional en zonas próximas a lesiones quirúrgicas, epilepsia, Enfermedad de Parkinson, …).
3.- NEURORRADIOLOGÍA.-
Es una subespecialidad, dentro de la especialidad de Radiología, dedicada al diagnóstico de las enfermedades del sistema nervioso, en el aspecto de obtención e interpretación de imágenes normales y patológicas. Así como la anterior especialidad estaba dedicada al estudio de la función, esta especialidad está dedicada al estudio de la estructura del sistema nervioso: a la Neuroimagen.
En los últimos diez años, ha tenido un auge extraordinario otra faceta de esta especialidad. Se trata de la posibilidad de conseguir objetivos terapéuticos de curación o ayuda a la curación de problemas vasculares. Se utilizan técnicas endovasculares que consiguen el cierre de malformaciones arteriovenosas o aneurismas, con menor riesgo que con el tratamiento quirúrgico convencional. En la realidad clínica, ambos especialistas, Neurorradiólogo y Neurocirujano trabajan conjuntamente cuando llega al Hospital un paciente con este tipo de patología, con el objetivo de obtener la curación con la menor agresividad posible.
Las pruebas diagnósticas útiles en Neurocirugía son las siguientes:
a) Radiología convencional.
Todavía sigue teniendo su utilidad la realización de radiografías, sobre todo tras accidentes o traumatismos, aunque también el médico puede solicitarlas ante la sospecha de determinados procesos que se ven claramente en una radiografía simple.
a. Rx de cráneo. Util en traumatismos craneoencefálicos, malformaciones congénitas…
b. Rx de columna (cervical, dorsal, lumbar). Son muy útiles para iniciar los estudios de enfermedades que afectan a la columna vertebral.
b) Tomografía axial computarizada
TAC o “scanner”. La tecnología ha evolucionado y permanece su utilidad, a pesar de la aparición de la Resonancia Magnética. Tiene un gran valor para observar el hueso, con imágenes tridimensionales, así como para apreciar la presencia de sangre intracraneal.
a. TAC de Cráneo.- Se utiliza sobre todo como exploración de urgencias, tras traumatismos craneoencefálicos o accidentes cerebro-vasculares. También en determinadas enfermedades congénitas (craneoestenosis…).
b. Angio-TAC.- Permite observar los vasos cerebrales en 3-D. Es una prueba muy útil para hacer el diagnóstico en enfermedades vasculares, sin necesidad de hacer una angiografía.
c. TAC de Columna.- Igualmente útil en urgencias, por la posibilidad de observar las fracturas en 3-D. También como preparación para una intervención quirúrgica y como control de ésta.
c) Resonancia Magnética o RM
Se ha convertido en la prueba diagnóstica de neuroimagen por excelencia. Sus posibilidades son muy grandes y aún se están abriendo nuevos campos.
a. RM Convencional.- Obtiene imágenes en los tres planos del espacio. Con diferentes técnicas permite diferenciar tejidos y estructuras con gran nitidez, dando imágenes que simulan cortes anatómicos dibujados a plumilla, con la enorme ventaja que se trata de la imagen real de un paciente. Le da al neurocirujano una imagen 3-D muy real, lo que ha cambiado de forma dramática el diseño de la intervención quirúrgica y sus resultados.
i. RM de Cráneo.- Se utiliza como exploración en prácticamente todo tipo da patología
ii. La RM de Médula.- La RM es la prueba diagnóstica por excelencia para el diagnóstico de enfermedades que afectan a la médula espinal.
iii. RM de Columna.- Combinada con la exploración con TAC, se obtiene una muy certera visión da la patología a tratar.
b. Espectroscopia.- Permite analizar la estructura bioquímica de los tejidos de los que se obtienen las imágenes de RM. De esta forma, se puede dar un diagnóstico con mayor exactitud en patologías como tumores cerebrales o epilepsias.
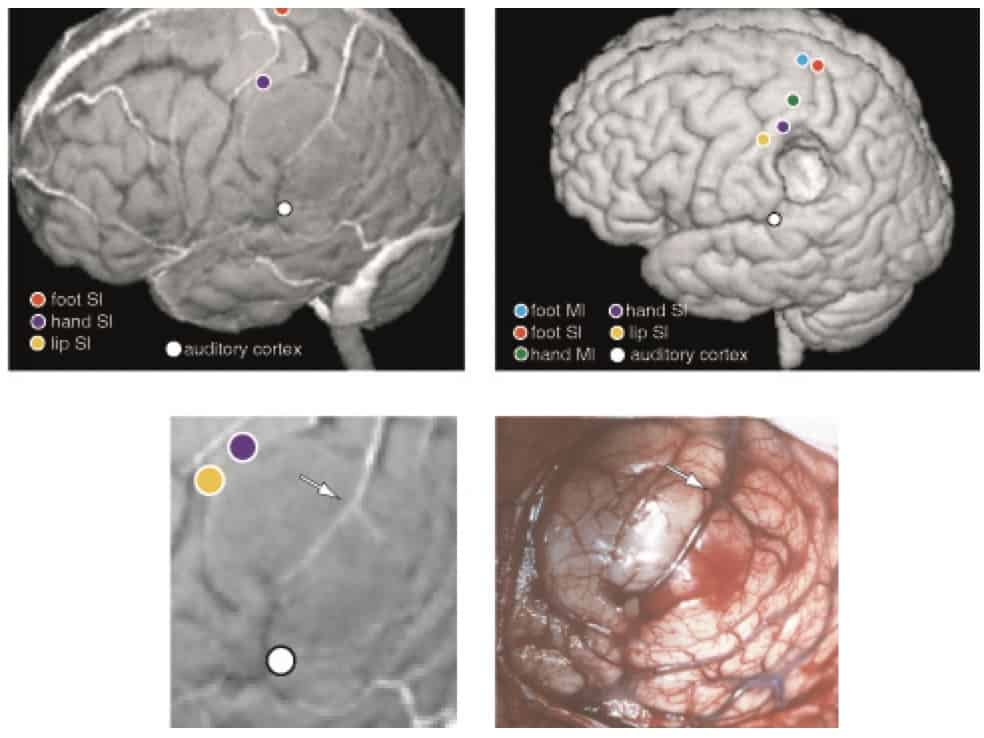
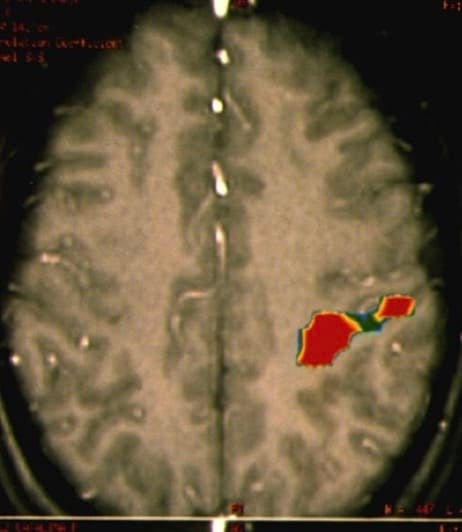
c. RM Funcional.- Las funciones que hoy día pueden ser detectadas con facilidad son: Función motora, lenguaje y visión. Ha sido la primera prueba diagnóstica que ha dado con precisión imágenes de dónde se encuentran estas zonas funcionales corticales, importantes desde el punto de vista quirúrgico, y su relación con lesiones que han de ser intervenidas quirúrgicamente. Es esencial su realización en tumores cercanos a regiones funcionalmente importantes y cirugía de la epilepsia.
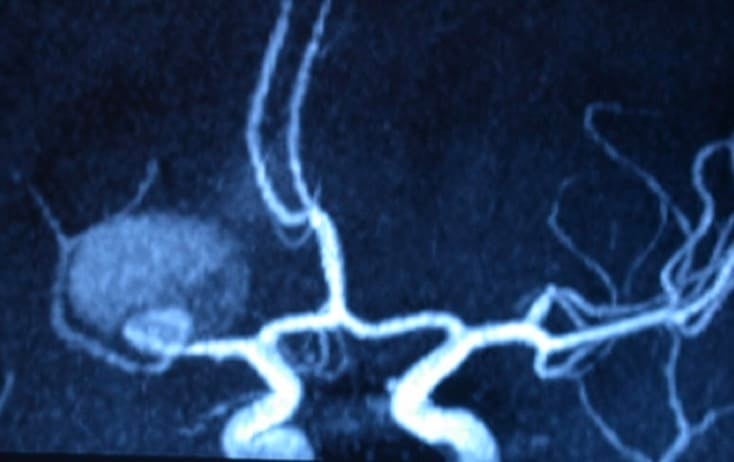
d. Angio-RM.- Es de similares características que la Angio-TAC, aunque la evolución de los nuevos softwares hacen predecir un futuro más prometedor para esta prueba.
e. Espectroscopia.- Permite, cada vez con mayor fiabilidad, hacer un posible diagnóstico anatomopatológico de la lesión. Más recientemente, la secuencia de AMIDA está también en línea con hacer un diagnóstico preciso de las lesiones tumorales y diferenciarlo de imágenes que pueden confundirse como las de radionecrosis.
f. Otras secuencias. Cada vez aparecen diferentes tipos de análisis y secuencias en la RM (FIESTA, FLAIR….) que serán explicadas en las clases de neurorradiología y que tienen gran interés quirúrgico en determinadas patologías quirúrgicas.
g. Conjunción con otras técnicas.- Aparte de estas otras técnicas, habría que hacer hincapié en la posibilidad que tiene la RM de aportar la imagen 3-D cerebral y conjugarla con otras pruebas diagnósticas. Destacamos, dentro del campo neuroquirúrgico, las siguientes:
i. MEG.- Los hallazgos neurofisiológicos y neuropsicológicos obtenidos en la MEG se pueden superponer a la imagen anatómica aportada por la RM, lo que da mucha mayor precisión a la localización funcional. Mejora, por tanto, a la RM funcional simple, dado que los estudios MEG funcionales son de mayor calidad y exactitud, aparte que con la MEG se están consiguiendo estudiar zonas corticales funcionales que no es posible con la RM funcional simple (Figura 13).
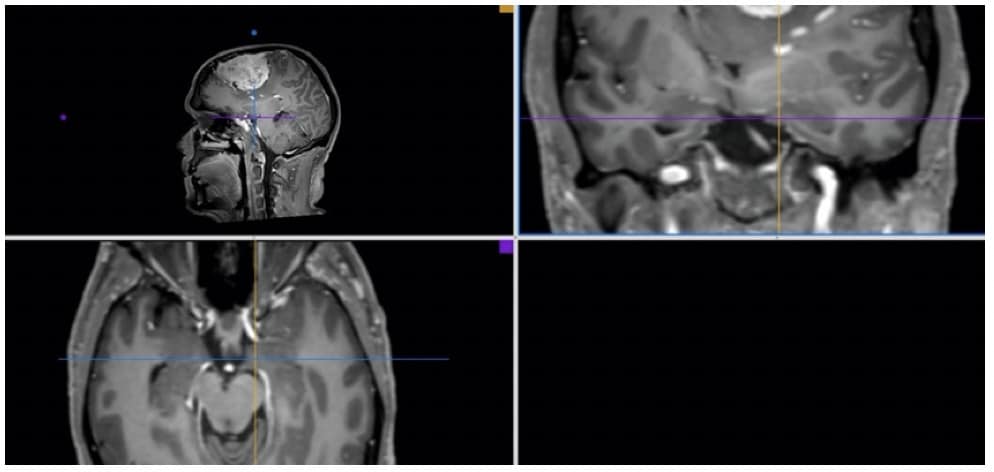
ii. Neuronavegación.- Se están generando equipamientos neuroquirúrgicos que consisten esencialmente en obtener una fusión de imágenes de TAC y RM craneal o de columna. Se consigue una imagen 3-D que, después en quirófano, se puede interconectar con la situación real del paciente y el campo quirúrgico. De manera que el equipo guía en todo momento al cirujano y le informa de los datos anatómicos y funcionales que precisa para hacer la intervención correcta. El neurocirujano, por tanto, no sólo cuenta ya con la posibilidad de un diseño prequirúrgico de la intervención, sino que tiene el soporte técnico necesario para ir guiado en todo momento por los cauces adecuados que le lleven a completar correctamente la actuación quirúrgica (Figuras 9 y 18).
d) Angiografía digital substraida (ADS)
La posibilidad de utilizar técnicas de digitalización de imagen y la aparición de catéteres especiales, han permitido obtener imágenes de la vascularización del sistema nervioso de alta calidad y sin los riesgos de años anteriores. Podemos considerar dos tipos de actuaciones
a. ADS Diagnóstica.- Obtiene imágenes 2-D o 3-D de los vasos (arterias y venas) cerebrales y medulares. Al neurocirujano le interesan estas imágenes no sólo para obtener un correcto diagnóstico (la presencia o no, por ejemplo, de un aneurisma), sino para conocer datos anatómicos que ayuden en el diseño de la intervención y durante el acto quirúrgico, dado que las arterias y, sobre todo, las venas cerebrales se ven muy bien en el campo quirúrgico
b. Terapéutica.- Ya hemos hablado de la capacidad del neurorradiólogo de “navegar” con catéteres dentro de los vasos cerebrales. Esto permite introducir en dichos vasos substancias o materiales con diseños adecuados para tratar la enfermedad vascular que se desea curar. Puede ir desde obstruir o trombosar un aneurisma cerebral a, todo lo contrario, colocar una malla (stent) que mantenga el calibre adecuado del vaso e impida su obstrucción. Es una especialidad en auge, que a velocidad de vértigo está consiguiendo mejorar materiales y técnicas, de manera que la neurocirugía está quedando relegada en multitud de procesos anteriormente quirúrgicos, dados los excelentes resultados que se obtienen y la menor agresividad que conllevan estas técnicas de neurorradiología intervencionista.
4.- MEDICINA NUCLEAR
Se basa en la capacidad existente de fabricar e introducir en el cuerpo humano un isótopo radioactivo. Dichos isótopos se diseñan para que vayan hacia el órgano que se desea estudiar. Con equipamiento especial (gammacámaras) es posible detectar la radiación emitida por dicho isótopo y obtener imágenes. Estas imágenes, aparte de poder tener una correlación con la estructura del órgano estudiado, tienen una enorme trascendencia funcional, dado que el isótopo es una sustancia que se incorpora al metabolismo.
En el momento actual hay dos tipos de exploraciones fundamentales:
a) Tomografía por emisión de positrones o PET
Da imágenes tridimensionales cerebrales y están en relación con el metabolismo de la glucosa. Son útiles para detectar zonas en que no hay una actividad neuronal normal, pudiendo ser el metabolismo bajo (como en el caso de una cicatriz epiléptica) o alto (como en el caso de un tumor agresivo). Su utilización principal, en relación con la Neurocirugía, se hace en dos campos: en la neurocirugía tumoral y en la cirugía de la epilepsia. Está teniendo también otras aplicaciones, en la cirugía de la enfermedad de Perkinson.
b) Tomografía por emisión de fotón único o SPECT
Al igual que con la anterior prueba, se pueden utilizar varios tipos de isótopos. Lo más frecuente es medir el flujo sanguíneo cerebral. Se utiliza sobre todo para el estudio de la epilepsia y últimamente de la enfermedad de Parkinson.
Estas técnicas y su aplicación serán explicadas igualmente por los especialistas en Medicina Nuclear.
5.- PSICOLOGÍA
El trabajo conjunto con los psicólogos está aportando una gran riqueza y capacidad diagnóstica y terapéutica.
La Psicología, a través de sus especialidades, entre las que destaca la Neuropsicología, está llegando a unas cotas muy altas en el conocimiento de las funciones normales y anormales cerebrales. Su aplicación es muy variada, destacando:
a) Estudio de funciones normales
El neuropsicólogo puede utilizar y diseñar tests para el estudio de las funciones normales en cualquier persona. Su aplicación, junto a técnicas como la RM y la MEG, permite ir conociendo la estructura cerebral en la que se asienta una determinada función: motora, lenguaje, memoria…
b) Estudio de alteraciones de la función cerebral
Con similar metodología, el neuropsicólogo puede llegar a cuantificar la afectación de una determinada función. La exploración neuropsicológica es muy compleja y precisa de tests para cuya ejecución se necesitan varias horas, así como para la interpretación de los resultados. De ahí que no pueda prodigarse este tipo de estudios.
Esto va a permitir diagnosticar y cuantificar con gran precisión una lesión funcional y, siguiendo el proceso a la inversa, su posible localización cerebral. Es muy útil en la cirugía de la epilepsia, dado que el hallazgo de una alteración funcional ayuda en muchas ocasiones a localizar el foco epileptógeno.
c) Control de la cirugía
Durante y tras la intervención quirúrgica, la evaluación neuropsicológica permite observar la recuperación de la función dañada u bien la aparición de nuevas alteraciones. Ya la cirugía no debe pretender no dejar secuelas neurológicas, sino ser aún menos agresiva y permitir no dejar secuelas neuropsicológicas y, si es posible, incluso recuperar funciones dañadas.
Aparte de las anteriores aplicaciones de los tests neuropsicológicos, la Psicología como rama de las Neurociencias permite estudiar a la persona desde otras facetas aún más complejas, llegando igualmente, en el momento actual, a niveles muy altos de precisión en la cuantificación de alteraciones de la personalidad como rasgos depresivos, paranoides, agresividad, inhabilidad social… Su utilidad en la Cirugía de la Epilepsia y en Psicocirugía es muy alta, dada la existencia de alteraciones concomitantes de la personalidad en un alto porcentaje de pacientes. Pero también otros procesos o enfermedades neuroquirúrgicas pueden tener una repercusión sobre la personalidad, siendo su estudio deseable desde este punto de vista.
Por último, hay que destacar la capacidad de la Psicología para diseñar tratamiento y rehabilitación de funciones cerebrales alteradas. De ahí la trascendencia de estar cada vez más unidas la Neurocirugía y la Psicología.
6.- PSIQUIATRÍA
Como rama independiente de la Medicina, la Psiquiatría ha tenido una época de excesivo aislamiento con otras especialidades. Hoy día, afortunadamente, la Psiquiatría es otro Servicio o Departamento más en un Hospital General. De esta situación se beneficia enormemente la Neurocirugía, dado que muchos procesos pueden producir alteraciones psicóticas que precisan de los métodos diagnósticos y terapéuticos psiquiátricos.
Hay que destacar también que hay un punto de unión muy estrecho, aunque aún muy en mantillas, entre la Neurocirugía y la Psiquiatría: la Psicocirugía. Está demostrado científicamente que determinados procesos psicóticos se pueden beneficiar de un tratamiento neuroquirúrgico, cuando no es posible controlarlos mediante tratamiento médico. Es una situación similar a la Cirugía de la Epilepsia. Aunque abusos posteriores a las primeras intervenciones, diseñadas en los años 40 por Edgar Moniz (por lo que le dieron el Premio Nobel) hicieron decaer este tipo de actuaciones. Hoy día están haciéndose de nuevo indicaciones quirúrgicas, con mayor precisión, dada la capacidad tecnológica de neuroimagen y de tests psicológicos que tenemos y se están introduciendo técnicas quirúrgicas menos agresivas, basadas en la neuroestimulación.
7.- NEUROENDOCRINOLOGÍA
La hipófisis es la glándula central que controla el resto del sistema endocrino. Se sitúa en la base del cráneo y es asiento de tumores benignos (adenomas) con extraordinaria frecuencia (el 10-15% de los tumores cerebrales). Este hecho hace imprescindible la colaboración con el endocrinólogo, en el proceso diagnóstico y tratamiento pre y postquirúgico de estas lesiones.
Pero además hay otros procesos tumorales (craneofaringiomas, por ejemplo) y de otra estirpe, que pueden afectar a la hipófisis o al hipotálamo, que es la región cerebral que controla la hipófisis. El diagnóstico y abordaje quirúrgico de estas lesiones han de ir coordinadas igualmente con el Servicio de Endocrinología del propio hospital.
8.- NEUROPATOLOGÍA
La Anatomía Patológica es otra de las especialidades básicas en un Hospital. La dedicación con exclusividad al estudio de las alteraciones del sistema nervioso es una subespecialidad demandada por la dificultad que presenta este campo. Por regla general, el neurocirujano está siempre en relación con neuropatólogos que realizan el estudio postquirúrgico y, en ciertos casos, estudios necrópsicos, que ayudan al diseño de un correcto tratamiento y al avance de los conocimientos médicos.
También esta materia será tratada en profundidad por los especialistas en Anatomía Patológica.
10.- NEUROCIENCIAS BÁSICAS
Existen numerosos investigadores de ciencias básicas, no sólo médicas (bioquímicos, biólogos, matemáticos…), dedicadas al estudio e investigación sobre el Sistema Nervioso. La Neurocirugía asimila también sus conocimientos, evolucionando y generando cambios continuos que mejoran los resultados quirúrgicos y amplían las posibilidades de tratamiento de otras enfermedades hasta ahora no “quirúrgicas”.
Siempre es bueno que un Servicio o Unidad de Neurocirugía colabore en alguna vía de investigación de este tipo. El contacto con personas dedicadas en exclusiva a la investigación, ayuda a mantener la Neurocirugía como una ciencia médica y a no caer en rutinas o sobrevaloraciones fuera de lugar.
TIPOS DE NEUROCIRUGIA
Si simplificáramos el Sistema Nervioso en un diagrama de bloques, habría que asimilarlo al de un ordenador personal. Al fin y al cabo, éste es un intento de copia del Sistema Nervioso.
Hay una carcasa y una estructura física (hardware), que se correspondería con las partes ya descritas y sus envolturas (cráneo y columna vertebral, así como las membranas duramadre, aracnoides y piamadre). Las neuronas funcionan de acuerdo a programas muy complejos de software, con capacidad de modificación de acuerdo con la información que reciben y la experiencia adquirida.
Se pueden considerar otras partes fundamentales como la capacidad de memoria (fundamentalmente en estructuras de la corteza cerebral) o la fuente de alimentación (que estaría en la sustancia reticular del tronco cerebral, manteniéndonos la situación de conciencia normal).
A todo lo anterior habría que añadirle unos periféricos que sirven para introducir información, asimilables al teclado, scanner, micrófonos, video, etc. Serían los órganos de los sentidos (vista, oído, olfato, gusto, tacto, dolor, sensibilidad propioceptiva [equilibrio, posición…], etc.).
Otro grupo de periféricos serviría para emitir información y serían asimilables a la impresora, pantalla, altavoz, etc. Lo constituirían los órganos efectores del lenguaje, los mecanismos productores del movimiento, etc.
Podemos diferenciar varios tipos de Neurocirugía, de acuerdo con el punto de visión que tengamos:
Función de la Neurocirugía
I.- Intentar recuperar la estructura y función de la zona afectada
Las diferentes enfermedades inciden sobre uno o varios de estos grupos de componentes y la función de la Neurocirugía va a consistir en
intentar recuperar la estructura y función de la zona afectada.
De acuerdo con esto, se pueden considerar varios tipos de neurocirugía:
1.- Reparadora
Actúa específicamente sobre estructuras o hardware afectado, por causas congénitas o traumáticas fundamentalmente. La idea es reconstituir el hardware a una situación lo más anatómica posible. Como ejemplos podríamos citar la cirugía de las craneoestenosis, de los aneurismas cerebrales o de los defectos cutáneos u óseos provocados por traumatismos craneoencefálicos.
2..- Exerética
En ocasiones se produce un acúmulo de tejidos o sustancias extrañas que precisan su retirada o extirpación. Es el caso de la cirugía tumoral o la evacuación de una hemorragia o un absceso cerebral.
3.- Funcional
Es la cirugía que más cerca incide sobre el software. Hay procesos, como la enfermedad de Parkinson, en la que las pérdidas de un determinado grupo de neuronas exacerban o frenan la actividad de otros grupos, apareciendo síntomas excitadores (temblor) o inhibidores (falta de movimientos), al romperse el equilibrio perfecto entre excitación-inhibición con el que funciona el Sistema Nervioso. La cirugía puede elegir otros núcleos funcionantes y en relación con los afectados, lesionándolos o estimulándolos, de forma que balanceen la función alterada.
II.- Tipo de patología a tratar y los instrumentos utilizados
Otra forma de dividir la Neurocirugía ha sido por el tipo de patología a tratar y los instrumentos utilizados.
Así, se diferencian fundamentalmente los siguientes grandes grupos:
1.- Microcirugía vascular
2.- Neurocirugía tumoral
3.- Neurotraumatología
4.- Neurocirugía estereotáxica y funcional
5.- Radiocirugía
6.- Neurocirugía pediátrica
7.- Neurocirugía de columna vertebral
8.- Cirugía de Base de Craneo
9.- Cirugía de la Corteza Cerebral
….
III.- Otro tipo de clasificación
Este tipo de clasificación está variando con el tiempo y no incluye todas las posibilidades, por lo que abogamos por la siguiente clasificación:
A.- Neurocirugía y patología:
1.- Neurocirugía general (traumatismos, tumores, infecciones,…)
2.- Neurocirugía super-especializada. Muy variable, según Centros:
a) Neurovascular
b) Neurooncología
c) Cirugía Base de Cráneo
d) Cirugía Corteza Cerebral
e) Neurocirugía Funcional
f) Neurocirugía de Columna
B.- Neurocirugía y edad:
1.- Neurocirugia pediátrica
2.- Neurocirugía del adulto
3.- Neurocirugía geriátrica
En los siguientes capítulos iremos entrando en los diversos aspectos de la Neurocirugía, agrupándolos por patologías o enfermedades, dado que es como se presentan en la realidad los problemas. Las soluciones neuroquirúrgicas se irán exponiendo en cada capítulo y el lector las podrá ir encuadrando en los diferentes tipos ya referidos.
PARTE II: HIPERTENSION INTRACRANEAL EDEMA CEREBRAL
En este tema se van a tratar de forma muy sucinta dos síndromes presentes en casi todas las patologías quirúrgicas que afectan al encéfalo: Hipertensión Intracraneal (HIC) y Edema Cerebral. Su correcto conocimiento permite abordar la primera fase de un tratamiento adecuado, que es común a muchas de las patologías neuroquirúrgicas.
PRESION INTRACRANEAL
Se puede definir como la presión que es necesario ejercer en una aguja colocada en los espacios subaracnoideos de forma que se evite la salida del líquido cefalorraquídeo (LCR) al exterior. Las cifras normales en decúbito supino, para un adulto, son de 10-15 mmHg.
El cerebro es el órgano más débil de la economía, por lo que está encerrado en la estructura ósea más potente, el cráneo. Para adecuar ambas estructuras, el cerebro ocupa casi todo el volumen craneal, encontrándose rodeado e inmerso en LCR, que lo protege al funcionar como un sistema hidrostático en el que “flota” (principio de Arquímedes) y que transmite presiones homogéneamente.
La presión positiva del LCR se debe a la conjunción de varios hechos. Por un lado el recipiente inelástico (el cráneo) en que se encuentra el encéfalo y el espacio relativamente distensible (espacio subaracnoideo raquídeo) por el que discurre el LCR. A esto hay que unir el sistema circulatorio (presión arterial positiva y sistema venoso de drenaje) para tener todos los elementos que influyen en la generación y mantenimiento de la presión intracraneal.
Para comprender esto, es muy útil observar el esquema de Davson (Figura 1). En él se incluye un recipiente (cráneo) lleno de líquido (LCR). Podemos medir la presión del recipiente mediante una columna de agua, en comunicación con su contenido (PIC). A este recipiente lo atraviesan 2 tubos, representativos del árbol vascular arterial y el sistema venoso de drenaje, por el que circula fluidos a su correspondiente presión (PA y PV).
En un primer supuesto, si los tubos fueran inelásticos, la presión dentro de ellos (PA y PV) no se transmitiría al recipiente.
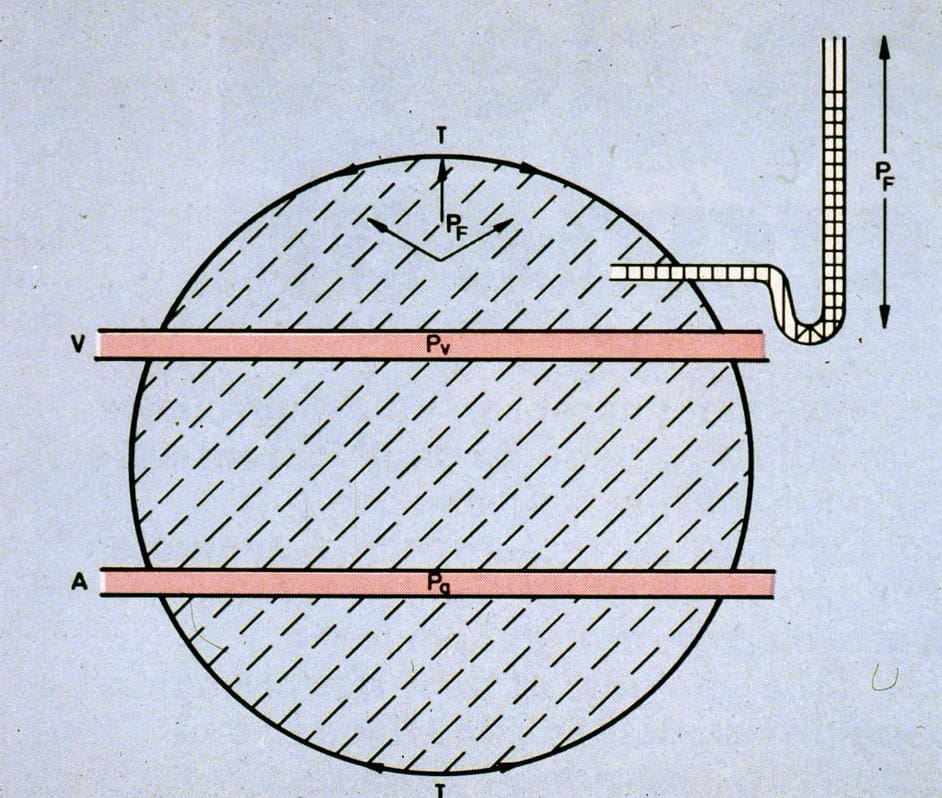
Si las paredes de uno de estos tubos fuera elástica (el representante de la circulación arterial, por ejemplo) y el recipiente fuera inelástico y estuviera herméticamente cerrado, la PA se transmitiría íntegramente al fluido del recipiente y la PIC sería igual que la PA.
En la realidad, el recipiente no está herméticamente cerrado (puede salir LCR hacia el espacio subaracnoideo espinal o puede reabsorberse en los senos venosos durales) y además el tubo representante de la circulación venosa es también elástico y puede colapsarse. El resultado final de la entrada de líquido arterial en el recipiente a una presión alta, se transforma en una presión positiva de todo el contenido, compensada por los mecanismos de amortiguación de LCR y venoso (que, por otra parte, están íntimamente ligados, al drenar el LCR en los senos venosos).
Por tanto, la PIC esta originada y mantenida por la PA. El resultado es una onda con dos componentes: cardíaco y respiratorio (figura 2). El cerebro “late” ante la entrada de sangre, que continuamente se compensa con salida de sangre venosa, salida de LCR y la elasticidad vascular. Y “respira”, coincidiendo la onda de mayor amplitud con la secuencia inspiración (se eleva) y espiración (desciende). Aunque en un paciente con respiración asistida estas tendencias se invierten, ascendiendo con la inspiración (el respirador genera una presión positiva que eleva la presión venosa central y, por consiguiente, impide el drenaje venoso intracraneal) y descendiendo con la espiración (al caer dicha presión inspiratoria)
TEORIA DE MONRO-KELLIE
Lo importante es mantener el equilibrio entre el continente intracraneal y los contenidos (parénquima cerebral [Vc ], volumen sanguíneo [Vs] y cantidad de LCR [Vlcr], de forma que se cumpla lo referido en la teoría de Monro-Kellie:
Vc + Vs + Vlcr = K
Si, por alguna circunstancia, apareciera un nuevo volumen extra [Ve], los otros componentes han de disminuir el suyo, de forma que:
Vc + Vs + Vlcr + Ve = K
Para esto hay unos mecanismos de compensación. Unos de acción rápida: reabsorción de LCR, salida de sangre venosa y vasoconstricción arteriolar. Otros precisan más tiempo, como la disminución del agua del espacio extracelular del parénquima cerebral.
En la clínica, las circunstancias que pueden hacer descompensar esta situación de equilibrio se pueden resumir en:
Factores de descompensación [Ve]:
– Del Vlcr: Hidrocefalia
– Del Vs: Hemorragia
– Del Vc: Tumores, Edema, Infeccciones.
CURVA PRESION-VOLUMEN
A medida que se incrementa el [Ve] los mecanismos de compensación dejan de ser efectivos, produciéndose entonces un incremento de la presión (PIC) en relación exponencial al incremento de volumen (figura 3).
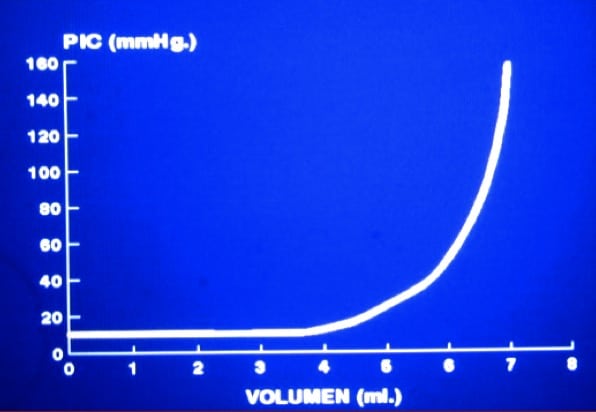
En el cerebro, por tanto, la relación Incremento de Presión/Incremento de Volumen es exponencial. En este contexto, se dice que existe una situación de alta elastancia (E), cuando el sistema craneoencefálico se encuentra en un límite en que pequeños incrementos de volumen van a generar un incremento peligroso de la PIC.
E = ΔP/ΔV
La situación de baja elastancia o alta complianza (C) es lo contrario, indicando que el sistema está muy distendido o relajado, permitiendo aumentos de volumen sin modificar la presión.
C = ΔV/ΔP
AUTORREGULACION CEREBRAL
El cerebro tiene unos potentes mecanismos para mantener el flujo sanguíneo (FSC) constante (no provocar anoxia y/o disminución del metabolismo), dado que no tolera más de 5 min. de isquemia.
Como cualquier flujo, en el cerebro el FSC está relacionado con su presión de perfusión (PPC) y la resistencia vascular (RVC).
FSC = PPC/RVC
La presión de perfusión es la diferencia entre la presión de entrada al sistema (Presión arterial) y la presión de salida (Presión venosa):
PPC = PA – PV
Pero, de hecho, la presión venosa en los senos durales es prácticamente igual que la presión intracraneal. Por lo que quedaría:
FSC = PA-PIC/RVC = K.
De acuerdo con esto, si la PIC aumenta se produce una vasodilatación cerebral (disminuye la resistencia vascular cerebral) para mantener el FSC constante.
Si el aumento de la PIC continúa, ha de aumentar la presión arterial para compensar el sistema. Este fenómeno es el denominado efecto Cushing, que ya observó la aparición de hipertensión arterial en pacientes con hipertensión intracraneal.
Pero si la PIC continúa aumentando, se puede llegar a producir un colapso vascular y descenso del FSC, por fracaso del sistema. Lo que conduce a una situación grave de isquemia y muerte cerebral.
CLINICA DE LA HIPERTENSION INTRACRANEAL (HIC)
Se pueden diferenciar tres conjuntos de síntomas y signos:
1.- Triada de inicio: cefalea, vómitos y edema de papila.
2.- Hay disminución progresiva del nivel de conciencia por:
• Disminución de la presión de perfusión cerebral y disminución del flujo sanguíneo cerebral.
• Lesión de la sustancia reticular del tronco cerebral
3.- Fenómenos de enclavamiento. Se producen al intentar salir masa encefálica a alta PIC por el agujero del tentorio o del agujero magno) (figura 4). Esto produce:
– Afectación del III par (midriasis unilateral al hemisferio cerebral dañado)
– Hemiparesia (por lo general contralateral al hemisferio cerebral dañado)
– Alteraciones respiratorias y hemodinámicas. Una de ellas ya referidas: Efecto CUSHING, consistente en bradicardia e hipertensión arterial.
DIAGNOSTICO
1.- Clínico
A.- Aparecen signos de afectación general, caracterizados por la disminución progresiva del nivel de conciencia. Es muy importante destacar que esta disminución ocurre siempre siguiendo los siguientes niveles, de mejor a peor:
– Conciencia normal
– Bradipsiquia (lentitud intelectual y de ejecución)
– Desorientación témporo-espacial
– Estupor. El paciente tiene tendencia a quedar dormido. Ante estímulos externos despierta y conecta con el ambiente.
o La agitación puede alternarse en esta fase. El paciente entra en situación de hiperactividad elemental intelectual y psíquica, sin responder al entorno.
– Coma. El paciente está inmóvil. Sólo responde ante estímulos externos. El más adecuado en la exploración es el dolor. Ante esto, el paciente responde de forma estereotipada y dependiendo de la gravedad:
o Coma con respuesta localizadora de estímulos
o Coma con respuesta en flexión
o Coma con respuesta en extensión
– Muerte cerebral
B.- Focal : Los síntomas y signos dependientes de la localización del proceso expansivo generador de HIC: III par, hemiparesia.
2.- Radiológico
RX de cráneo:
En situaciones de HIC crónica, se pueden ver las impresiones digitiformes de las circunvoluciones cerebrales sobre la tabla interna y erosión de las apófisis clinoides. En los niños es fácil apreciar la separación o diástasis de suturas aún no cerradas.
TAC y RM:
Visualizan los procesos expansivos ocasionantes de la HIC, así como la existencia de desviaciones de línea media (Figura 5) y los fenómenos de enclavamiento del parénquima cerebral a nivel de agujero del tentorio (Figura 4) o de las amígdalas cerebelosas en el agujero magno (Figura 6).
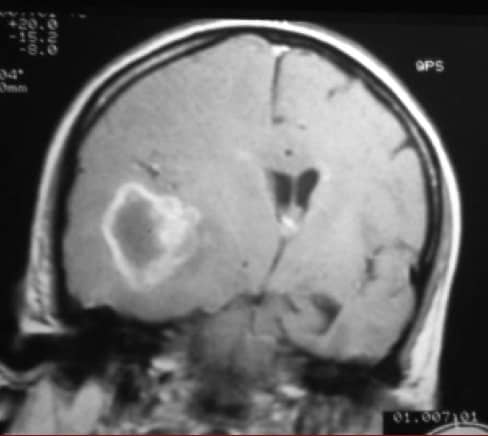
TRATAMIENTO
1.- En primer lugar, hay que atender al fenómeno desencadenante de la HIC:
– Hidrocefalia: Drenaje de LCR
– Hematomas: Evacuación
– Tumores: Extirpación
– …
2.- Edema Cerebral
Pero en la mayoría de las ocasiones, además del volumen del proceso expansivo, se produce un aumento sobreañadido de volumen por un fenómeno complejo que acompaña a casi todas las lesiones del SNC: Edema Cerebral.
Clásicamente, se distinguen dos grandes grupos o formas de edema cerebral. Puede ser:
– Citotóxico: Por lesión directa a glía y neuronas. La causa más frecuente es hipoxia. El edema es intracelular.
– Vasogénico: Se produce tras la afectación de la barrera hematoencefálica y se caracteriza por un incremento del líquido extracelular, por aumento de la permeabilidad del endotelio de los capilares cerebrales. El edema suele ser focal y contribuye a aumentar los desplazamientos y herniaciones o enclavamientos cerebrales. Acompaña a la mayoría de los procesos tumorales, hemorragias e infecciones. Es, por tanto, el más frecuente en la clínica neuroquirúrgica.
HIC y edema cerebral están muy interrelacionados, ya que todo edema cerebral produce HIC y la mayoría de procesos generadores de HIC (excepto la Hidrocefalia) tienen un componente de edema cerebral.
Por tanto, el tratamiento del edema cerebral va a favorecer la reducción de la Hipertensión Intracraneal. Con estos criterios, las medidas a nuestro alcance para tratar la HIC se pueden diferenciar en:
i.- Corregir la alteración de la barrera hematoencefálica:
– Corticoides, en especial la Dexametasona
ii.- Facilitar el drenaje venoso:
– Colocar al paciente incorporado
– Manejo adecuado del respirador.
iii.- Disminuir el volumen intracraneal:
– Sanguíneo circulante: Hiperventilación (produce vasoconstricción por aumento de la pO2 y consiguiente disminución del volumen cerebral circulante)
– Extracelular: hiperosmóticos (manitol), diuréticos…
– Drenaje de LCR, mediante catéter intraventricular.
iv.- Proteger el metabolismo neuronal:
– Barbitúricos
– Antagonistas del calcio
– Fenitoina
– …..
Todas estas medidas han de ser utilizadas dependiendo del proceso, su velocidad de crecimiento, la situación aguda o crónica del paciente, etc.
En casos graves, los pacientes son controlados en Unidades de Cuidados Intensivos o de Reanimación Anestésica, con control continuo de la situación de HIC (monitorización de la PIC) y con control permanente del nivel de conciencia (Escala de Glasgow).
PARTE III: HIDROCEFALIAS Y OTRAS ALTERACIONES DE LA CIRCULACIÓN DEL LIQUIDO CEFALORRAQUIDEO
INTRODUCCIÓN
Esta parte se va a dividir en 3 grandes apartados. En primer lugar se repasarán las nociones más importantes sobre la fisiología del LCR., en estrecha conexión con lo referido anteriormente
En segundo lugar se estudiarán las hidrocefalias.
Por último, se recogerán algunos otros cuadros clínicos en relación con alteraciones de la circulación del LCR.
FISIOLOGÍA DEL LCR
I.- FORMACIÓN
La mayor parte del LCR se produce a nivel de los plexos coroides, dentro de los ventrículos cerebrales.
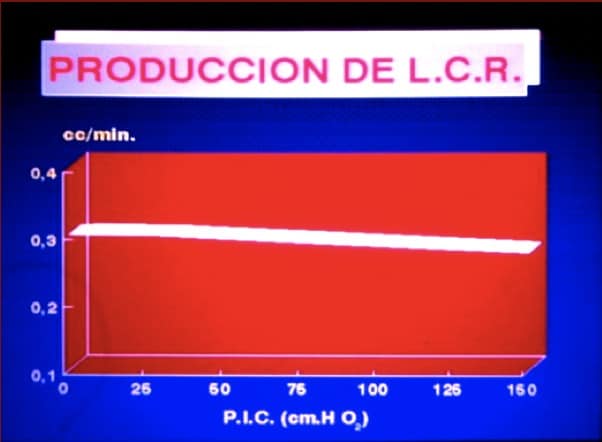
Esta producción es un proceso activo, que precisa energía. La cantidad aproximada es de 0’30 cc/min. (aproximadamente unos 500 cc/día). Dado que hay un total de 140 cc., el LCR se renueva cada 6-8 horas.
Es muy importante destacar que la producción no es presión dependiente (Figura 1). Esto explica que una persona pueda morir por hipertensión intracraneal (HIC) provocada por una hidrocefalia.

El LCR se puede producir en otros lugares, dado que está en continuidad anatómica con el espacio extracelular. Esto explica el fracaso de intervenciones propuestas para solucionar las hidrocefalias, consistentes en la extirpación de los plexos coroides.
II.- CIRCULACIÓN
El LCR discurre a través de los ventrículos y sus comunicaciones (agujeros de Monro y acueducto de Sylvio), para finalmente salir del IV ventrículo a través de los agujeros de Luschka y Magendie hacia la cisterna magna. A partir de aquí el LCR va a las diferentes cisternas de la base, sube por los espacios subaracnoideos y llega hasta la convexidad craneal.
Esta circulación se ve favorecida por el empuje del nuevo LCR formado, la expansión y expresión ventricular provocada por la onda pulsátil cerebral, los gradientes de presión, los efectos posturales y los cilios del epitelio ependimario (estos dos últimos, menos importantes).
III.- REABSORCIÓN
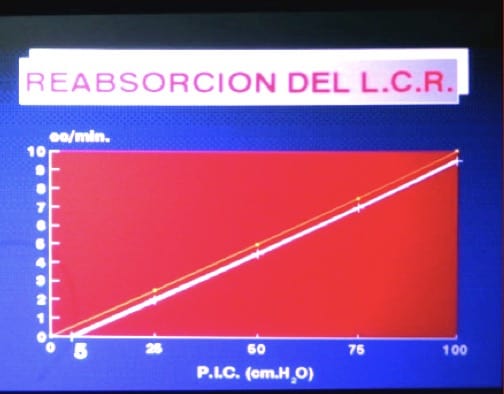
La mayor parte se produce a nivel de los senos venosos durales, en las vellosidades aracnoideas. El mecanismo es unidireccional (jamás entra sangre desde el seno hacia el espacio subaracnoideo) y se produce siempre que haya un gradiente de presión entre espacio subaracnoideo y venoso de muy pocos cm. de H2O.
La reabsorción es, por tanto, presión-dependiente. Es uno de los mecanismos de compensación rápida ante un aumento brusco de presión intracraneal.
IV.- FUNCION
Hay que considerar al LCR como una estructura unida metabólicamente al espacio extracelular cerebral. Sus funciones son principalmente:
A.- Limpieza
B.- Regulación del entorno extracelular.
C.- Transferencia endocrina (endorfinas…)
D.- Mecánica:
– Protección y flotabilidad: 1.500 gr. de cerebro suspendido en LCR tienen una masa virtual de sólo 50 gr.
– Reduce el momento y aceleración del cerebro.
– Mantenimiento y homogeneización de la presión hidrostática en la que se encuentra el cerebro (PIC).
HIDROCEFALIA
CONCEPTO
Aumento del LCR dentro del cráneo (Brain, 1962). Este concepto amplio incluiría la hidrocefalia ex vacuo (por atrofia cerebral primaria).
Es más acertada la de Milhorat: Trastorno o desajuste entre la formación y reabsorción de LCR, de suficiente magnitud como para producir una neta acumulación de fluido dentro de las cavidades ventriculares. Supone un concepto dinámico activo y excluye la hidrocefalia ex vacuo.
PATOGENIA
Si seguimos las bases fisiológicas, se podrían considerar tres tipos de hidrocefalias:
1.- Por exceso de secreción de LCR: Hipersecretoras.
2.- Por obstrucción de las vías de circulación del LCR: Obstructivas.
3.- Por trastornos en la reabsorción del LCR: Arreabsortivas.
Las hidrocefalias hipersecretoras son más teóricas que reales. Sólo se podrían admitir en el caso de la existencia de un papiloma de plexos coroides. Y aún así la hidrocefalia producida se debe más a la obstrucción ventricular por la masa tumoral que a la hipersecreción de dicho tumor.
Por tanto, en la práctica, como refería Dorothy Russell en 1949, la hidrocefalia se debe a una obstrucción patológica en algún punto de las vías de circulación del LCR.
Dandy apreció que, a los pacientes con hidrocefalias a los que colocaba un colorante (test de la fenosulfoftaleina) a nivel ventricular, los podía dividir en dos grupos:
A. Aquellos en los que se apreciaba el colorante en el LCR obtenido mediante punción lumbar: Hidrocefalias Comunicantes.
B. Aquellos en los que no se recogía colorante a nivel lumbar: Hidrocefalias No Comunicantes.
Otro hecho importante a tener en cuenta es que, dependiendo de la calidad de la obstrucción en la salida y reabsorción del LCR, así como de los mecanismos compensatorios, las hidrocefalias se pueden manifestar con una PIC alta, media o incluso baja.
CLASIFICACION
Hay, como ya hemos visto, una gran profusión terminológica en las hidrocefalias, por lo que se produce a veces confusión y falta de interrelación entre los diferentes términos.
En un intento de aclarar esta situación, se expone a continuación las diferentes clasificaciones y su correlación entre ellas:
A.- Patogénica
A1.- Obstructivas:
A1a.- Univentriculares (obstrucción en uno de los agujeros de Monro)
A1b.- Biventriculares (obstrucción de los dos agujeros de Monro)
A1c.- Triventriculares (obstrucción en el acueducto de Sylvio)
A1d.- Tetraventriculares (obstrucción de agujeros de Luschka y Magendie)
B2.- No obstructivas:
B2a.- Arreabsortivas
B2b.- Hipersecretoras (¿)
B2c.- Ex vacuo (¿)
B.- Dandy
B1.- No comunicantes
B2.- Comunicantes
C.- Etiológica
C1.- Congénitas
C2.- Adquiridas
D.- Edad de presentación
D1.- Hidrocefalia en el niño
D2.- Hidrocefalia del adulto
E.- Dinámica del LCR
E1.- Hidrocefalia de presión alta
E2.- Hidrocefalia de presión media
E3.- Hidrocefalia de presión baja
Si nos fijamos, las hidrocefalias en el niño son, con mayor frecuencia, congénitas. Éstas, a su vez, suelen ser obstructivas y, por tanto, no comunicantes, cursando con presión alta. Existiendo una cierta correlación entre A1-B1-C1-D1-E1.
Por el contrario, en el adulto las hidrocefalias suelen ser adquiridas, no obstructivas en un gran porcentaje y, por tanto, comunicantes, de presión media o baja, como después veremos; existiendo una cierta correlación entre A2-B2-C2-D2-E2.
Aunque también se dan hidrocefalias obstructivas, no comunicantes, de presión alta.
CLINICA Y DIAGNOSTICO
De acuerdo con la edad de presentación, los cuadros clínicos y proceso diagnóstico pueden variar:
A.- HIDROCEFALIA EN EL NIÑO
A su vez, podemos apreciar varias etapas:
I.- En el Recién nacido (entre 0-2 años)
Epidemiología
Hay que destacar varios hechos:
– A los 3 meses de edad, 1-2 de cada 1000 nacimientos van a presentar hidrocefalia.
– Es mayor la frecuencia de causas congénitas que adquiridas (3:1)
– Cursan sólo con hidrocefalia aproximadamente un 1‰ de nacimientos
– En el 0’5-1‰ de nacimientos la hidrocefalia se asocia con espina bífida.
Etiología
En los casos de hidrocefalia congénita influyen factores teratógenos, como malnutrición, toxinas, toxoplasmosis… Son raras las hidrocefalias con carácter hereditario.
Las hidrocefalias adquiridas son más raras, ocasionadas por infecciones, hemorragias, traumatismos o tumores.
Patología
A.- Los tipos de hidrocefalia congénita son:
1.- Estenosis del Acueducto de Silvio. Suponen el 70% de las hidrocefalias. Se producen como consecuencia de gliosis o formas anómalas (“forking”) a nivel del acueducto. Es el tipo de hidrocefalia que se asocia con la espina bífida abierta.
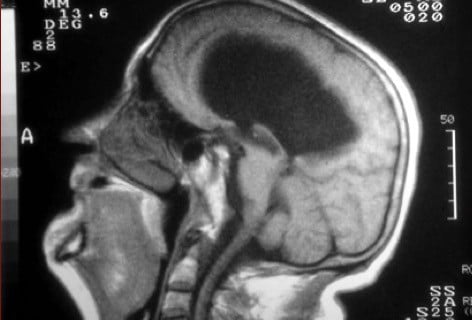
2.- Chiari tipo 2.- Se asocia la hidrocefalia con malformación de Chiari y espina bífida.
3.- Chiari tipo1.- En ocasiones se asocia la malformación de Chiari con hidrocefalia e incluso siringomielia.
3.- Malformación o Quiste de Dandy-Walker. Se debe a una atresia congénita de los agujeros de Luschka y Magendie.
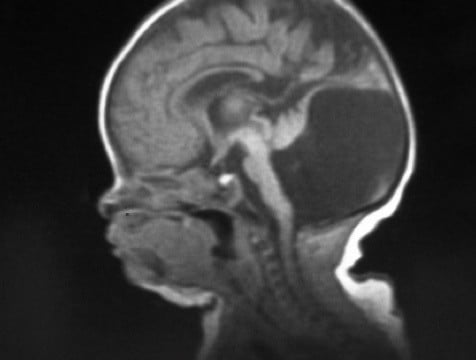
4.- Ocasionada por tumores congénitos, quistes aracnoideos o malformaciones vasculares (malformación de la vena de Galeno).
B.- Las hidrocefalias adquiridas en el recién nacido se deben fundamentalmente a infecciones (meningitis, ventriculitis) o hemorragias. Son, por tanto, hidrocefalias comunicantes. También, aunque más raras, las hidrocefalias pueden deberse a tumores u otros procesos obstructivos.
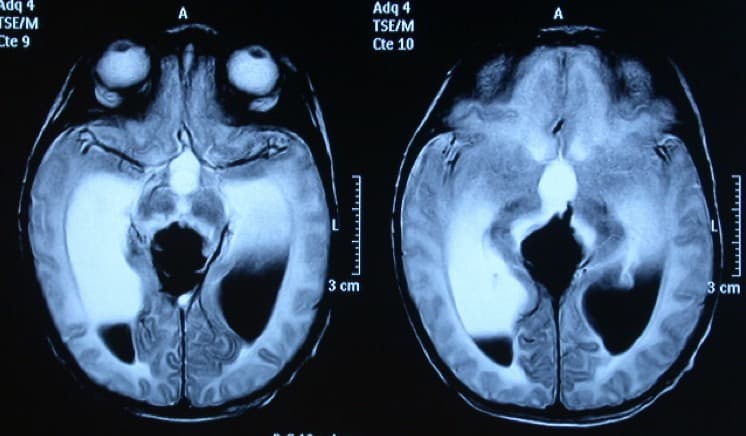
Fisiopatología
Hay que tener en cuenta varios hechos:
1. El cerebro inmaduro no ha completado su mielinización, por lo que aumenta su distensibilidad.
2. El cráneo también es distensible, por lo que aumenta su tamaño, sin aumentar mucho la PIC. Esto permite una situación progresiva de aumento del tamaño de la cabeza sin provocar una situación de hipertensión intracraneal que conduzca a la muerte.
Esto trae como consecuencia:
A. Atrofia de la sustancia blanca no mielinizada.
B. Edema periventricular y posible alteración en la formación y emigración neuronal desde la zona ventricular hacia la corteza cerebral.
Todo lo anterior puede traer consecuencias graves de déficit intelectual y neurológico, así como epilepsia.
Clínica
El aumento de la PIC se va a traducir en aumento del tamaño de la cabeza, con aumento de la fontanela, que además está tensa, diástasis de suturas y aumento de las venas a nivel del cuero cabelludo.
También se afectan los núcleos oculomotores mesencefálicos, con paresias en la abducción de la mirada y, lo más típico, con ojos en puesta de sol o en sol naciente (los niños están mirando hacia abajo, las pupilas están parcialmente ocultas por el párpado inferior y no pueden llevar la mirada hacia arriba), equivalente al signo de Parinaud.
Los niños están irritables.
Si la hidrocefalia es muy marcada, la percusión del cráneo suena a olla cascada (signo de Macewen) y la transiluminación del cráneo es positiva (en niños menores de 9 meses.
La configuración de la cabeza y la morfología de las diástasis de suturas puede sugerir el tipo de hidrocefalia. Así, la fosa posterior pequeña sugiere una estenosis de acueducto, frente al quiste de Dandy-Walker en que aumenta excesivamente su tamaño, o la cabeza más homogénea de las hidrocefalias comunicantes. Esto se observa mejor en las exploraciones radiológicas.
Diagnóstico
Se realiza basándose en la clínica, Rx de cráneo, exploración con ecografía transfontanelar, TAC y/o RM.
II.- En el niño (2-10 años)
Se pueden distinguir varios tipos clínicos
1.- Niños que tenían ya una hidrocefalia no diagnosticada
Suelen ser niños con desarrollo intelectual normal o bajo, con tamaño de la cabeza en los límites altos.
Este tipo de hidrocefalias se denomina “parada” o “compensada”. Las causas serían similares a las del recién nacido, siendo lo más frecuente la estenosis de acueducto y las hidrocefalias post-infecciosa o post-hemorrágica. El cuadro se descompensa ante un traumatismo craneoencefálico, infección o de forma espontánea.
Al hacer las pruebas diagnósticas podemos encontrar en la Rx signos de HIC y en la TAC o RM una hidrocefalia muy importante.
Ante la duda de si está compensada o no, lo mejor es hacer estudios de PIC con monitorización prolongada de ésta. En caso de que se detecten niveles de PIC altos, estaría indicado el tratamiento.
2.- Niños que desarrollan hidrocefalia cuando las suturas están cerradas
Aparecen, como en el adulto, los síntomas y signos de hipertensión intracraneal: cefaleas, vómitos, edema de papila y disminución del nivel de conciencia. A los que habría que añadir los síntomas y signos focales de las causas (tumores, meningitis, hemorragias…u obstrucción de una derivación de LCR previa).
El diagnóstico se realiza fundamentalmente con TAC y RM.
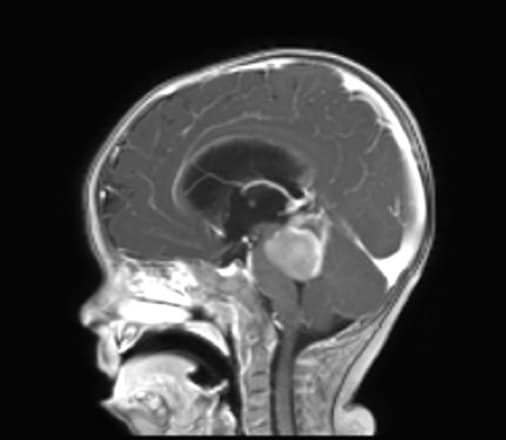
B.- HIDROCEFALIA EN EL ADULTO
I.- Hidrocefalia obstructiva
La etiología congénita es menos probable a medida que avanza la edad. Por el contrario, la adquirida es más frecuente, ocasionada por tumores y hemorragias fundamentalmente.
La clínica es de hipertensión intracraneal, sobreañadida a la provocada por el factor causal.
El diagnóstico se realiza mediante TAC y/o RM
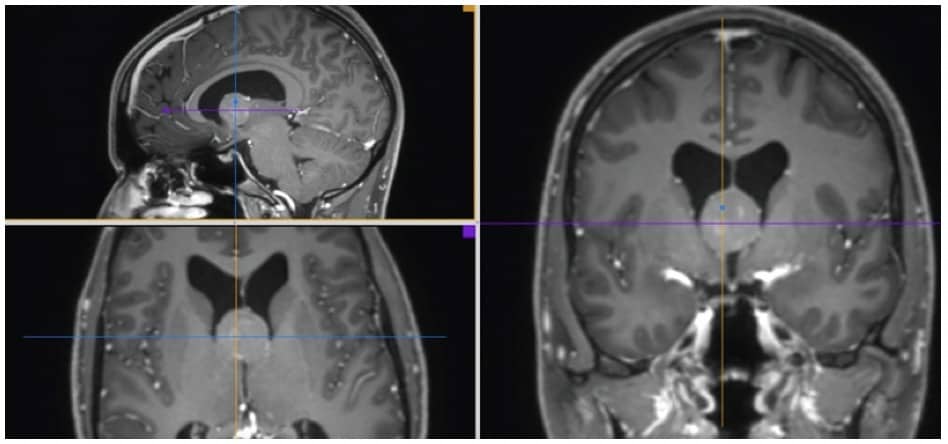
II.- Hidrocefalia comunicante
Sinonimia
En el adulto este tipo de hidrocefalia es más frecuente que en el niño y muy característica. Fue descrita por Hakim y Adams en los años 60 y le dieron el nombre de hidrocefalia de presión normal del adulto. También se puede llamar hidrocefalia arreabsortiva o comunicante. Esto puede generar confusión al referirse todos los términos al mismo proceso.
Nosotros preferimos denominarla hidrocefalia comunicante arreabsortiva (HICA), respetando la tradición de los conceptos de Dandy y dando el nombre al fenómeno fisiopatológico que la provoca. A partir de aquí, el resto de los términos no son totalmente correctos, ya que también se pueden dar en niños y cursar con presiones medias normales, bajas o altas.
Etiopatogenia
Se debe a una obstrucción de los lugares de reabsorción de LCR en los espacios subaracnoideos, a causa de una infección meníngea, hemorragia subaracnoidea, hematoma subdural bilateral o por causas desconocidas.
Los acontecimientos fisiopatológicos no son totalmente conocidos, aunque podríamos resumirlos en los siguientes estadíos:
1º.- Se provoca, en primer lugar, una dificultad en la reabsorción del LCR de pequeña intensidad, aumentando la PIC y el tamaño ventricular.
2º.- Se genera a continuación un aumento de la tensión a nivel de la pared ventricular e incremento de la reabsorción transependimaria del LCR.
3º.- Si estos fenómenos “compensan” la hidrocefalia, se detiene aparentemente el proceso y baja la PIC. Pero ya se ha producido una lesión de la estructura paraventricular.
4º.- Como persiste la dificultad de reabsorción de LCR, pueden mantenerse los ventrículos amplios a pesar de que baje la PIC, con incremento de la tensión a nivel de la pared ventricular ya dañada. Esto se explica por la ley de Laplace que refiere una relación directamente proporcional de la tensión de la pared de un recipiente con la presión dentro de él y el radio. Por lo que el problema se perpetúa y aumenta lentamente el tamaño ventricular con el tiempo, sin necesidad de que aumente la PIC.
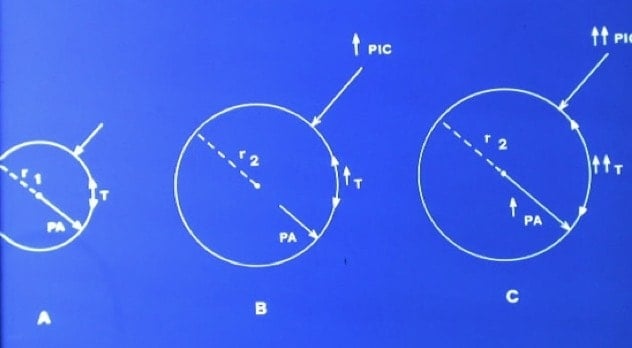
Clínica
La presentación del cuadro clínico es insidiosa, de lenta evolución y fluctuante.
En primer lugar aparece un trastorno de la marcha, similar al parkinsoniano. A continuación un deterioro intelectual progresivo, hasta llegar a la demencia. Por último, aparecen alteraciones de esfínteres, con incontinencia urinaria.
En alto porcentaje de casos vamos a poder evidenciar un antecedente infeccioso, hemorrágico o traumático. Aunque cada vez se detectan más casos de etiología desconocida.
Diagnóstico
Es importante diferenciar este cuadro con otros que producen la misma triada clínica (trastorno de la marcha, demencia e incontinencia de esfínteres). Es fácil diferenciarlo del hematoma subdural crónico o los tumores frontales, tanto en la TAC como con la RM.
Pero, en ocasiones, no es tan fácil diferenciarlas de las demencias seniles y preseniles que cursan con hidrocefalia ex vacuo (HIEV). Y es muy importante, ya que las HIEVs no tienen solución; pero en las HICAs sí se puede obtener reversión de los síntomas tras una correcta derivación del LCR.
Los datos que nos van a ayudar a diferenciar HICA de HIEV son los siguientes:
1.- Antecedentes clínicos de etiología clara de HICA: Meningitis, hemorragia subaracnoidea, hematoma subdural.
2.- Clínica fluctuante de alteraciones de la marcha y deterioro intelectual. El paciente y familiares relatan que hay días en que se encuentra muy bien y otros en los que decae.
3.- TAC y RM:
a.- Aumento del tamaño ventricular sin signos de atrofia cerebral (surcos cerebrales no marcados).
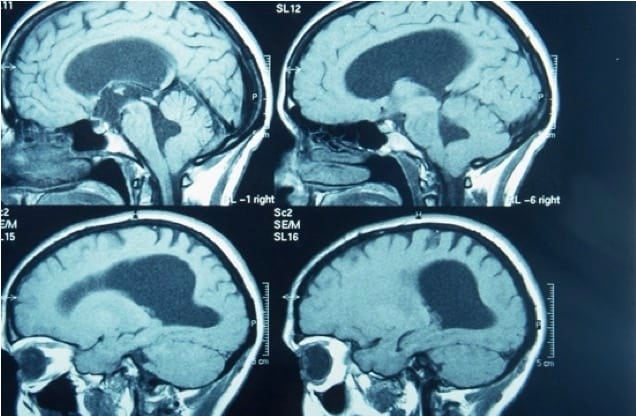
b.- Hipodensidad o hipointensidad periependimaria, sugerente de edema o trasudado de LCR.
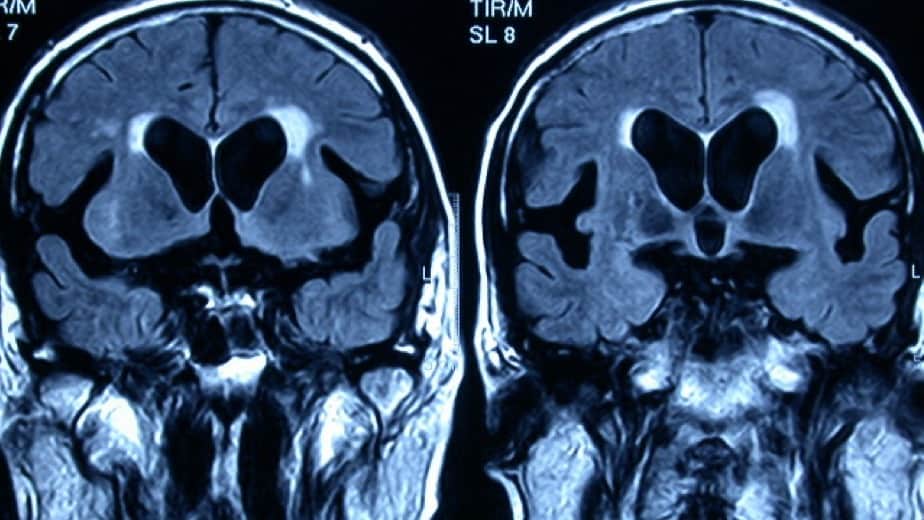
c.- En la RM se puede apreciar aumento de flujo a nivel del acueducto de Silvio
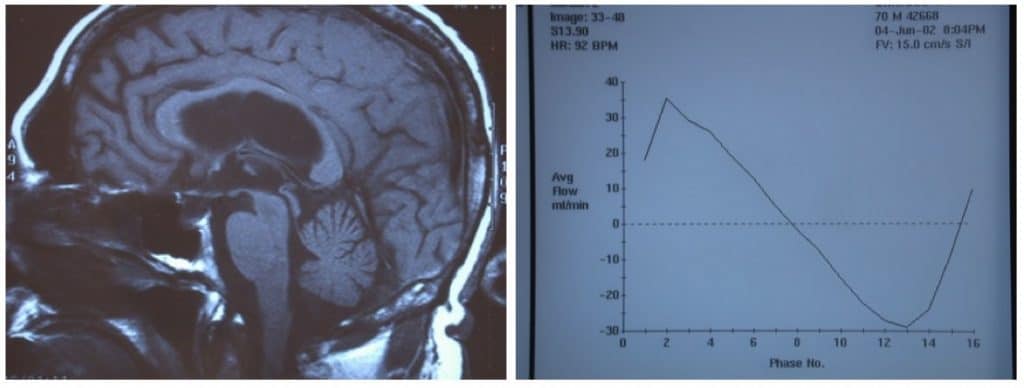
4.- Estudio de la dinámica de LCR: Test de Infusión.
Hay múltiples tests, aunque todos ellos tienen la misma finalidad: infundir líquido (suero salino o LCR artificial) a nivel lumbar y estudiar las variaciones de presión que se producen.
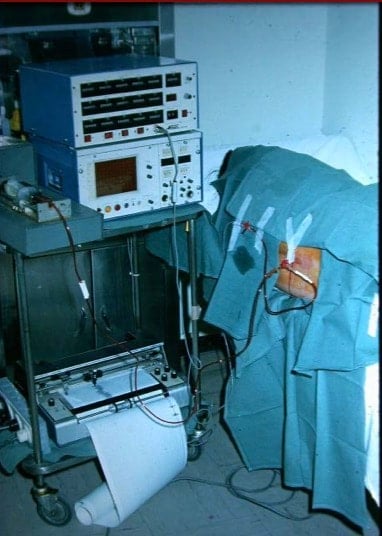
Como regla general, las HICAs van a presentar aumentos anómalos de PIC ante la infusión de LCR, mientras que en las HIEVs la respuesta va a ser normal o fisiológica dado que no hay afectación en la reabsorción de LCR (que en condiciones normales puede llegar a ser 10 veces superior a la cantidad de LCR que se produce).
5.- Monitorización de la PIC.- En ocasiones es muy útil observar los cambios espontáneos de la PIC a lo largo de un mínimo de 24 horas. Pueden detectarse aumentos patológicos de la PIC, sobre todo durante el sueño, que indiquen la presencia de una HICA.
6.- Cisternografía isotópica.- Consiste en inyectar en el espacio subaracnoideo (lumbar o en cisterna magna) un isótopo radiactivo (Tecnecio [99mTc-DTPA]) y observar a lo largo de 48 horas su recorrido intracraneal. Hoy día está en desuso esta técnica.
Pronóstico
Si el paciente tiene sólo alteraciones de la marcha, los resultados tras la derivación ventrículo-peritoneal son prácticamente del 100% en cuanto a reversión de síntomas.
Si ya ha aparecido deterioro intelectual, los buenos resultados se obtienen en el 80-90% de los casos.
Si la triada clínica está completa, los resultados son menores. Posiblemente porque ya hay un componente de atrofia cerebral y daño neuronal cerebral asociados.
Los riesgos de la intervención quirúrgica y de menor posibilidad de reversión de los síntomas aumentan con la edad. Por lo que, a partir de los 75 años, hay que valorar cuidadosamente el paciente, su clínica y las pruebas diagnósticas para indicar correctamente el tratamiento quirúrgico.
TRATAMIENTO DE LAS HIDROCEFALIAS
El tratamiento es prácticamente igual para todas las hidrocefalias y en todas las edades: derivar el LCR desde la cavidad ventricular al exterior. No obstante, conviene hacer una sistematización de todos los posibles tratamientos.
Dandy propuso la extirpación de los plexos coroides en 1918, pero nunca dio resultado a pesar de varios intentos posteriores con mejorías técnicas. Como hemos referido, el único tratamiento es realizar una derivación o “shunt” de LCR. Pero éstas pueden ser:
1.- Derivaciones intracraneales:
Diseñadas para salvar el obstáculo, siendo su indicación principal la estenosis de acueducto u obstrucciones a nivel del IV ventrículo. Pero hay que estar seguros de que la reabsorción de LCR no está también afectada. Se han propuesto muchos tipos:
a.- Ventriculostomía, a nivel de la lámina terminalis del III ventrículo. Se puede hacer por vía subfrontal o con técnicas estereotáxicas-endoscópicas.
b.- Ventrículocisternostomía (Torkildsen). Consistía en colocar un catéter que unía ventrículo lateral y cisterna magna. Daba malos resultados a largo plazo.
c.- Se ha llegado a proponer una derivación ventrículo-seno transverso. En teoría es muy similar a las vías naturales de salida de LCR del cráneo. Queda adquirir experiencia para aceptarlas clínicamente.
d.- Colocar un catéter en el acueducto de Sylvio, con técnicas endoscópicas, para unir III y IV ventrículos
Pero hoy día solamente se suele realizar la Ventriculostomía del III ventrículo, con técnicas endoscópicas, abriendo el ventrículo a la cisterna perimesencefálica.
2.- Derivaciones extracraneales:
Se han intentado prácticamente a todas las cavidades del organismo, pero hoy día las más utilizadas son:
a.- Ventrículo-peritoneal. Sobre todo en niños, ya que permite introducir una importante longitud de catéter distal en la cavidad peritoneal, que va saliendo a medida que el niño crece, sin necesidad de recambios durante muchos años. Es en la práctica la que se utiliza hoy día en casi el 100% de los casos.
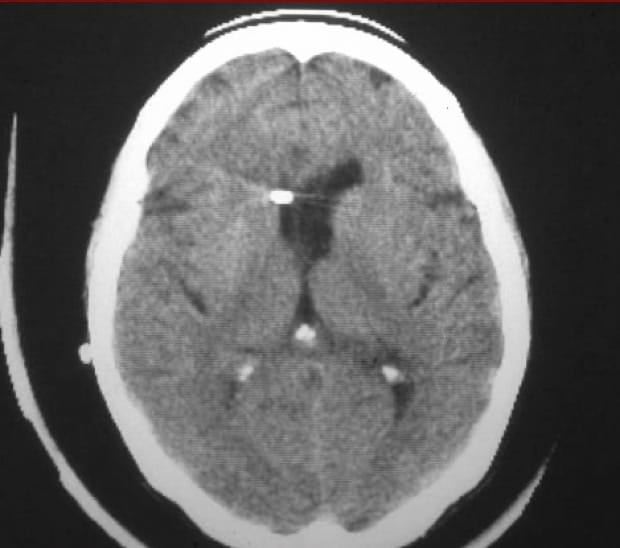
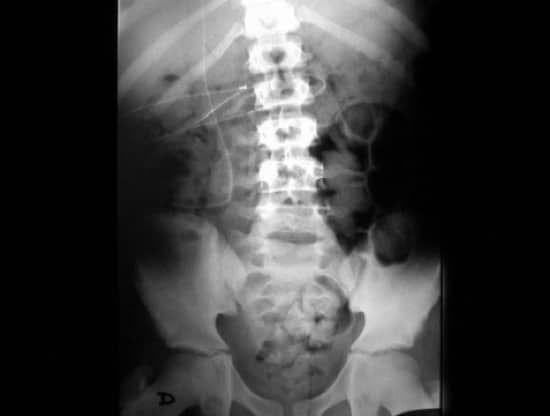
b.- Ventrículo-atrial. A través de la vena yugular se lleva la punta del catéter distal a la aurícula derecha. Se reserva a los casos en que no sea posible la anterior opción.
c.- Lumbo-peritoneal. En casos seleccionados de hidrocefalia comunicante.
Las complicaciones de los sistemas de derivación de LCR son relativamente frecuentes y se deben fundamentalmente a obstrucciones de los catéteres o de los sistemas valvulares, infecciones, aparición de hematomas o higromas subdurales por exceso de drenaje de LCR, o por complicaciones del catéter distal (perforación de vísceras, quistes peritoneales, endocarditis…).
No obstante, en los últimos años hemos asistido a una mejora en los materiales y diseños de estos sistemas, denominados genéricamente VÁLVULAS de LCR, puesto que intentan adaptarse a la presión de la hidrocefalia que se pretende tratar y mantener el espacio intracraneal en las mejores condiciones fisiológicas posibles. Esto ha hecho que la implantación de estos dispositivos sea cada vez más segura, presente menores complicaciones y su funcionamiento sea muy prolongado, durante años sin precisar revisiones o reposiciones quirúrgicas.
OTRAS ALTERACIONES EN LA CIRCULACIÓN DEL LCR
En este grupo de patologías se podrían incluir, además de las que se exponen a continuación, otras ya referidas en las clases de malformaciones, entre las que destacan el Chiari I y II así como la siringomielia, muy relacionadas con alteraciones de la circulación del LCR durante el periodo fetal, de acuerdo con la teoría hidrodinámica de Gardner (ver temas de malformaciones craneoencefálicas y raquimedulares).
HIDRANENCEFALIA
Es un defecto congénito en el que no hay desarrollo cerebral y se mantiene el cráneo intacto. La cavidad está llena de LCR y puede crecer el cráneo. La causa parece ser infarto de ambos territorios carotídeos o infecciones en la fase post-neurulación
Son malformaciones que suceden en el tercer trimestre de vida fetal. Los hemisferios cerebrales están sustituidos por sacos membranosos llenos de LCR, aunque los lóbulos temporal y occipital, ganglios basales y resto de encéfalo pueden estar conservados, aunque son anormales.
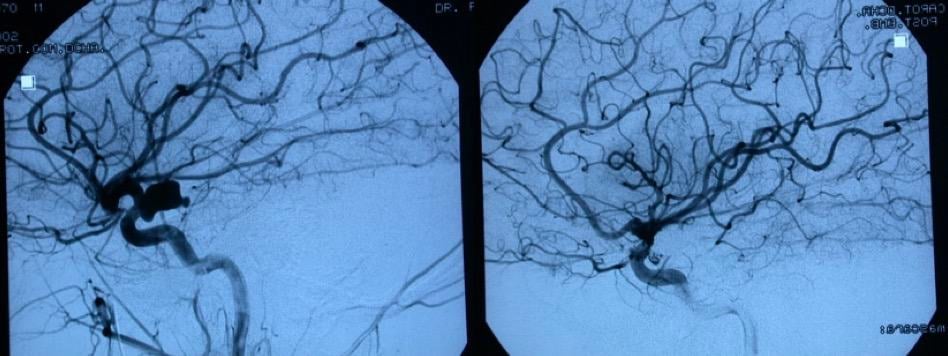
La diferencia con una hidrocefalia verdadera es trascendental, puesto que estos casos no son indicación de derivación de LCR, excepto que haya crecimiento de la cabeza, puesta que no va a conseguirse recuperación del manto cortical. Las pruebas más importantes son el EEG (ausencia de actividad cortical), la RM y la angiografía (no flujo en ambas carótidas, con circulación normal en territorio vértebro-basilar).
HIDROCEFALIA EXTERNA
Se caracteriza por un aumento del espacio subaracnoideo, sobre todo a nivel frontal, con tamaño ventricular normal.
Aparece este cuadro durante el primer año de vida y produce aumento del diámetro cefálico. Suele remitir espontáneamente.
La etiología es desconocida y se asume que puede ser una forma de alteración en la reabsorción del LCR.
Hay que establecer un correcto diagnóstico diferencial con los higromas subdurales bilaterales. Para esto se intenta en la RM apreciar la existencia del signo de las venas corticales: en la hidrocefalia externa se pueden ver venas que atraviesan el espacio subaracnoideo desde la corteza a la duramadre, mientras que en los higromas subdurales el espacio subaracnoideo está colapsado y no es posible verlas (Figura 17).
Sólo en el caso de que se produzca un aumento excesivo de la cabeza estaría indicado el tratamiento con derivación de LCR.
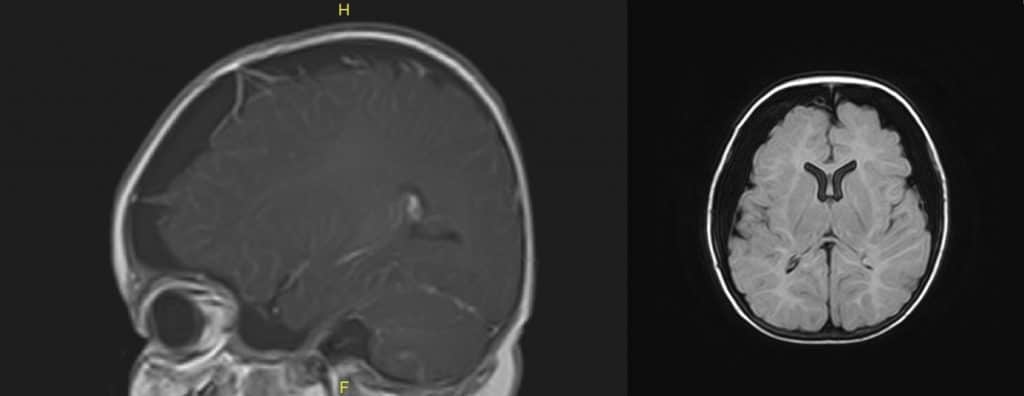
HIPERTENSIÓN INTRACRANEAL BENIGNA
También denominado pseudotumor cerebral, es un cuadro clínico raro en el que se aprecia hipertensión intracraneal (cefalea con edema de papila y ausencia de masa intracraneal) y ventrículos cerebrales de pequeño tamaño.
Su importancia reside en que puede llegar a producir pérdida de visión.
Su etiopatogenia no está clara. Una de las causas parece ser la trombosis de senos durales.
En otros casos se debe a efectos secundarios de fármacos o intoxicaciones con determinadas drogas (corticoides, tetraciclinas, litio, anticonceptivos…)
Es más frecuente en mujeres y se asocia con obesidad. La edad de presentación es entre los 5-15 años y alrededor de los 30.
En un 10% de los casos se pueden producir pérdidas de visión. Aunque en la mayoría de los casos el cuadro clínico se soluciona espontáneamente.
El diagnóstico se realiza tras efectuar TAC o RM, comprobar el tamaño ventricular pequeño y la ausencia de procesos expansivos. La angiografía permite descartar o poner de manifiesto trombosis de senos durales. A continuación se evidencia la HIC mediante una punción lumbar y medida de presión de LCR (superior a 20mmHg.).
El tratamiento puede ser complejo. En casos de riesgo de pérdida de visión, se administran diuréticos (acetazolamida, para disminuir la producción de LCR) o incluso corticoides. Si no responde, se plantea la posibilidad de derivación lumbo-peritoneal o descompresión del nervio óptico.
FORMACIONES QUÍSTICAS
QUISTE ARACNOIDEO
También se denominan quistes leptomeníngeos. Se producen durante el desarrollo cerebral y a consecuencia de un desdoblamiento de la aracnoides, que atrapa LCR.
Aparecen en la superficie del encéfalo y su pared es la aracnoides que se desdobla en 2 capas, formando una cavidad con contenido líquido incoloro semejante al LCR. Son muy frecuentes, con localización predominante en la cisura de Silvio, supraselar y en fosa posterior. Pueden alcanzar grandes tamaños.
La mayoría de las veces son asintomáticos. En otras ocasiones se manifiestan por crisis epilépticas focales, siendo muy difícil discernir si el quiste es activo o la colección de LCR es pasiva, resultante de un déficit de desarrollo focal cerebral.
Es menos frecuente que lleguen a adquirir un gran tamaño, produciendo cuadros de hipertensión intracraneal o clínica aguda hemorrágica (por rotura de venas puente corticales-durales).
El diagnóstico se realiza mediante TAC y/o la RM. Aunque en ocasiones es difícil diferenciarlos de otros tipos de quistes muy raros (quistes ependimarios o quistes neuroentéricos).
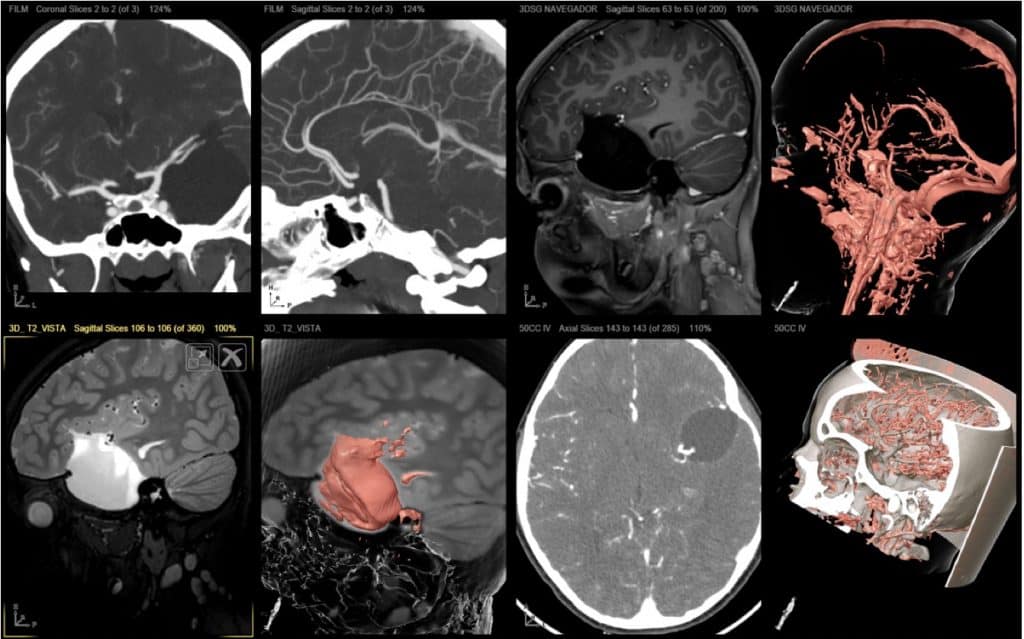
El tratamiento es quirúrgico, si son sintomáticos. Hay dos alternativas principales:
1.- Derivación cisto-peritoneal, con buenos resultados aunque con riegos de malfuncionamiento e infección y con dependencia del sistema de por vida.
2.- Desbridamiento quirúrgico de las membranas (microcirugía o endoscopia), con riesgos propios de intervención mayor y recidiva del quiste. La elección de una u otra dependerá del tipo de quiste, edad del paciente y experiencia del equipo quirúrgico.
QUISTE PORENCEFÁLICO
Son espacios quísticos, llenos de LCR, en el parénquima cerebral y que pueden comunicar o no con los ventrículos.
Se deben primariamente a una lesión cerebral, con pérdida de sustancia, que se rellena de LCR.
No precisan, por tanto, tratamiento quirúrgico.
FISTULAS DE LCR
La salida de LCR fuera del espacio intracraneal puede deberse a varias causas:
1.- Espontánea. Es rara, siendo el lugar más frecuente a nivel de silla turca (síndrome de silla turca vacía o por tumor invasivo hipofisario), a nivel de peñasco o a nivel de lámina cribosa.
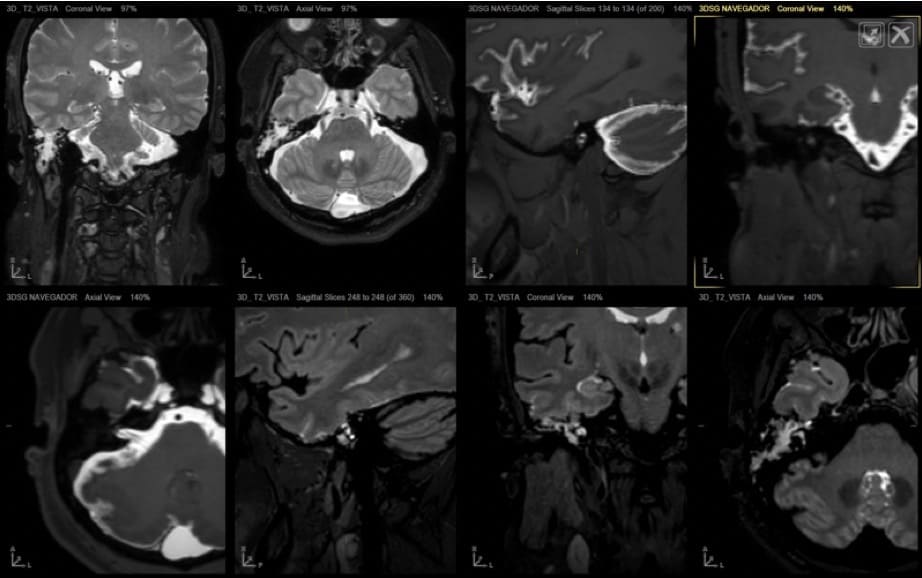
2.- Adquirida. Bien postraumática o postquirúrgica.
Se suelen manifestar mediante rinorrea u otorrea. Su importancia se basa en el riesgo de producción de meningitis.
El proceso diagnóstico es en ocasiones difícil. El tratamiento es siempre quirúrgico, mediante craneotomía, acceso al lugar de rotura de duramadre y hueso, con reposición y cierre de dichas estructuras. En ocasiones hay que ayudarse de la colocación de una derivación lumbo-peritoneal permanente.
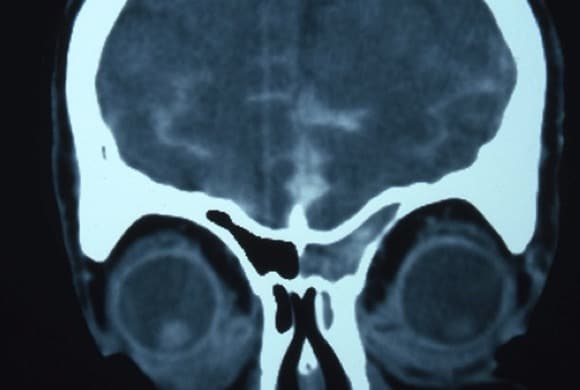
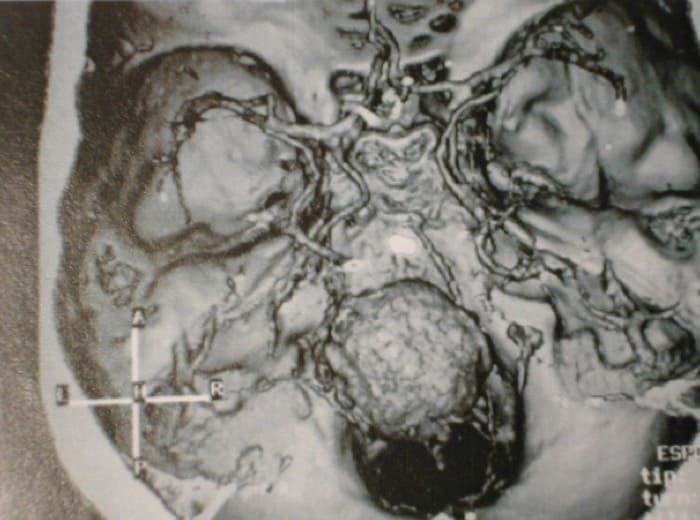
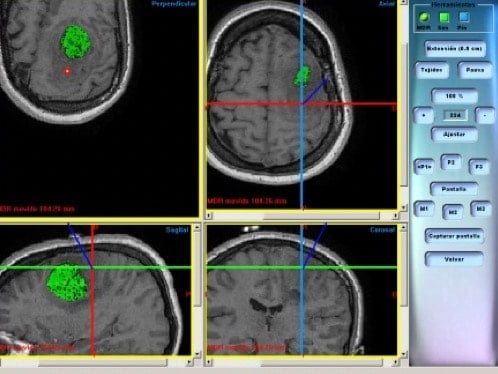
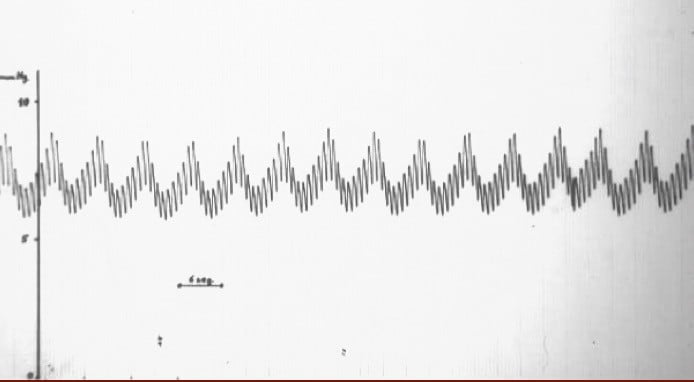
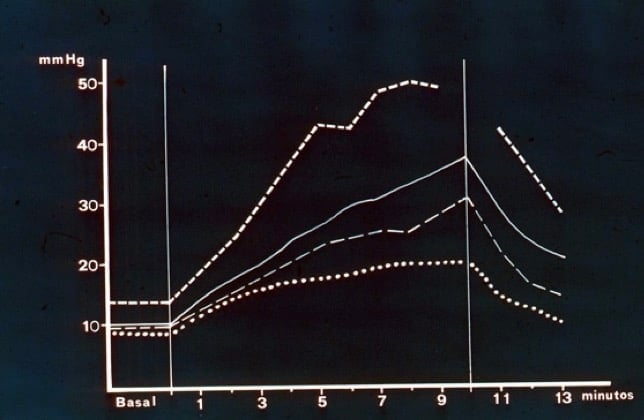



Excelente revision muy completa y didactica. Toca la mayoria de punyos importantes para no decir todos.
Los felicito un tema muy dificil lo han hecho de facil entendimiento
Hola buenas noches, mí nombre es Héctor Escobar soy enfermero coordinador de una UCI en Tucumán Argentina me gustaría recibir información sobre todo tipos de innovación de la neurológia clínica y cirugía