Neurocirugía funcional.Trastornos del movimiento
Tema 10. Parte III – Trastornos del movimiento
Dr. Rafael García de Sola
Otros trabajos del Dr. Rafael garcía de Sola
INTRODUCCIÓN A LOS TRASTORNOS DEL MOVIMIENTO
La Enfermedad de Parkinson (EP) es el trastorno extrapiramidal más frecuente. Fue descrita por vez primera por James Parkinson en Inglaterra en 1817. Su incidencia es de 1-2 casos/1000 habitantes, afectando aproximadamente al 1% de la población mayor de 50 años, siendo más frecuente entre los hombres que entre las mujeres. El origen de esta enfermedad parece encontrarse en causas genéticas y ambientales (tóxicos, insecticidas o disminución de la ingesta de vitaminas con efecto antioxidantes).
FISIOPATOLOGÍA
Los ganglios basales (GB) son el conjunto de núcleos profundos subcorticales cerebrales que forman parte de un circuito de realimentación entre diferentes partes del córtex cerebral. Intervienen en la generación y control de la actividad motora, formando parte del sistema extrapiramidal, aunque también participan en funciones cognitivas y comportamentales.
El mal funcionamiento de este sistema extrapiramidal explica la mayor parte de la sintomatología de la enfermedad de Parkinson y otros trastorno extrapiramidales del movimiento.
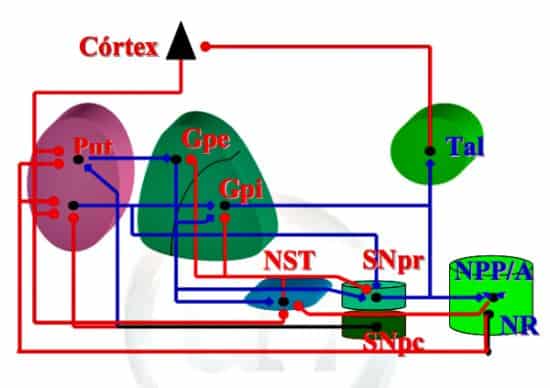
La causa primaria de la EP es la depleción del neurotransmisor dopamina (DA) en el estriado debido a la pérdida de las células en la pars compacta de la sustancia negra. Como resultado, se produce un aumento de la función celular inhibitoria en los núcleos que forman la salida de los GB, que son el globo pálido interno (Gpi) y la sustancia negra, en su parte reticulada (SNpc). Este incremento de la salida inhibitoria va a dar lugar a un “bloqueo funcional” de los núcleos motores del tronco del encéfalo y de determinados subnúcleos talámicos que, a su vez, proyectan sobre la corteza cerebral.
La consideración del presente modelo como base fisiopatológica de la EP ha llevado al desarrollo de terapias racionales y eficaces. Desde el punto de vista médico, la depleción de DA se sustituye por medio de la aplicación de L-dopa y otros agentes dopaminérgicos.Y desde el punto de vista quirúrgico, la hiperactividad se corrige bloqueando la salida de los GB.
TIPOS DE MOVIMIENTOS ANORMALES
En primer lugar daremos un repaso a las principales formas clínicas de alteraciones del movimiento por afectación del sistema extrapiramidal. A continuación veremos la clasificación de las principales enfermedades con trastornos del movimiento de tipo extrapiramidal y más en relación con el tratamiento neuroquirúrgico
En cuanto a los principales síntomas extrapiramidales, hay que destacar:
1.- Bradicinesia:
Es la lentitud de ejecución de movimientos de las extremidades y del cuerpo en general. A nivel de la mímica de la cara, la persona queda sin capacidad de expresión (amimia). La afectación motora del lenguaje da lugar a un habla monótona. Si esta lentitud afecta a la marcha, se hace a pequeños pasos y con episodios de bloqueo o congelación cuando desean pasar el umbral de una puerta, por ejemplo.
2.- Temblor:
Es la oscilación rítmica de una parte del cuerpo. Puede clasificarse de numerosas formas:
A) De reposo:
Se manifiesta cuando la zona temblorosa del cuerpo está sin actividad motora voluntaria y se desactiva al iniciar actividad voluntaria. Es el tipo de temblor que se presenta en la Enfermedad de Parkinson.
B) Postural y de acción (terminal):
Se manifiesta, al contrario del anterior, cuando se ejecutan movimientos voluntarios y se mantienen las posturas. Es como la exageración del temblor fisiológico o normal que todos hemos sentido con el estrés o el cansancio. Se da en determinadas situaciones endocrinológicas como la hipoglucemia o el exceso de hormona tiroidea, así como por exceso de drogas como la cafeína, alcohol y multitud de medicamentos. Entre las enfermedades extrapiramidales donde se pueden observar, destacan el Temblor Esencial, algunos casos de Distonía y Enfermedad de Parkinson, así como en afectaciones cerebelosas.
C) Intencional:
Aparece cuando se comienza a mover una parte del cuerpo hacia un objeto, o al retirarla. Es característico de afectación cerebelosa por esclerosis múltiple, traumatismos, tumores, drogas, etc.
3.- Alteración de la marcha:
Sobre todo en la enfermedad de Parkinson se produce un trastorno de la marcha y de los reflejos posturales. Esto se traduce en una marcha a pequeños pasos, con el tronco flexionado y sin braceo. Hay tendencia a correr como buscando el centro de gravedad (marcha festinante). Tienen dificultad para dar la vuelta de forma rápida y pueden tener fenómenos de bloqueo al pasar el umbral de una puerta, al subir o bajar escaleras, etc.
4.- Corea:
Son movimientos complejos, irregulares e impredecibles que progresan de forma continua por diferentes partes del cuerpo. Pueden ser muy breves y bruscos o bien lentos y como reptantes. En este último caso se denomina coreoatetosis.
5.- Balismo:
Son movimientos muy bruscos, que afectan la parte proximal de una extremidad, lanzándola con gran fuerza. Suele afectar a las extremidades de un solo lado del cuerpo (hemibalismo).
6.- Distonía:
Son contracciones musculares mantenidas que acaban produciendo un retorcimiento y posturas anormales de forma repetitiva. Suelen disminuir si el sujeto se relaja y permite mover la parte del cuerpo distónica hacia donde suele dirigirse. Por el contrario, aumenta cuando se intenta resistir el movimiento involuntario. Estro hace que en muchas ocasiones el sujeto intente adoptar posturas y trucos con los que se manifiesta la distonía de forma menos acusada, pero que le hace parecer y ser diagnosticado erróneamente de histeria.
7.- Tics:
Son, por lo general, movimientos bruscos, estereotipados, coordinados, que varían en intensidad y se repiten a intervalos irregulares o en situaciones especiales del sujeto. Éste siente la necesidad de realizarlos, puede suprimirlos voluntariamente, pero al precio de una tensión creciente hasta que los vuelve a realizar.
Los tics pueden ser fisiológicos (manierismos) o patológicos, presentes en numerosas enfermedades ye intoxicaciones por drogas o medicamentos.
8.- Mioclonias:
Es un movimiento muy rápido, repentino y breve de contracción muscular (mioclonia activa) o de relajación (mioclonia pasiva). Las mioclonias se pueden presentar en sujetos normales (hipo o sacudidas durante el sueño) o ser inducidas por el estrés o el ejercicio. Pero son expresivas de muchas enfermedades del sistema nervioso central, entre las que destacan algunas formas de epilepsia.
9.- Estereotipias:
Es un movimiento involuntario, dentro de un patrón determinado, repetitivo, continuo, sin propósito determinado, como ritualístico, de una parte del cuerpo, postural o de la expresión del lenguaje. Puede ser simple, como el hacer movimientos repetitivos de sacar la lengua, o más complejos como cruzar y descruzar las piernas continuamente. Puede darse en sujetos normales (manierismos) o en enfermedades neurológicas y psiquiátricas.
10.- Discinesias:
Son movimientos complejos, que se sitúan en una mezcla entre los descritos en los párrafos 6 al 9, que aparecen fundamentalmente como efectos secundarios de drogas como la L-Dopa administrada en la enfermedad de Parkinson.
CLASIFICACION DE LOS TRASTORNOS DEL MOVIMIENTO
La colaboración entre la Organización Mundial de la Salud y la Movement Disorder Society han completado recientemente la clasificación de los trastornos del movimiento dentro de la International Classification of Diseases, Tenth Revisión: Neurological Adaptation (ICD-10 NA), de los que destacamos, por sus posibilidades o relación con el tratamiento neuroquirúrgico, las siguientes:
- Enfermedad de Parkinson Idiopática
- – Clásico
- – Acinético
- – Tembloroso
- – Dificultad de la marcha/Inestabilidad postural
- – Hemiparkinson
- Parkinsonismo secundario:
- – Farmacológico, tóxico, postencefalítico…
- Parkinsonismo en otras enfermedades:
- – Alzheimer, tumores, accidentes cerebrovasculares…
- Distonia
- – Discinesias inducidas por fármacos
- – Distonías idiopáticas no familiares
- – Tortícolis espasmódica
- Otras trastornos extrapiramidales del movimiento:
- – Temblor esencial
- – Corea inducida por fármacos
- – Síndrome de piernas dolorosas y dedos en movimiento
- – Hemibalismo
- Trastornos extrapiramidales del movimiento en enfermedades:
- – Esclerosis múltiple
- – Traumatismos craneoencefálicos
- – Accidentes cerebrovasculares
- – …
ENFERMEDAD DE PARKINSON
Es la enfermedad extrapiramidal más frecuente y en la que, a lo largo de la historia se han ido aplicando numerosos tipos de tratamiento quirúrgico, dado el porcentaje de pacientes a los que la medicación no consigue controlar del todo sus síntomas incapacitantes.
Su apariencia es muy típica y ya fue descrita por James Parkinson como “Parálisis agitante”
La causa inmediata de la enfermedad, como ya hemos referido, es la afectación de uno de los núcleos del sistema extrapiramidal (sustancia negra), que provoca la falta de un neurotransmisor (Dopamina) en otros núcleos. Esto acaba produciendo un aumento de la función celular inhibitoria de una parte de los núcleos extrapiramidales y liberación de otros núcleos activadores de la corteza cerebral.
MANIFESTACIONES CLINICAS
En la enfermedad de Parkinson van apareciendo de forma lentamente progresiva un conjunto de 4 síntomas característicos: temblor de reposo, lentitud en los movimientos (bradicinesia), rigidez plástica y alteración de la marcha con afectación de los reflejos posturales e inestabilidad.. En algunos pacientes predomina el temblor, mientras que en otros puede comenzar con signos acinético-rígidos.
Cuando la EP está avanzada, los pacientes presentan un importante o notorio trastorno de la marcha, una hipocinesia y bradicinesia ostensibles y temblor de reposo. Además de los 4 síntomas cardinales (temblor, rigidez, bradicinesia y alteración de la marcha y del equilibrio) aparecen otras manifestaciones: Micrografia (escriben con letra muy pequeña e ilegible), pérdida de destreza en las actividades de la vida diaria (vestirse, lavarse…), amimia o cara de máscara, hipofonía (pérdida del volumen de la voz), sialorrea (producción en exceso de saliva), dolores articulares, seborrea, alteraciones autonómicas (estreñimiento, impotencia, hipotensión ortostática…), así como problemas neuropsiquiátricos (depresión, pérdidas cognitivas e incluso demencia, alucinaciones…).
Al principio todos los pacientes responden muy bien a la administración de L- Dopa, pero a partir de varios años de tratamiento estos pacientes presentan fluctuaciones con la medicación, presentando periodos de “on” (función motora buena y desaparición de los síntomas parkinsonianos) o de “off” (función motora pobre y reaparición de los síntomas parkinsonianos). Tras la administración prolongada de L-Dopa a dosis altas los pacientes pueden presentar discinesias durante los periodos “on” que suelen ser coreiformes, pero también pueden ser en forma de distonías, mioclonias u otras alteraciones del movimiento.
DIAGNOSTICO
Se hace sobre todo por los síntomas clínicos que presenta el paciente y la exploración neurológica subsiguiente. Pero es fundamental un correcto diagnóstico que favorezca un adecuado planteamiento terapéutico a largo plazo, que mejore el pronóstico de la enfermedad.
La Resonancia Magnética es clave para detectar parkinsonismos secundarios a otras enfermedades neurológicas.
El PET puede ser también importantes en el diagnóstico y, sobre todo, en el seguimiento: comparando las variaciones en el tiempo de los patrones típicos de aumento de la actividad metabólica en globo pálido y tálamo y la disminución de esta actividad en áreas premotoras corticales.
Hay numerosas escalas que permiten la valoración de un paciente con Enfermedad de Parkinson:
1.- UPDRS (Unified Parkinson’s Disease Rating Scale).
Se valora el estado mental, las actividades de la vida diaria, capacidad motora y complicaciones de la medicación.
2.- Estadíos en la Escala de Hoehn y Yahr :
- I.- Afectación unilateral
- II.- Afectación bilateral
- III.- Afectación moderada bilateral y del equilibrio, pero puede hacer vida independiente.
- IV.- Afectación severa bilateral, pero aún puede caminar y mantenerse en pie sin ayuda.
- V.- Confinado a la silla o a la cama, a no ser que le ayuden.
3.- Medición del tiempo en “on” con o sin discinesias, así como del tiempo en “off”
4.- Tomas de vídeo con reflejo de ejecución de tests motores
5.- Test de L-Dopa : Se deja de dar la medicación durante un periodo de 12 horas y se mide la Escala UDPRS tras recibir la primera dosis matinal de L-Dopa.
TRATAMIENTO
Dado que en la enfermedad de Parkinson se produce una alteración del balance entre varios neurotransmisores, con déficit de la DA y exceso de acetil-colina (ACh) en los núcleos de la base (estriado), el tratamiento se dirige a restaurar este balance dopamina-acetilcolina. Bien aumentando la concentración de DA en los estos núcleos o bien intentando disminuir o bloquear el efecto de la ACh. Entre los fármacos más importantes, hay que destacar:
Fármacos dopaminergicos
Estos pretenden aportar la dopamina que falta, mediante dos mecanismos: llevarla directamente al cerebro (A) o manteniendo el efecto de la acción de la dopamina sobre los receptores neuronales (B).
A.- Levodopa :
La levodopa (L-Dopa) continúa siendo el pilar básico del tratamiento de la enfermedad de la EP idiopática. Al administrarla por vía oral llega al cerebro y allí se transforma en dopamina. Es especialmente eficaz a la hora de revertir la bradicinesia. La asociación a carbidopa (Sinemet® 250/25 o Sinemet Plus® 100/25) o benseracida (Madopar® 200/50), (inhibidores de la dopa decarboxilasa) ha supuesto un importante avance terapéutico, ya que estas sustancias bloquean la metabolización y desaparición de la L-Dopa a nivel del resto del organismo, por lo que llega más al cerebro y de forma más continua y nivelada.
Los principales efectos secundarios periféricos de la dopamina son: vómitos síntomas gastrointestinales, taquicardia e hipotensión ortostática. La administración prolongada de L-Dopa puede acabar produciendo efectos adversos en el sistema nerviosos, como alteraciones psiquiátricas, discinesias y fluctuaciones clínicas: wearing off (disminución del tiempo de beneficio terapéutico) y periodos on-off prolongados o muy rápidamente fluctuantes.
B.- Agonistas dopaminérgicos:
Bromocriptina (Parlodel®), Lisuride (Dopergin®), Ropirinol (Requip®), Pergolida (Pharken®).
Los agonistas dopaminérgicos actúan directamente sobre los receptores dopaminérgicos postsinápticos, no sobre la síntesis ni el almacenamiento presináptico de la dopamina. En este sentido van a acabar obteniendo una respuesta similar a la dopamina, pero sin precisar que exista ésta en las neuronas. Por lo que son útiles en la prevención y tratamiento de las fluctuaciones motoras.
Inhibidores del metabolismo de la DA Selegilina (Plurimen®)
Potencian la acción de la Dopamina al bloquear su degradación metabólica, por lo que se sualen asociar a la L-Dopa y precisar incluso el descenso de la dosis de esta última..
Anticolinérgicos
Trihexifenidilo (Artane®)
Biperideno (Akineton®)
Prociclidina
Su indicación actual está limitado a pacientes jóvenes con enfermedad de inicio y temblor incapacitante. Sus múltiples efectos secundarios (estreñimiento, visión borrosa, mareos y nauseas) limitan su utilización en otros casos.
Amantadine
Su mecanismo de acción se desconoce, aunque parece tener un efecto anticolinérgico y propiedades como antagonista del NMDA (N-metil-D-Aspartato). Es efectivo contra la acinesia y rigidez, pero menos contra el temblor. Su tratamiento se propone en el inicio de la enfermedad.
TRATAMIENTO FARMACOLÓGICO
Hay muchas pautas de tratamiento farmacológico, aunque lo importante es concebir un planteamiento terapéutico para cada paciente, teniendo en cuenta la cronicidad de la enfermedad con la que nos enfrentamos. Una de estas pautas podría ser:
1.- Inicio de la enfermedad:
- – Selegilina
- – Amantadine
- – Anicolinérgicos
2.- Síntomas que comienzan a ser incapacitantes:
- – Agonista dopaminérgico
- – L-Dopa
3.- En casos en los que se precisa controlar los síntomas de forma urgente:
- – L-Dopa
- – Añadir posteriormente agonistas dopaminérgicos
TRATAMIENTO QUIRURGICO
Debido al avance progresivo de la enfermedad así como a la aparición de los importantes efectos secundarios derivados del tratamiento (más del 50% de los pacientes a los 5 años), es preciso otro abordaje terapéutico que dé respuesta a los pacientes con enfermedad de Parkinson avanzada: el tratamiento quirúrgico. La mejor comprensión fisiopatológica, junto con la notable aportación que suponen las nuevas técnicas de neuroimagen (especialmente la resonancia magnética) y de neurofisiología (registro intraoperatorio con microelectrodos, electroestimulación), que permiten una más precisa localización de la diana quirúrgica e incrementan el margen de seguridad de la cirugía moderna, han supuesto un nuevo resurgir de la cirugía estereotáxica de los ganglios o núcleos basales extrapiramidales, para poder dar respuesta al problema que supone la severa limitación que tiene el tratamiento médico en pacientes con muchos años de evolución.
Como se ha visto al hablar de la fisiopatología, la idea principal es disminuir las órdenes inhibitorias que parten desde los núcleos extrapiramidales y que van a bloquear la acción, tanto a los núcleos motores de la médula espinal, como a la corteza cerebral a través del tálamo.
Las principales opciones quirúrgicas son:
1.- Procedimientos ablativos.
Consisten en la producción de una lesión (termolesión o sección con palidotomo) en un núcleo concreto. Se trata por tanto de un procedimiento irreversible. Destacan la palidotomía y la talamotomía (núcleo ventrolateral).
2.- Estimulación cerebral profunda (ECP).
Se implantan electrodos de estimulación crónica, unidos a un generador de pulsos externo (a la manera de un marcapaso cardíaco). La corriente que pasa a través de este electrodo inhibe la actividad neuronal del núcleo donde se ha implantado (tálamo ventrolateral, pálido interno o subtálamo). Su principal ventaja respecto a las técnicas ablativas o lesivas es doble: por un lado, la acción es reversible y, en caso de que no obtengamos beneficios tras la estimulación, se puede retirar el electrodo sin que hayamos dañado el cerebro; por otro lado, posibilita la realización de intervenciones bilaterales, necesarias para muchos pacientes, sin que produzcan los efectos colaterales graves de las lesiones bilaterales. Además, la ECP permite adaptar los parámetros de estimulación a las necesidades de cada paciente, según su eficacia clínica y los posibles efectos adversos que pueda inducir la ECP.
3.- Otras técnicas.
Existen otras técnicas todavía en fase de experimentación pero que aun no tienen aplicación en clínica, como los implantes cerebrales de células fetales o del glomus carotídeo.
En la tabla siguiente se comparan los resultados de las principales técnicas quirúrgicas sobre los síntomas cardinales, así como la existencia de efectos adversos.

Dadas las ventajas indudables de las técnicas de ECP, las técnicas ablativas no se consideran, en general, como primera elección.
Dentro de las técnicas de ECP, la estimulación del núcleo subtalámico es la más efectiva y la más utilizada en la actualidad, por lo que la describiremos en detalle a continuación.
Estimulación subtalámica
El éxito de la cirugía estereotáxica se basa en la localización estricta de la zona diana y en la ejecución precisa de la lesión o colocación del electrodo de estimulación. Para ello se requieren 3 etapas fundamentales: 1) estimación anatómica de la diana quirúrgica (mediante empleo de guía estereotáxica y neuroimagen); 2) registro neurofisiológico y 3) lesión o implantación del electrodo de estimulación. Para una correcta implantación de electrodos en el núcleo subtalámico, se siguen estos procedimientos:
A.- Determinación de las coordenadas del núcleo subtalámico.
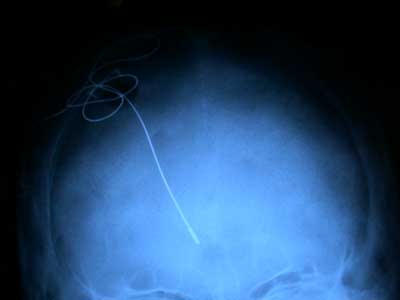
Para ello es necesario colocar el marco de la guía estereotáxica (Leksell u otra cualquiera y adecuada) en la cabeza del paciente, que se fija por medio de 4 tornillos al cráneo, empleando anestesia local. Este marco no es otra cosa que un sistema de referencia que nos permite situar en el espacio tridimensional cada región del cráneo y cerebro del paciente. Para ello, se emplean técnicas de neuroimagen como el TAC helicoidal, la RM y la ventriculografía que es una técnica más antigua pero que introduce menor distorsión en la determinación de los puntos de referencia (Fig.2).
B.- Comprobación de la localización anatómica: estudio neurofisiológico.
A pesar de las diferentes técnicas de neuroimagen, diversos grupos con gran experiencia han demostrado que existe una significativa discrepancia entre los blancos o dianas teóricos y la situación final de los electrodos de ECP. Por esta razón, el éxito de cualquier procedimiento quirúrgico para la ECP depende todavía y en última instancia de la caracterización neurofisiológica.
Esta técnica consiste en introducir un pequeño electrodo metálico hasta la zona que se desea registrar y estimular, ya que el mismo electrodos se puede utilizar para ambas acciones (Fig.3). El electrodo va soportado sobre el arco de la guía estereotáxica y dirigido hacia el punto diana. Poco antes de llegar a éste, el electrodo se va introduciendo gracias a un micromanipulador que lo puede ir avanzando a pequeños intervalos de distancia de incluso 1 micra. Este tipo de electrodo tiene una punta finísima (microelectrodo) que permite detectar la actividad de una neurona u un pequeño grupo de neuronas. Los electrodos están fabricados con metal (platino-iridio o tungsteno) y están aislados por medio de una capa generalmente plástica (kapton o epoxilita), mientras que la punta, de unos 5-20 µm está aislada por medio de vidrio.
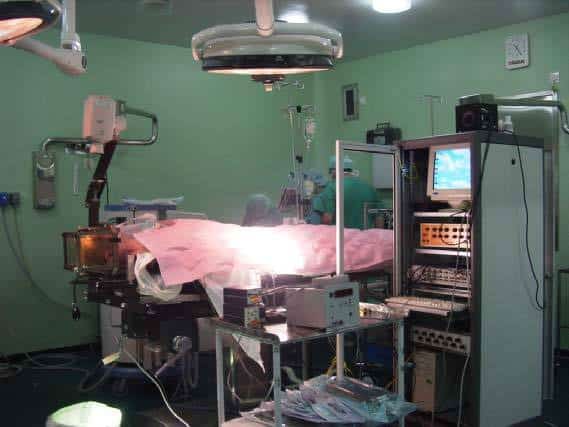
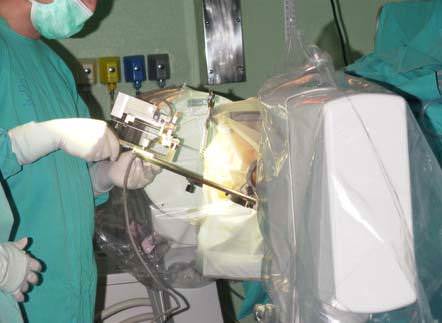
El estudio con microelectrodos pretende identificar, por medio de las características electrofisiológicas diferentes de cada núcleo, cual es el núcleo exactamente registrado. De este modo podemos estar seguros de que se trata del núcleo subtalámico. Además, por medio de métodos de activación (realización de movimientos voluntarios e involuntarios) podemos situar el electrodo en la región del núcleo que corresponda a la parte del cuerpo más afectada, lo que supone una gran especificidad en el tratamiento.
La microestimulación, tras la fase de registro con microelectrodos, permite definir más precisamente la zona registrada por medio de la observación de los efectos fisiológicos evocados. La estimulación puede realizarse básicamente de dos formas: pasando corriente, para lo que se precisa un sistema de aislamiento (SIU), o bien estableciendo una caída de potencial a través del electrodo. En nuestra opinión, este sistema es desaconsejable, debido a que los cambios de impedancia pueden modificar la corriente que se aplica. Los parámetros de los pulsos son:
Duración de los pulsos: 60-100 µs.
Intensidad (mA): menor de 1 mA
Frecuencia: 100-200 Hz.
La estimulación puede evocar parestesias, cuando se estimula el lemnisco lateral (cuando el electrodo es medial y dorsal), o contracciones musculares, si se estimula la vía corticoespinal (electrodo muy lateral). Cuando el electrodo se sitúa en al sustancia negra, la corriente puede propagarse hasta el III par, originando movimientos oculares. Un criterio útil para identificar la localización errónea del electrodo consiste en observar la presencia de parestesias o actividad motora cuando las frecuencias de estimulación son bajas (10-20 µA, 300 Hz, 200 µs).
C.- Implantación del electrodo.
Una vez que se ha determinado el lugar óptimo de implantación del electrodo, se retira el micro electrodo y se coloca en su lugar el electrodo de ECP (Medtronic®). Antes de proceder a la implantación definitiva, se vuelve a comprobar que no se observan efectos secundarios durante la estimulación (macroestimulación), pasando pulsos monopolares de 60 µs, a una frecuencia de 130 Hz y comprobando los electrodos más extremos en ambas direcciones, con un voltaje mínimo de 4 V.
El electrodo se deja totalmente subcutáneo y se conecta a una prolongación que se hace aflorar a la piel, tras un recorrido por debajo del cuero cabelludo, de forma que disminuya los riesgos de infección.
D.- Test de función.
Terminada la intervención, el paciente es mantenido bajo profilaxis antibiótica y, a partir de las 24horas, se inicia un periodo de prueba durante el cual se procede a estimular los diferentes contactos del electrodo implantado y observar los efectos beneficiosos o adversos (si los hubiere), a la vez que se maneja adecuadamente las pautas de medicación habitual del paciente.
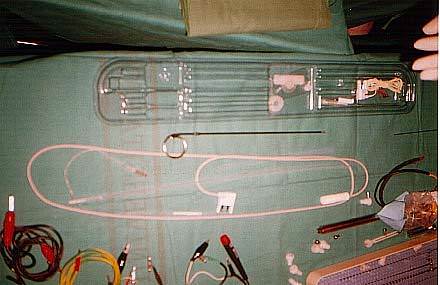
E.- Implantación definitiva del sistema.
En caso de que el resultado de la estimulación fuera satisfactorio, para el paciente y tras los tests adecuados neurológicos, a los 4-6 días se programa al paciente para una segunda intervención (bajo anestesia general). En ésta se procede a la implantación definitiva del sistema generador de pulsos, que se sitúa en el tejido subcutáneo de la región infraclavicular del mismo lado, conectado al electrodo intracerebral. A partir de las 24 horas se vuelve a probar el tipo de estimulación y contactos más eficaces en reducir la clínica del paciente sin producir ningún efecto secundario. Este proceso de ajuste suele llevar unos 2 a 4 días, utilizando un equipo que permite variar en el generados implantado los parámetros y contactos a estimular mediante telemetría. El paciente es dado de alta una vez esté ajustada la medicación y pauta de estimulación, aunque posteriormente en las revisiones sucesivas se procede a ir reajustando aún mejor éstos, de acuerdo con la actividad y necesidades reales diarias del paciente.
Cualquiera de los cuatro contactos del electrodo puede ser utilizado para estimulación monopolar (con el generador de impulsos actuando como ánodo), y dos contactos o más pueden ser elegidos en combinación para la estimulación bipolar. La duración del impulso, la amplitud y la frecuencia de estimulación, así como la selección de contactos activos y el modo de estimulación (monopolar o bipolar), son manipulados por el médico mediante una unidad externa de programación. De forma adicional, el paciente puede conectar o desconectar el estimulador aplicando un imán sobre la región subclavicular. Los parámetros habituales en el caso de la EP presentan los siguientes rangos:
Duración del pulso : 60-90 µ
Voltaje : 2-3.5 V
El ajuste dependerá de cada paciente, teniendo en cuenta la evolución clínica, la existencia de posibles efectos secundarios y los valores de determinados parámetros físicos de gran importancia como la impedancia de los electrodos, la densidad de carga o la corriente media por fase, que imponen serias restricciones a la estimulación para garantizar la seguridad del paciente.
En cuanto a los resultados clínicos de la estimulación, la mejoría supera el 60% global en la UPDRS III (subescala motora) en off . Los mejores resultados se dan, en orden decreciente, sobre el temblor, la rigidez, la marcha e inestabilidad postural y la bradicinesia. Adicionalmente se ha observado una mejoría en on del 30%. Además, en la estimulación del núcleo subtalámico se ha obtenido un resultado igualmente muy satisfactorio sobre las discinesias y las fluctuaciones motoras on/off, así como sobre los rebeldes episodios de freezing o congelación de la marcha, permitiendo además una reducción de la dosis de fármacos de un 40-50%.
Las complicaciones asociadas con la estimulación de dicho núcleo se pueden diferenciar entre aquellas debidas al procedimiento quirúrgico, las debidas a la estimulación y las que están relacionadas con el equipo técnico. La complicación más seria (al igual que en otras técnicas estereotáxicas) es la hemorragia intraparenquimatosa que ocurre en un 1-3%. Se han observado episodios de confusión transitoria y agitación psicomotriz, intra y postoperatorios, más frecuentes en pacientes de mayor edad, así como, rara vez, trastornos en la memoria, dificultad para la concentración y cambios de personalidad.
Los efectos adversos inducidos por la estimulación incluyen apraxia en la apertura palpebral, diplopia, parestesias y movimientos involuntarios (corea), la mayoría de los cuales se suelen solventar ajustando la programación. Es rara la aparición de hemibalismo (suele ser transitorio).
Las complicaciones inherentes al equipo de estimulación (1-3%) pueden ser la migración del electrodo, su rotura o desconexión, erosiones en la piel y fallo del equipo. La infección se ha descrito en un 5% de los casos.
En conclusión, a pesar de la complejidad técnica de la estimulación crónica bilateral del núcleo subtalámico, así como los posibles efectos adversos descritos, sus beneficios globales en los pacientes parkinsonianos seriamente afectados, superan claramente el coste de estas dificultades. Esta técnica supone, hoy por hoy, la mayor posibilidad de obtener una mejoría definitiva de todos los síntomas motores incapacitantes en estos pacientes con EP avanzada.
El resultado obtenido en la enfermedad de Parkinson, gracias a la estimulación del núcleo subtalámico, está trasladándose a las otras enfermedades con trastornos motores extrapiramidales, referidas anteriormente en la clasificación de la OMS. De forma que, por ejemplo, en el temblor esencial se está cambiando de diana y sustituyendo el núcleo ventral intermedio (Vim) por el subtalámico y probablemente ocurra lo mismo con las distonías, hasta ahora tratadas mediante estimulación del pálido interno.
Con la estimulación cerebral profunda se ha abierto, por tanto, un camino de actuación sobre el sistema extrapiramidal, que pretende obtener de nuevo un balance excitador-inhibidor que compense los síntomas tan discapacitantes que llegan a producir este tipo de enfermedades. Su gran ventaja es que no provocan destrucción de ninguna estructura, de forma que dejan el sistema nervioso inalterado y las posibilidades abiertas a cualquier otro tipo de actuaciones futuras (como puede ser el implante celular o la microadministración selectiva de fármacos).
El hecho de que estas nuevas perspectivas precisen al menos 5-10 años hasta que puedan ser aplicadas con éxito, junto a los resultados muy satisfactorios de la estimulación del núcleo subtalámico, no deja lugar a dudas de que en el momento actual no debe prolongarse el tratamiento médico en estos pacientes si comienza a ser ineficaz, sin proponerles esta nueva posibilidad terapéutica quirúrgica.


Mi madre tiene implantado el electrodo desde el 2004.todo ha ido muy bien hasta que en un cambio de bateria ,empezo a ponerse roja la zona y tuvieron que sacar el aparato colocadi en la clavicula y los cables .no el electrodo.por una infeccion.le han puesto sonda gasogastrica con bomba de levodopa.carbidopa.y no va bien.mi madre estaba muy bien con la estimulacion craneal profunda.hacia vida casi normal.ahora no puede andar.ni reir.ni comer.lleva pañal.y casi no habla.lo unico que hace es llorar.y no nos han dado muy buenas expectativas de volver a implantar el estimulador.en el ramon y cajal.por pequeñas costritas… Leer más »