Tema 11 – Epilepsia y el sueño
Dr. Virgilio Hernando Requejo
Neurociencias
Otros trabajos del Dr. Virgilio Hernando
Ver presentación Epilepsia y sueño
EPILEPSIA
Definiciones
Crisis comicial: manifestación clínica de una sincronización anómala y excesiva de una población de neuronas corticales
Epilepsia: tendencia a la repetición de crisis comiciales no producidas por desencadenantes sistémicos o neurológicos
Epileptogénesis: secuencia de procesos que dan lugar a que el tejido neural normal se vuelva hiperexcitable
Neurofisiología de la corteza
La corteza cerebral humana consta de 3-6 capas de neuronas
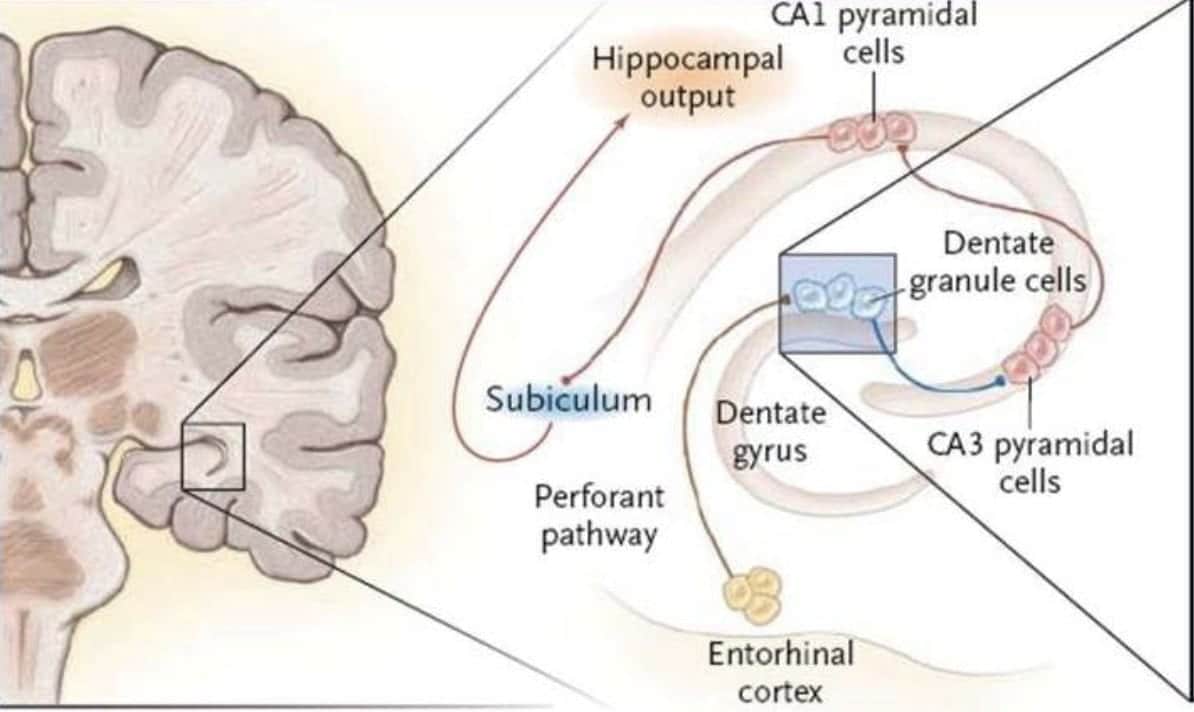
La corteza más antigua filogenéticamente (archicortex, tres capas): hipocampo, estructura cortical temporal mesial muy relacionada con los fenómenos epilépticos:
- – Subilculum (transición a las 6 capas)
– Asta de Ammon (CA1, CA2, CA3)
– Giro dentado
Dos clases de neuronas:
- De proyección (por ej. piramidales), por lo general excitadoras
Interneuronas (por ej. neuronas en cesta), por lo general inhibidoras de las de proyección o de otras interneuronas inhibidoras
Una neurona de proyección excitada sinapta con sus interneuronas, que inhibirán a las de proyección de la vecindad
Algunas interneuronas tienen axones largos, y podrían funcionar como “marcapasos” de activación neuronal)
Bases de la excitabilidad
La excitabilidad favorece la despolarización mediante:
- Neurotrasnsmisión excitatoria aumentada
Neurotransimsión inhibitoria disminuída
Alteraciones en los canales iónicos voltaje dependientes
Alteraciones iónicas intra o extracelulares
Estímulos repetitivos síncronos subumbrales
Mecanismos de génesis de crisis
Excitación excesiva:
- Iónica: entrada de Na+, Ca++
Neurotrans: glutamato, aspartato
Inhibición insuficiente:
- Iónica: entrada de Cl-, salida de K+
Neurotrans: GABA
Factores que intervienen en la excitabilidad de las neuronas
(Mecanismos de control del nivel de activación neuronal
Intraceclulares (intrínsecos):
- Tipo, nº y distribución de los canales voltaje o ligando dependientes
Cambios bioquímicos en los receptores (por ej. la fosforilación de los NMDA aumenta la excitabilidad)
Activación de sistemas de segundo mensajero
Modulación genética (expresión particular de diversos receptores)
Extracelulares:
- Neuronas vecinas
Glía (buffer)
Espacio extracelular (concentraciones iónicas; por ej. la disminución del volumen extracelular aumenta el K y se dificultará su salida para la repolarización)
Sinápticos:
- Receptores: cambios en la densidad, conductancia o en la capacidad de unirse al neurotransmisor
Remodelación de los contactos sinápticos (depende de dónde se produzcan habrá mayor o menor excitabilidad)
Cambios en el metabolismo del neurotransmisor, por ej. por parte de la glía
Cómo la actividad de redes neuronales aumentan la excitabilidad neuronal
Las redes neuronales asumen “a otro nivel” el control de la actividad de cada neurona
En el giro dentado, las aferencias a la red neuronal activan directamente la neurona de proyección (célula granular en el hipocampo). Pero también activan interneuronas (células bipolares y células en cesta), que inhibirán a las neuronas de proyección vecinas (feed-forward inhibition).
La célula granular, a su vez, activará interneuronas, que serán sus inhibidoras (feedback inhibition).
Fenómeno de sprouting: se generan múltiples axones excitatorios, de modo que “desequilibran la balanza”
También puede ocurrir lo contrario: pérdida de neuronas inhibitorias
Causas de epilepsia
Hereditarias (por ej. canalopatías) Adquiridas (las más frecuentes):
- TCE
Hemorragia cerebral
Tumor cerebral
Infección SNC
¿Crisis febriles?
» Entre al noxa y la primera crisis pasa un periodo de latencia de maes/años durante el cual se produce la epileptogénesis»
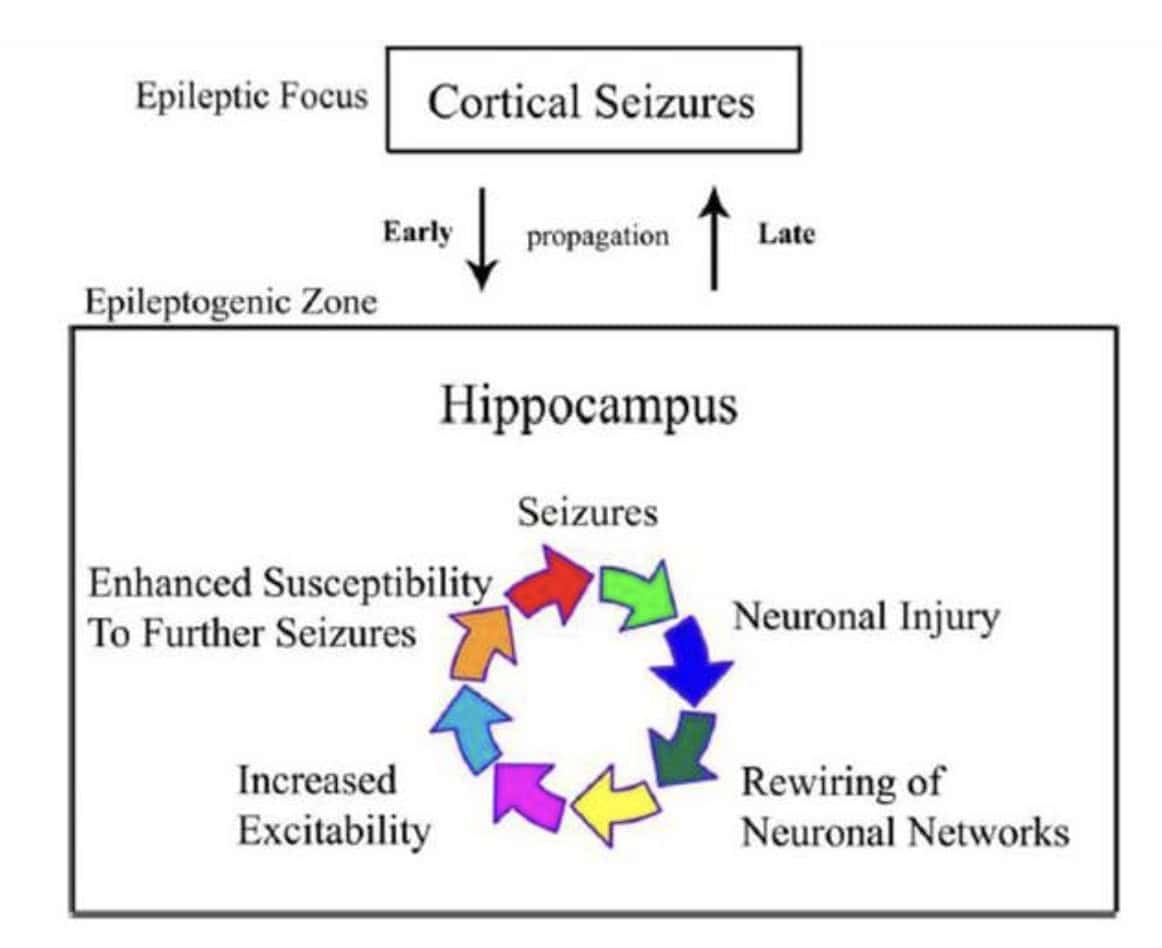
Epileptogénesis a partir del daño neuronal
Múltiples procesos celulares (en las epilepsias genéticas un único canal iónico alterado puede explicar todo el trastorno, en las adquiridas no)
Cambios progresivos en los canales iónicos voltaje y ligando dependientes que generan hiperexcitabilidad
Alteración de la conectividad sináptica
La primera crisis facilitará la siguiente (“la pescadilla que se muerde la cola”)
Kindling
Epileptogénesis producida por descargas subumbrales a una frecuencia adecuada en hipocampo y amígdala
Se ha demostrado en la rata y en otras especies animales, pero con mayor dificultad a medida que se asciende en la escala filogenética; no ha podido evidenciarse en humanos
ALTERACIONES DEL SUEÑO
Introducción
El sueño es un estado fisiológico en el que el nivel de vigilancia está disminuido y el individuo descansa
La fisiología del sueño es tan compleja como la de la vigilia en su regulación neurológica, endocrina, metabólica o cardiorrespiratoria.
El estado de sueño puede sufrir alteraciones por motivos físicos o psíquicos, que ocasionen trastornos potencialmente graves.
Anatomía y fisiología del sueño
Cuando predomina el sistema activador reticular el individuo está alerta (actividad tónica de las neuronas catecolaminérgicas y colinérgicas).
Cuando su influencia decae los sistemas inhibidores inducen el estado de sueño.
Contribuyen a la vigilia:
- Proyecciones histaminérgicas y peptidérgicas del hipotálamo posterior
Actividad de los sistemas visual y auditivo
Sustancias endógenas y exógenas (por ej. catecolaminas)
Dos grandes tipos de sueño:
Sueño lento (sin movimientos oculares rápidos o NREM)
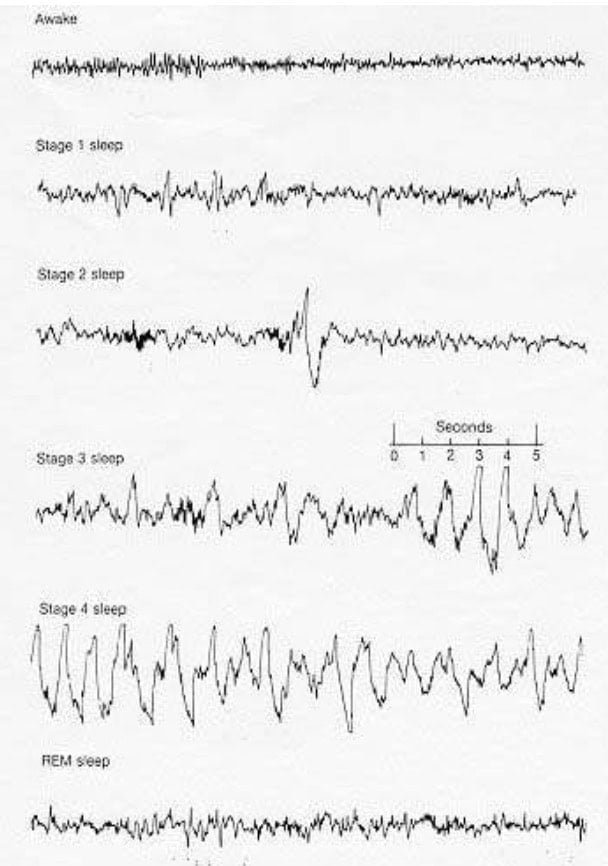
- Se distinguen las fases I, II, III y IV, según la actividad progresivamente más lenta del EEG
El tono muscular persiste y los movimientos oculares son lentos y esporádicos
Respiración profunda y regular
El sueño rápido o paradójico (con movimientos oculares rápidos o REM):
- Actividad del EEG similar a la de vigilia, hipotonía muscular y movimientos oculares rápidos y en salvas
Respiración irregular
Durante el sueño REM hay erecciones de los órganos genitales y ocurre la actividad onírica (los ensueños)
Fase I: transición desde la vigilia al sueño. Desaparición del patrón regular α (alfa) e instauración de un patrón de amplitud baja y de frecuencia mixta, predominantemente en el intervalo theta (2 a 7 Hz), con movimientos oculares lentos «en balancín»
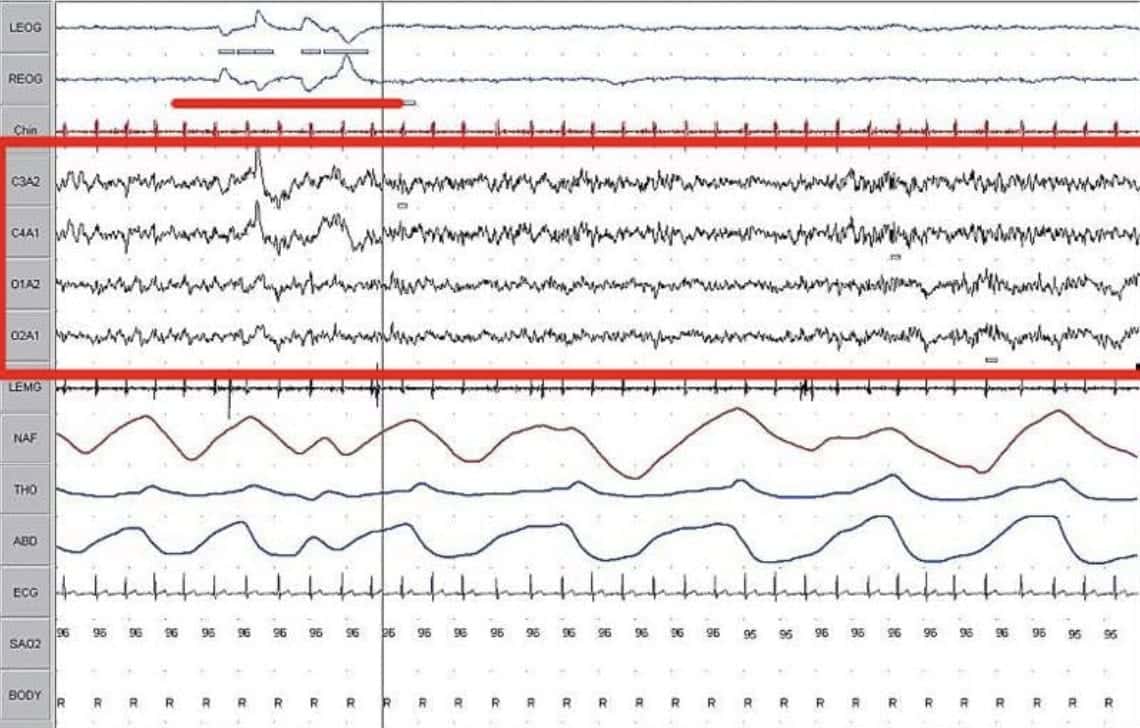
Fase II: complejos K y husos de sueño superpuestos a una actividad de base ≈ fase I. Los complejos K son descargas lentas, negativas (hacia arriba) y de amplitud elevada que se continúan inmediatamente después por una deflexión positiva (hacia abajo). Los husos de sueño son descargas de alta frecuencia de corta duración que presentan una amplitud característica con subidas y bajadas. No hay actividad ocular y el EMG ≈ fase I
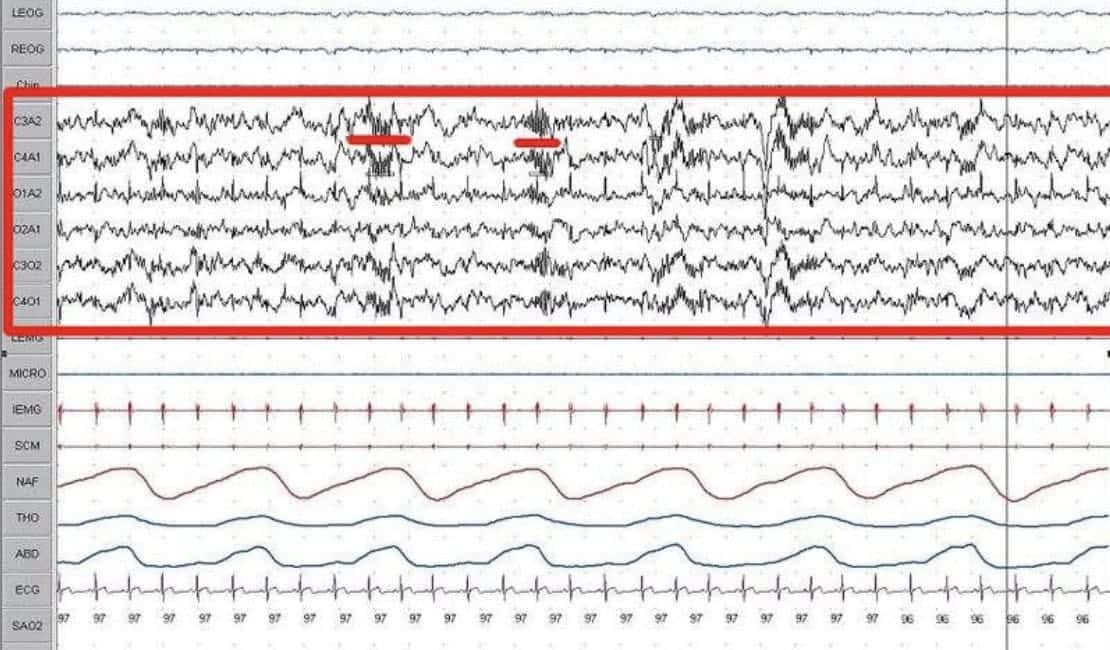
Fases III y IV: sueño con más del 20% (fase III< 50%, fase IV>50%) de actividad delta de amplitud elevada (> 75 microV)(0,5 a 2 Hz). Los husos del sueño pueden persistir, sigue sin haber actividad ocular, y la actividad del EMG permanece en un nivel reducido
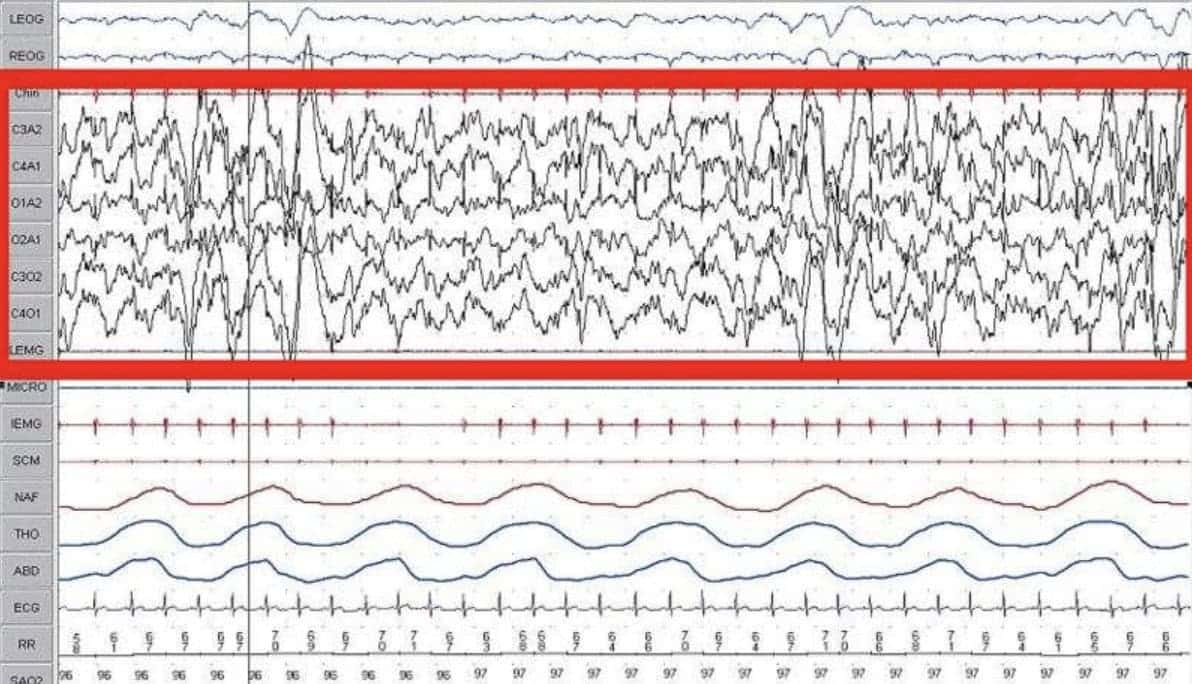
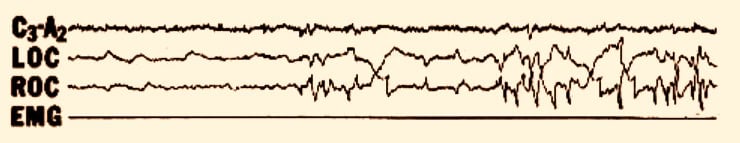
Fase REM, o «sueño paradójico“: EEG de baja amplitud y de frecuencia mixta ≈ fase I. En este contexto, se producen brotes de actividad más lenta (3 a 5 Hz) con deflexiones negativas superficiales («ondas en diente de sierra») que se superponen con frecuencia a este patrón. El EOG da muestras de MOR similares a las que se observan cuando la persona en cuestión permanece despierta y con los ojos abiertos. La actividad del EMG permanece ausente reflejando la atonía muscular completa de la parálisis motora descendente característica de este estado.
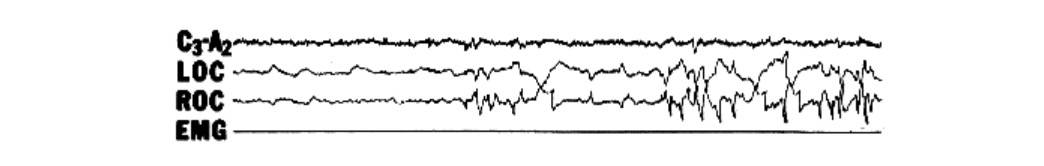
Organización del sueño fisiológico
Ciclos de 90-120 min (4-5 en 8 horas)
Fase I: 5 % del tiempo total de sueño
Fase II: 25 %
Fases III y IV: sueño lento, 45 %
REM: 25 %
Trastornos del Sueño y de la vigilia: Insomnios
Síndromes con dificultad para iniciar o mantener el sueño nocturno.
En >60 % la causa es psicofisiológica, psiquiátrica o asociada a fármacos y drogas.
Ansiedad: insomnio de conciliación
Depresión: despertar precoz.
Los hipnóticos y el alcohol aumentarán el sueño, pero a costa de reducir o suprimir las fases IV y REM y de riesgo de tolerancia y dependencia.
Insomnio asociado a movimientos anormales en las piernas:
- Síndrome de las piernas inquietas
Mioclonía nocturna: contracción tónica prolongada que afecta sobre todo los extensores del pie y del muslo y que aparece periódicamente durante la noche
Insomnio en los ancianos:
- Fragmentación y reducción fisiológicas del sueño
Suelen asociarse problemas físicos de otro origen (que provocan, por ej., dolor) y trastorno del ánimo
Insomnio en las enfermedades neurológicas
- Las lesiones en la región posterior del hipotálamo y la parte superior del tronco producen letargo, y las lesiones en el área preóptica y de la región protuberancial medial e inferior, insomnio
Las lesiones en el hipotálamo provocan también una disrupción otrosritmos circadianos (temperatura, atención, secreción hormonal)
Muchas enfermedades neurológicas dificultan el sueño:
- Enfermedad de Parkinson
Pacientes hemipléjicos por la inmovilidad Pacientes parapléjicos por los espasmos musculares,
Polineuritis o en la neuralgia postherpética o del trigémino por las crisis de dolor
Deterioro cognitivo
Trastornos del horario (o programa) vigilia-sueño:
Transitorios: jet lag, cambio de turno de trabajo, “trasnochar”.
Si los cambios frecuentes de horario de sueño se mantienen durante mucho tiempo pueden originar alteraciones persistentes del ciclo vigilia-sueño y trastornos orgánicos:
- Mayor adicción al alcohol y a los fármacos Úlcera péptica
Arritmias cardíacas Dismenorreas
Cefaleas y otros trastornos «psicosomáticos»
Retraso o avance del comienzo del sueño o un ciclo circadiano diferente al habitual de 24 horas: “cronoterapia”, para retomar el ritmo circadiano normal
Narcolepsia
- Etiología desconocida
Presentación familiar en el 6-52 %; generalmente herencia dominante con penetrancia incompleta Existe una estrecha relación con los antígenos de
histocompatibilidad HLA-DR2 y HLA-DQw1, presentes en
prácticamente el 100 % de los pacientes
Mala regulación del sueño REM: hipersomnia (excesiva somnolencia)
El síndrome completo incluye cuatro manifestaciones:
- Crisis de sueño diurno (100 % de los casos) Crisis de cataplejía (68 %) Alucinaciones hipnagógicas (30 %) Parálisis del despertar (24 %)
La combinación de las tres primeras está presente en >50% de los pacientes, aunque el síndrome completo puede tardar hasta 20 años en instaurarse.
Suele debutar en la 2ª o 3ª décadas
El sueño nocturno suele estar alterado
Las crisis de sueño (REM):
- Precipitadas por: calor, comida (sobre todo dulces o hidratos de carbono), viajes, actividades monótonas y cansancio; también pueden presentarse en plena actividad
Las siestas suelen ser breves (10-30 min) pero en casos especiales, por ejemplo, mujeres durante la menstruación, puede durar varias horas
En general, tras una crisis, el paciente se despierta despejado y descansado y suele disponer de un rato o unas horas de resistencia al sueño, en las que puede planificar una mayor actividad (p. ej., conducir).
No es infrecuente que los individuos narcolépticos tengan episodios de amnesia y conducta automática asociados a un estado de subvigilancia muy prolongado
Las crisis de cataplejía:
- Hipotonía brusca que puede afectar los elevadores de los párpados, maseteros, músculos cervicales, músculos antigravitatorios de las piernas o elevadores de los brazos e, incluso, todos ellos
Se desencadena por un estímulo de sorpresa, agradable o desagradable, la risa, el enfado
El paciente nota que se le caen los párpados, la mandíbula o la cabeza hacia adelante o que se le aflojan los brazos y las piernas y puede llegar a caer al suelo y lesionarse.
Aunque el paciente esté inmóvil no tiene trastornos respiratorios ni de los movimientos oculares
Las alucinaciones hipnagógicas:
- Impresiones visuales muy vívidas con una sensación de intenso realismo, generalmente de caras o figuras en movimiento desordenado, a veces acompañadas de impresiones auditivas
Aparecen sobre todo en el adormecimiento del sueño nocturno o de las crisis de narcolepsia
Las parálisis del despertar (base fisiopatológica común con las crisis de cataplejía): el individuo, que ya ha recuperado la conciencia tras el sueño nocturno o la siesta, tiene la impresión de no poder moverse durante unos segundos (aunque pueden durar varios minutos)
Diagnóstico:
- Anamnesis Polisomnografía
Test de latencias múltiples HLA
Hipocretina en LCR
Descartar que la hipersomnia sea sintomática de otra enfermedad endocrina, respiratoria o del SNC
Tratamiento:
Para la narcolepsia:
- Una o dos siestas programadas al día
Apoyo psicológico
Metilfenidato (10-60 mg/día)
Modafinilo
Para la cataplejia:
- Antidepresivos tricíclicos: clomipramina (60-100 mg/día) o amitriptilina (25-75 mg/día)
Inhibidores de la recaptación de serotonina
Hipersomnia idiopática “del sistema nervioso central”
- Síndrome frecuentemente familiar (asociación al antígeno HLA-Cw2)
Crisis de sueño NREM durante el día y sueño nocturno muy prolongado (> 9 horas)
Debe excluirse un síndrome de apneas nocturnas, una lesión orgánica cerebral del tronco cerebral o del diencéfalo, un estado depresivo, hipotiroidismo, estado de postinfección ocasionado por virus de Epstein-Barr u otras causas de hipersomnia
Síndrome de Kleine-Levin
Síndrome idiopático raro y con frecuencia autolimitado Adolescentes (la relación varón/mujer es de 4:1)
Episodios periódicos de somnolencia durante los que duermen muchas horas, asociados a un apetito desordenado y alteraciones de conducta, en particular irritabilidad e hipererotismo.
Las anfetaminas pueden mejorar la somnolencia, pero empeoran la conducta
Síndrome de apneas del sueño
- Cambios fisiológicos nocturnos: postura en decúbito, elevación del diafragma, caída hacia atrás de la lengua, disminución del tono muscular, de la sensibilidad del centro respiratorio y del reflejo de la tos:
- Menos de 30 apneas centrales <10 sg no es patológico Roncopatía simple: vibración de las paredes hipotónicas de la faringe y del velo del paladar
Las apneas pueden aumentar por:
Enfermedades pulmonares
Obstrucción parcial de las vías respiratorias
Debilidad neuromuscular
Lesiones cerebrales que disminuyen la sensibilidad del centro respiratorio
Fármacos
Tres tipos de apnea
Centrales por depresión del centro respiratorio (raras):
- Prematuridad
Arnold-Chiari
Otras lesiones bulboespinales (infecciosas, vasculares)
Fármacos (barbitúricos, alcohol)
Obstructivas, en las que la vía respiratoria queda bloqueada pero persisten los movimientos ventilatorios de la pared torácica, con aumento de la presión intratorácica:
- Macroglosia
Hipertrofia de la úvula y del paladar blando
Engrosamiento de las amígdalas y las adenoides
Obstrucciones nasales
Obesidad con cuello corto
Quistes y tumores que obstruyen las vías respiratorias.
Mixtas
Apneas
Los elementos fisiopatológicos fundamentales del síndrome de apneas del sueño son la hipoxia y la hipercapnia, que conducen a:
- Hipertensión arterial
Hipertensión pulmonar con cor pulmonale crónico
Arritmias cardíacas
Posibilidad de muerte súbita durante el sueño (y síndrome de la muerte súbita del lactante)
Apnea – Clínica:
- Hipersomnia diurna
Insomnio (más frecuente si predominan las apneas centrales)
Episodios de conducta automática y amnesia por la noche
Enuresis y caídas de la cama en un adulto Cefalea matutina
Disminución del rendimiento escolar o laboral Impotencia sexual
Irritabilidad y trastornos de humor
Apnea – Diagnóstico:
Poligrafía (movimientos torácicos, respiración nasal, oximetría)
Apnea – Tratamiento:
Medidas higiénicas, dieta, ejercicio físico
Corrección quirúrgica de las posibles obstrucciones (amígdalas, adenoides, paladar, nasales, etc)
Uveofaringopalatoplastia: tratamiento más radical que mejora más el ronquido que las apneas
CPAP (presión positiva continua en vía aérea)
Trastornos del Sueño y de la vigilia: Parasomnias
Fenómenos episódicos que ocurren durante el sueño Benignas, con gran incidencia infantil y familiar
Buen pronóstico en la mayoría de los casos
Peor pronóstico si aparecen en un adolescente o adulto que no las ha sufrido previamente o que las tuvo en la infancia y reaparecen (expresión de estados psicopatológicos que requieren un tratamiento especializado)
Dos grupos:
- Fenómenos propios y exclusivos del sueño
Trastornos que también ocurren durante la vigilia pero que se agravan durante el sueño y pueden llegar a alterarlo
Pesadillas:
- Ensueños desagradables
Propias del REM, especialmente al final de la noche
Pueden acompañarse de cierta hiperactividad autónoma
El individuo recuerda bien el contenido angustioso del ensueño
Terrores nocturnos:
Propios de NREM, generalmente en el primer tercio de la noche. Muy frecuentes en niños
El paciente:
- Se incorpora en la cama dando un grito y con los ojos abiertos comienza a vocalizar una visión terrorífica con gran descarga vegetativa
No conecta con el ambiente a pesar de la apariencia de estar despierto
Tras un rato de agitación se calma, se duerme y no recuerda nada al día siguiente
Sonambulismo (asociado con frecuencia a somniloquia):
- Durante el sueño NREM
Breves episodios de conducta automática en un estado aparente de vigilia pero sin relación con el ambiente
El individuo se sienta o se levanta de la cama, camina, se pone o quita alguna prenda de ropa y vuelve a la cama, o tiende a salir de la habitación por la puerta o por la ventana (es conveniente colocar pestillos de difícil acceso o alarmas)
Enuresis:
- En sueño NREM o REM
En algunos pasa de los 4-5 años y llega a la adolescencia
La enuresis primaria no tiene una base psicopatológica aunque se exacerbe durante períodos de tensión nerviosa como los exámenes, por lo que no está indicado un tratamiento psiquiátrico
Siempre desaparece con la edad
Movimientos rítmicos:
- Rechinar los dientes, balancear la cabeza o el tronco
Son muy frecuentes en los niños, transitorios, y no requieren tratamiento
“Paseos nocturnos”
- Remedan al sonambulismo pero ocurren durante la fase II del sueño
Responden al tratamiento con carbamazepina o fenitoína, por lo que no se ha descartado su posible origen epiléptico
Sueño REM sin atonía:
- En pacientes con lesiones del tronco cerebral, idiopático, e Parkinson Durante la fase REM el individuo no está hipotónico e inmóvil sino que presenta una conducta agitada, aberrante y agresiva
Responde al clonazepam
Tratamiento:
Las pesadillas, los terrores y el sonambulismo si son muy intensos y frecuentes: diazepam
Enuresis: imipramina, vasopresina (sólo se recomiendan en niños mayores y en situaciones puntuales -campamentos escolares, fines de semana fuera del hogar, etc-)